 typ av folder som betyder, klicka på rubrik - öppnar flik med info
typ av folder som betyder, klicka på rubrik - öppnar flik med info  typ av folder som betyder, klicka på rubrik - stänger flik med info
typ av folder som betyder, klicka på rubrik - stänger flik med info Till rubrik kan det finnas underrubrik, klicka på samma sätt där för att
öppna
 eller stänga
eller stänga  flik med info.
flik med info. | Loading .... [/produkt/html/data/m-chemp.php] .... ok |
 typ av folder som betyder, klicka på rubrik - öppnar flik med info typ av folder som betyder, klicka på rubrik - öppnar flik med info  typ av folder som betyder, klicka på rubrik - stänger flik med info typ av folder som betyder, klicka på rubrik - stänger flik med info Till rubrik kan det finnas underrubrik, klicka på samma sätt där för att öppna  eller stänga eller stänga  flik med info. flik med info. |
Inom kemin är baser en grupp kemiska föreningar med i allmänhet lutaktig smak, som har förmågan att uppta vätejoner varvid de i en vattenlösning ger ett pH-värde över 7, eller mer allmänt, avge elektronpar. En sådan lösning kallas basisk, eller alkalisk. Starka baser är frätande. Baser som är lösliga kallas alkalier om de innehåller och avger hydroxidjoner (OH-). Styrkan av en bas kan relateras till dess baskonstant. En bas kan tillsammans med en korresponderande syra (ett syra-baspar) bilda ett buffertsystem. Exempel på vanliga baser är natriumhydroxid (NaOH) och ammoniak (NH3). Metalloxider, hydroxider och speciellt alkoxider är basiska och motanjoner av svaga syror är svaga baser. Baser kan ses som den kemiska motsatsen av syror. En reaktion mellan en syra och en bas kallas för neutralisation. Baser och syror är motsatser eftersom en syras effekt är att öka koncentrationen av hydroniumjoner (H3O+) i vatten, medan baser minskar koncentrationen. Baser och syror finns vanligtvis i vattenlösningar. Dessa lösningar av baser reagerar med vattenlösningar av syror och skapar därmed vatten och salter i lösningarna. Referens = Litteratur om kemiska hälsorisker [chemfile() chemdata.dat (efter *)] [chemfile(), nC=0 nr=alkali, f1=/produkt/info/html/alkali.htm] Alkalier är ämnen som då de löses i vatten gör vätskan alkalisk (höjer pH-värdet). Alkalisk (basisk) är motsatsen till sur. Starkt alkaliska lösningar är starkt frätande, t ex koncentrerade vattenlösningar av natriumhydroxid (lut). Andra exempel på alkalier är kalciumhydroxid och kaliumhydroxid. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument]
Ammoniak (NH3) är en gas med stor industriell användning. Den är lättlöslig i vatten. Vattenlösningen, som också kallas för ammoniak eller ibland ammoniumhydroxid, avger ammoniakångor som verkar irriterande och höga halter är frätande på andningsvägar, ögon och hud. Ammoniak i höga halter kan bilda explosiva blandningar med luft. Vid kontakt mellan ammoniak och klor, brom, jod eller kvicksilver kan det bildas ytterst stötkänsliga explosiva ämnen. Vattenlösningar av ammoniak reagerar med zink, aluminium eller lättmetaller och bildar vätgas. Vätgas bildar med luft explosiva blandningar. Ammoniak reagerar också våldsamt med syror. Stänk av koncenterad ammoniak fräter på huden och ger upphov till rodnad, blåsor och sår. Ångor av ammoniak är starkt irriterande för ögonen. Höga halter ammoniakångor eller stänk i ögonen av ammoniaklösning kan ge bestående ögonskador. Ammoniakångor irriterar och fräter på andningsvägarna. Inandning av högre halter förorsakar illamående, huvudvärk och andnöd. I allvarligare fall kan det uppstå lunginflammation. Det finns även risk för astma. De långsiktiga verkningarna av att andas in lägre halter av ammoniak är dåligt undersökta. Utsläpp av ammoniak till den yttre miljön bidrar till såväl övergödning som försurning.
Kalciumhydroxid (släckt kalk, Ca(OH)2) bildas då vatten tillsätts kalciumoxid (CaO). Kalciumhydroxid verkar irriterande på andningsvägar, ögon och hud, men i betydligt lägre grad än kalciumoxid.
Kaliumhydroxid (KOH) är ett starkt frätande ämne som förekommer antingen i fast form (pulver, flingor, stänger, kristallina massor) eller i vattenlösning. Kaliumhydroxid är mera frätande än de flesta syror i motsvarande koncentrationer. Nedsväljning kan redan i små mängder ge allvarliga skador på matstrupen. Koncentrerad kaliumhydroxid kan ke svårläkta frätskador på huden. Även utspädda lösningar kan vid längre tids kontakt ge upphov till frätskador, t ex om kaliumhydroxid kommer in i skyddshandskarna. Utspädda lösningar kan också vid upprepad hudkontakt ge upphov till hudirritation och icke allergiskt kontakteksem. Stänk av kaliumhydroxid i ögonen kan förorsaka allvarliga ögonskador med risk för synförlust. Vid inannding av damm och dimma som innehåller kaliumhydroxid irriteras och skadas andningsvägarna. Höga halter kan ge upphov till livshotande lungskador (lungödem). Kaliumhydroxid löser sig i vatten under kraftig värmeutveckling. Kaliumhydroxid angriper metaller som aluminium, tenn, bly och zink under utveckling av vätgas. Vätgas kan ge explosiva blandningar med luft.
Lut är en blandning av natriumhydroxid (NaOH) och kaliumhydroxid (KOH) i vattenlösning och är starkt frätande. Utspilld lut gör golvet mycket halt och kan ge upphov till halkolyckor. Lut är mera frätande än de flesta syror i motsvarande koncentrationer. Nedsväljning kan redan i små mängder ge allvarliga skador på matstrupen. Koncentrerad lut kan ge svårläkta frätskador på huden. Även utspädda lösningar kan vid längre tids kontakt ge upphov till frätskador, t ex om lut kommer in i skyddshandskarna. Utspädda lösningar kan också vid upprepad hudkontakt ge upphov till hudirritation och icke allergiskt kontakteksem. Stänk av lut i ögonen kan förorsaka allvarliga ögonskador med risk för synförlust. Vid inannding av damm och dimma som innehåller lut irriteras och skadas andningsvägarna. Höga halter kan ge upphov till livshotande lungskador (lungödem). Lut löser sig i vatten under kraftig värmeutveckling. Lut angriper metaller som aluminium, tenn, bly och zink under utveckling av vätgas. Vätgas kan ge explosiva blandningar med luft.
Natriumhydroxid (kaustiksoda, natronlut NaOH) är ett starkt frätande ämne som förekommer antingen i fast form (pulver, flingor, stänger, kristallina massor) eller i vattenlösning. Natriumhydroxid är mera frätande än de flesta syror i motsvarande koncentrationer. Nedsväljning kan redan i små mängder ge allvarliga skador på matstrupen. Koncentrerad natriumhydroxid kan ke svårläkta frätskador på huden. Även utspädda lösningar kan vid längre tids kontakt ge upphov till frätskador, t ex om natriumhydroxid kommer in i skyddshandskarna. Utspädda lösningar kan också vid upprepad hudkontakt ge upphov till hudirritation och icke allergiskt kontakteksem. Stänk av natriumhydroxid i ögonen kan förorsaka allvarliga ögonskador med risk för bestående synskada. Vid inannding av damm och dimma som innehåller natriumhydroxid irriteras och skadas andningsvägarna. Höga halter kan ge upphov till livshotande lungskador (lungödem). Natriumhydroxid löser sig i vatten under kraftig värmeutveckling. Natriumhydroxid angriper metaller som aluminium, tenn, bly och zink under utveckling av vätgas. Vätgas kan ge explosiva blandningar med luft. Referens = Litteratur om kemiska hälsorisker [chemfile(), file(), referens i dokument]
Råbensen är en flyktig organisk vätska extraherad från gasen som utvecklas vid torrdestillation av kol. Består främst av bensen (>70%), toluen (10-15%) och xylen (2-5%), kan innehålla andra kolväten i låga halter. Bensen kan ge cancer (leukemi) och finns tillsammans med 95 andra ämnen i den högsta cancerriskklassen. Klassningen är gjord av International Agency for Research on Cancer (IARC). Bensen tas lätt upp i kroppen, både vid inandning av gas och ångor samt vid hudkontakt med lösning, och förs sedan snabbt vidare till alla kroppens vävnader framförallt till fettvävnaden. Vid exponering för ämnet i höga doser påverkar bensen det centrala nervsystemet. Vid långvarig och upprepad inandning av bensen finns risk för anemi 1) och ökad infektionskänslighet. 1)
Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
SSAB I koksverket vid SSAB i Luleå finns en gasbehandlingsanläggning med en serie olika processer där rågasen från torrdestillationen av kol till koks renas i flera steg och där utvinns Stenkolstjära Stenkolstjära från rågasen separeas i förlaget genom att kyla gasen, i kylaren med ammoniakvatten och resten i elektrofilter. Från kylaren leds kondensatvatten till kondensatbehandlingen där tjära och beck separeras 1). Stenkolstjära och beck är hälsofarliga och de är även starkt hud- och ögonirriterande. Hudkontakt i kombination med solexponering kan ge svårartade eksem. 1)
Tjära / beck Tjära är en trögflytande vätska som erhålls som kondensat vid pyrolys (torrdestillation) av organiska material som kol och petroleum, tjära som bildas från kol kallas för Det finns risk för hudcancer och överkänslighet för solljus (fototoxiskt eksem) efter långvarig direktkontakt med tjära/beck. Eksem av typ fototoxiskt uppstår då huden utsätts för solljus. Polyaromatiska kolväten, polycykliska aromatiska kolväten eller polyaromater, ofta förkortat PAH av engelska Polycyclic Aromatic Hydrocarbons, är en grupp ämnen som finns i stenkol och petroleum (råolja). Det mest kända av dessa ämnen är benso(a)pyren. Flera av PAH-ämnena är cancerframkallande, t ex benso(a)pyren. Dessa ämnen har dessutom obehaglig lukt redan vid låga koncentrationer. PAH-ämnen är inte flyktiga men de sprids över stora områden med partiklar. Tjära och beck innehåller polyaromatiska kolväten (PAH). Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument] Referens = SSAB Luleå [chemfile(), file(), referens i dokument] Råbensen I naftalentvätten absorberas naftalen, bensen, toluen och xylen från gasen i processolja. I bensentvätten absorberas bensen, xylen och toluen från gasen i processolja. Processoljan leds till bensenanläggningen för utvinning av råbensen (bensen, xylen, toluen). Referens = SSAB Luleå [chemfile(), file(), referens i dokument] [chemfile(), nC=0 nr=452-b, f1=/produkt/info/html/452-b.htm] Rågas, koksgas Vid koksningen, som är en torrdestillation utan lufttillförsel, avdrivs flyktiga ämnen i kolet som gas, sk Rågasen renas i flera steg. Den renade rågasen ( Koksningsprocessen Vid koksningsprocessen avger kolet sina flyktiga beståndsdelar i form av rågas, med följer även vattenångan från fukten i kolet. Den största delen av rågasen består av vätgas och metangas, men den innehåller även ämnen som bensen, svavel, tjära samt en mängd olika kolväteföreningar t ex cyanider. Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
Svavel Svavel är ett grundämne som vid rumstemperatur är ett gult fast ämne. Vid antändning av svavel bildas giftig gas (svaveldioxid). Blandningar mellan luft och svaveldamm är explosiva. Inandning av svaveldamm ger upphov till inflammation i näshålan och till lungskador (emfysem 1)) med försämrad lunfunktion som följd. Hudkontakt med svavel kan orsaka irritation och svaveldamm kan ge upphov till ögonskador. 1)
Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), chemdata.dat, referens i dokument] Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), chemdata.dat, referens i dokument] Produktion svavel Svavel erhålls som en biprodukt från koksgas i koksverk vid tillverkning av koks från kol. Referens = SSAB Luleå [chemfile(), chemdata.dat, referens i dokument]
Genom de egenskaperna kan bekämpningsmedel också orsaka skada på hälsan och miljön. Därför är det viktigt att de är godkända av Kemikalieinspektionen och att de används på rätt sätt. För att få sälja eller använda ett bekämpningsmedel i Sverige krävs att det är granskat och godkänt av Kemikalieinspektionen. Godkända bekämpningsmedel får en behörighetsklass som visar vem som får använda det och som ställer olika kunskapskrav på användaren. I bekämpningsmedelsregistret finns de produkter registrerade som har godkänts av Kemikalieinspektionen. De handlar bl a om vilka verksamma ämnen produkterna innehåller, på vilket sätt de får användas, om produktens godkännande gäller eller om det har upphört. Referens = kemikalieinspektionen [chemfile(), file(), referens i dokument] Beroende på användningsområde kan ett bekämpningsmedel vara antingen ett växtskyddsmedel eller en biocidprodukt. Växtskyddsmedel används för att skydda växter inom jordbruk, skogsbruk och trädgårdsbruk. Biocidprodukter är exempelvis impregneringsmedel, båtbottenfärger och slembekämpningsmedel. Växtskyddsmedlen kan i sin tur indelas efter användningsområde - herbicider mot ogräs - fungicider mot svampar - insekticider mot insekter Referens = Sveriges Lantbruksuniversitet [chemfile(), file(), referens i dokument]
Ett växtskyddsmedel kan vara ett kemiskt eller ett biologiskt bekämpningsmedel. Ett kemiskt växtskyddsmedel är en blandning som består av ett verksamt ämne eller flera verksamma ämnen. Till det verksamma ämnet eller ämnena tillsätts olika typer av medel som underlättar användning och spridning. Det kan exempelvis vara lösningsmedel, eller emulgeringsmedel. Det är de verksamma ämnena som ger skyddseffekten. I ett biologiskt bekämpningsmedel är det en bioteknisk organism, dvs en levande organism som är verksam för att uppnå den skyddande effekten av medlet. Referens = Kemikalieinspektionen [chemfile(), file(), referens i dokument]
Exempel på biocidprodukter är - desinfektionsmedel - träskyddsmedel - myggmedel - båtbottenfärger. En biocidprodukt är en produkt avsedd att förstöra, oskadliggöra, hindra, förhindra verkningarna av eller på annat sätt kontrollera skadliga organismer på annat sätt än genom enbart fysisk eller mekanisk inverkan. Biocider är ämnen som används mot levande organismer. Biocider betecknas ofta med ett prefix som anger typen av organism som medlet används mot, t ex - Fungicid (svampar) - Algicid (alger) - Insekticid (insekter) - Baktericid (antibakteriellt medel) Referens = Kemikalieinspektionen [chemfile(), file(), referens i dokument]
Ett biologiskt bekämpningsmedel är en typ av bioteknisk organism som kan vara antingen en biocidprodukt eller ett växtskyddsmedel. Vid biologisk bekämpning används ofta naturliga fiender till de skadeorganismer som ska bekämpas. Sådana fiender kan vara mikroorganismer såsom bakterier, virus och svampar eller makroorganismer såsom nematoder (rundmaskar), insekter eller spindeldjur. Biotekniska organismer är produkter som består av eller innehåller levande organismer och som har framställts i bekämpningssyfte eller annat tekniskt syfte. Biologiska bekämpningsmedel som består av mikroorganismer ska, precis som kemiska bekämpningsmedel, vara godkända av Kemikalieinspektionen för att få säljas eller användas. Ett medel godkänns bara om det är godtagbart ur hälso- och miljösynpunkt. Växtskyddsmedel som innehåller mikroorganismer omfattas av EU:s växtskyddsmedelsförordning. Biocidprodukter som innehåller mikroorganismer omfattas av EU:s biocidförordning eller den svenska bekämpningsmedelsförordningen. Referens = Kemikalieinspektionen [chemfile(), file(), referens i dokument]
Referens = Kemikalieinspektionen [chemfile(), file(), referens i dokument]
Tjära / beck Tjära är en trögflytande vätska som erhålls som kondensat vid pyrolys (torrdestillation) av organiska material som kol och petroleum, tjära som bildas från kol kallas för Det finns risk för hudcancer och överkänslighet för solljus (fototoxiskt eksem) efter långvarig direktkontakt med tjära/beck. Eksem av typ fototoxiskt uppstår då huden utsätts för solljus. Polyaromatiska kolväten, polycykliska aromatiska kolväten eller polyaromater, ofta förkortat PAH av engelska Polycyclic Aromatic Hydrocarbons, är en grupp ämnen som finns i stenkol och petroleum (råolja). Det mest kända av dessa ämnen är benso(a)pyren. Flera av PAH-ämnena är cancerframkallande, t ex benso(a)pyren. Dessa ämnen har dessutom obehaglig lukt redan vid låga koncentrationer. PAH-ämnen är inte flyktiga men de sprids över stora områden med partiklar. Tjära och beck innehåller polyaromatiska kolväten (PAH). Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument] Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
Genom de egenskaperna kan bekämpningsmedel också orsaka skada på hälsan och miljön. Därför är det viktigt att de är godkända av Kemikalieinspektionen och att de används på rätt sätt. För att få sälja eller använda ett bekämpningsmedel i Sverige krävs att det är granskat och godkänt av Kemikalieinspektionen. Godkända bekämpningsmedel får en behörighetsklass som visar vem som får använda det och som ställer olika kunskapskrav på användaren. I bekämpningsmedelsregistret finns de produkter registrerade som har godkänts av Kemikalieinspektionen. De handlar bl a om vilka verksamma ämnen produkterna innehåller, på vilket sätt de får användas, om produktens godkännande gäller eller om det har upphört. Referens = kemikalieinspektionen [chemfile(), file(), referens i dokument] Beroende på användningsområde kan ett bekämpningsmedel vara antingen ett växtskyddsmedel eller en biocidprodukt. Växtskyddsmedel används för att skydda växter inom jordbruk, skogsbruk och trädgårdsbruk. Biocidprodukter är exempelvis impregneringsmedel, båtbottenfärger och slembekämpningsmedel. Växtskyddsmedlen kan i sin tur indelas efter användningsområde - herbicider mot ogräs - fungicider mot svampar - insekticider mot insekter Referens = Sveriges Lantbruksuniversitet [chemfile(), file(), referens i dokument]
Ett växtskyddsmedel kan vara ett kemiskt eller ett biologiskt bekämpningsmedel. Ett kemiskt växtskyddsmedel är en blandning som består av ett verksamt ämne eller flera verksamma ämnen. Till det verksamma ämnet eller ämnena tillsätts olika typer av medel som underlättar användning och spridning. Det kan exempelvis vara lösningsmedel, eller emulgeringsmedel. Det är de verksamma ämnena som ger skyddseffekten. I ett biologiskt bekämpningsmedel är det en bioteknisk organism, dvs en levande organism som är verksam för att uppnå den skyddande effekten av medlet. Referens = Kemikalieinspektionen [chemfile(), file(), referens i dokument]
Exempel på biocidprodukter är - desinfektionsmedel - träskyddsmedel - myggmedel - båtbottenfärger. En biocidprodukt är en produkt avsedd att förstöra, oskadliggöra, hindra, förhindra verkningarna av eller på annat sätt kontrollera skadliga organismer på annat sätt än genom enbart fysisk eller mekanisk inverkan. Biocider är ämnen som används mot levande organismer. Biocider betecknas ofta med ett prefix som anger typen av organism som medlet används mot, t ex - Fungicid (svampar) - Algicid (alger) - Insekticid (insekter) - Baktericid (antibakteriellt medel) Referens = Kemikalieinspektionen [chemfile(), file(), referens i dokument]
Ett biologiskt bekämpningsmedel är en typ av bioteknisk organism som kan vara antingen en biocidprodukt eller ett växtskyddsmedel. Vid biologisk bekämpning används ofta naturliga fiender till de skadeorganismer som ska bekämpas. Sådana fiender kan vara mikroorganismer såsom bakterier, virus och svampar eller makroorganismer såsom nematoder (rundmaskar), insekter eller spindeldjur. Biotekniska organismer är produkter som består av eller innehåller levande organismer och som har framställts i bekämpningssyfte eller annat tekniskt syfte. Biologiska bekämpningsmedel som består av mikroorganismer ska, precis som kemiska bekämpningsmedel, vara godkända av Kemikalieinspektionen för att få säljas eller användas. Ett medel godkänns bara om det är godtagbart ur hälso- och miljösynpunkt. Växtskyddsmedel som innehåller mikroorganismer omfattas av EU:s växtskyddsmedelsförordning. Biocidprodukter som innehåller mikroorganismer omfattas av EU:s biocidförordning eller den svenska bekämpningsmedelsförordningen. Referens = Kemikalieinspektionen [chemfile(), file(), referens i dokument]
Referens = Kemikalieinspektionen [chemfile(), file(), referens i dokument]
Bensen är giftigt vid inandning, förtäring och långvarig hudkontakt. Ämnet kan lätt tas upp i kroppen vid inandning av ångor och genom hudkontakt med lösning. Stänk i Bensen kan ge ärftliga genetiska skador och leukemi (cancer) vid långvarig och upprepad exponering. Bensen är 1) Ångor av bensen är irriterande på andningsvägar och ögon. Vid långvarig och upprepad inandning av bensen finns risk för 1)
Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument]
Polyaromatiska kolväten (PAH) är en grupp av kemiska ämnen som i allmänhet förekommer i blandning med varandra. Det mest kända av de här ämnena är benso(a)pyren. Vid tillverkning av koks från kol i ett koksbatteri bildas koksgas och den orenade processgasen innehåller hög halt PAH. Polyaromatiska kolväten finns i stenkolstjära, som är en biprodukt vid tillverkning av koks från kol i ett koksverk. Höga halter kan uppstå på arbetsplatser där uppvärmd stenkolstjära hanteras. Hudkontakt med PAH, t ex i stenkolstjära, kan ge hudcancer. Inandning av PAH, både i gasform och PAH som har fastnat på partiklar kan ge lungcancer. Referens = Litteratur om kemiska hälsorisker [chemfile() chemdata.dat (efter *)]
[cfile() nchem=2 f1=/produkt/info/html/cyanid-a.htm ] Cyanider Cyanider och cyanföreningar är kemiska föreningar i vilka ingår en cyangrupp (kväve bundet till kol, CN). Cyanider är mycket giftiga vid såväl inandning som hudkontakt och kan orsaka huvudvärk, yrsel, öronsusningar, andnöd, illamående, kräkningar. Höga halter orsakar snabbt oregelbunden puls, andningsstillestånd, kramper och medvetslöshet. Cyanider kan vid uppvärmning bilda den mycket giftiga gasen Risk för att vätecyanid bildas vid exponering för cyanider Vätecyanid kan bildas genom hydrolys av cyanid, t ex då ångor av cyanider inandas och cyaniderna hydrolyseras till vätecyanid t ex i kontakt med slem. Hydrolys är en kemisk process där en molekyl klyvs i kontakt med vatten, t ex vid hydrolys av cyanider då frigörs den farliga cyanidjonen (CN) och då finns risk att vätecyanid bildas. Vid nedsväljning av cyanider i vätska, ångor eller partiklar som är kontaminerade med cyanider kan cyanider reagerar med magens saltsyra till Förgiftning Vätecyanid inaktiverar cellandningen genom att binda till järnet i ett protein i cellen som kallas för cytokrom C. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [cfile()] Cyanider råjärn [cfile() nchem=2 f1=/produkt/info/html/CN056.htm] I masugnen kan cyanid bildas vid extremt höga temperaturer på gasen i masugnens topp. Oftast försvinner den av sig själv på vägen genom masugnen men i speciella fall kan den stanna kvar Den varma gasen från masugnen renas i en torr och en våt behandling i cyklon respektive skrubber. Den våta gasreningen sker med hjälp av vatten. Om det finns cyanider i gasen kan de hamna i vattnet som används vid den våta gasreningen och som recirkuleras i en slambassäng. Det kan även ske cyanidutsläpp till slambassängen vid ojämn drift i masugnen, t ex vid ett bandgångshaveri till matningen av masugnstoppen. Referens = SSAB Luleå [cfile()] [cfile() nchem=2 f1=/produkt/info/html/CN056-r.htm] Vid råjärnstillverkning kan cyanider förekomma i vattnet i slambassängen för recirkulering av vatten som används vid våtgasrening av masugnsgas. Referens = SSAB Luleå [cfile()] Risker Hudkontakt med vattnet i bassängen eller inandning av ångor från bassängen kan medföra att cyanider tas upp i kroppen och då finns det risk att den starkt giftiga gasen Referens = SSAB Luleå [cfile()] Koksgaskondensat [cfile() nchem=2 f1=/produkt/info/html/CN452.htm] Vid torrdestillation av stenkol tilll koks omvandlas 25% av kolet till rågas som innehåller flyktiga ämnen från kolet, bl a cyanider. På koksbatteriet finns risk för exponering för cyanider, eftersom det uppstår rök och stoft då luckor öppnas vid påfyllning av stenkol till batteriet och stoftpartiklarna kan vara kontaminerade med cyanider. Inandning av partiklar kontaminerade med cyanid medför risk för exponering för cyanider. Vid nedsväljning kan cyanider från partiklar lösas i slem och komma i kontakt med magens saltsyra och då finns risk att den starkt giftiga gasen vätecyanid bildas. Rågasen renas i flera steg i gasreninigsanläggningen. Den renade rågasen kallas för koksgas och innehåller metan, koloxid, vätgas, kvävgas, vätesulfid och även spårmängder av fenoler och cyanider. Koksgas tranporteras till användare i rörledningar och det bildas kondensat som samlas upp i vattenlås. På rörens insida och i vattenlåsen kan det därför bildas beläggningar av kondensat som kan innehålla fenoler och cyanider.. Referens = SSAB Luleå [cfile()] [cfile() nchem=2 f1=/produkt/info/html/CN452-r.htm] Cyanider, koksgaskondensat Cyanider kan finnas i koksgaskondensat och avlagringar av koksgaskondensat i ledningssystem och vattenlås för koksgas Referens = SSAB Luleå [cfile()] Risker Cyanider kan vid uppvärmning bilda vätecyanid. Vid arbeten som medför att koksgaskondensat, t ex i koksgasledningar, utsättes för höga temperaturer kan den starkt giftiga gasen Inandning av Referens = Litteratur om kemiska hälsorisker [cfile()]
Dioxiner Av de totalt 210 kongenerna bedöms 17 kongener, varav 7 PCDD och 10 PCDF, vara både mycket toxiska (giftiga) och persistenta (svårnedbrytbara i miljön). Vanligtvis är det de här 17 olika toxiska PCDD- och PCDF-kongenerna som brukar analyseras. Den mest giftiga kongenen, och den mest studerade, är PCB PCB är en förkortning för polyklorerade bifenyler. Dessa utgör en serie av 209 enskilda kongener (varianter) som skiljer sig genom antalet kloratomer och deras plats i molekylen. PCB är en industrikemikalie som har haft många olika användningsområden pga dess värmetålighet och isolerande förmåga. PCB har t ex använts i kondensatorer, transformatorer, värmeväxlare, fogmassor i hus och i färger. Sedan 1970-talet har användning av PCB varit förbjuden i Sverige. Referens = Livsmedelsverket [chemfile(), file(), referens i dokument] Dioxiner i stålindustrin Dioxiner kan bildas vid skrotsmältning i stålverk och en mindre del bildas vid torrdetillation av stenkol till koks i koksverk. De dioxiner som bildas binds i hög grad till stoft och mängden från stålverk påverkas bl a av hur processerna styrs. Dioxiner som bildas vid skrotsmältning beror på att skrotet kan innehålla klorhaltigt plast, t ex PVC (polyvinylklorid) eller annat material som innehåller klor eller PCB. Referens = SSAB Luleå [chemfile(), file(), referens i dokument] Hälsorisker med dioxin och dioxinlika PCB I olika typer av studier av djur och människa misstänks dioxiner och PCB kunna påverka reproduktionen (fortplantningen), immunförsvarets funktion, utvecklingen av centrala nervsystemet (hjärnan), samt orsaka cancer. Stabila och fettlösliga Dioxiner och PCB är stabila och fettlösliga föreningar som är svåra att bryta ner. De finns därför kvar i miljön och i kroppen under lång tid. Egenskaperna gör också att dessa ämnen anrikas i näringskedjorna, vilket innebär att de högsta halterna återfinns i bl a rovfiskar från förorenade områden. Fettlösligheten gör att dioxiner och PCB ansamlas i fettvävnaden hos djur och människor. Referens = Livsmedelsverket [chemfile(), file(), referens i dokument] [chemfile(), nC=0 nr=dioxin2, f1=/produkt/info/html/dioxin2.htm] Dioxinekvivalenter (TEQ) För att kunna bedöma den totalt effekten av alla dioxinlika ämnen används ofta ett ekvivaleringsverktyg där den samlade halten av dioxiner och dioxinlika PCB uttrycks i TCDD-ekvivalenter (TEQ). Det är de 17 särskilt toxiska (giftiga) dioxinerna som brukar räknas samman som ett viktat medelvärde, till mängd toxiska ekvivalenter (TEQ). Detta innebär att giftigheten hos de olika dioxin- och PCB-kongenerna sätts i relation till TCDDs giftighet. Om en kongen är hälften så giftig som TCDD, får den toxicitetsekvivalentfaktorn (TEF) 0,5. Genom att multiplicera koncentrationen för varje enskild kongen med dess TEF och därefter summera erhålls den totala halten av TCDD-ekvivaler (TEQ). Utgångspunkten för TEQ-systemet är att samtliga dioxiner och dioxinlika PCB verkar via samma mekanism, via den sk dioxin- eller Ah-receptorn, i kroppen och ger upphov till samma effekter. Effekterna anses vara additiva, dvs kan slås ihop. Den senaste översynen av TEF gjordes under 2006 i WHO:s regi (van den Berg et al 2006). Världshälsoorganisationen (WHO) är ett specialiserat organ inom Förenta nationerna (FN) som handlar om internationell folkhälsa. Dioxiner och PCB i maten Människor får i sig mest dioxiner och PCB via maten. Ämnena är fettlösliga och finns främst i feta animaliska livsmedel som fisk, kött och mejeriprodukter. Särskilt höga halter finns i fet fisk som strömming och vildfångad lax från förorenade områden, t ex Östersjön, Bottniska viken, Vänern och Vättern. Referens = Livsmedelsverket [chemfile(), file(), referens i dokument]
Fenoler Inandning av ångor eller hudkontakt med fast fenolmassa kan ge upphov till huvudvärk, yrsel, illamående, förvrängning av syn- och hörselintryck, muskelsvaghet, kramper, andningssvårigheter samt i allvarligare fall medvetslöshet. Långvarig och upprepad exponering för fenol kan ge upphov till illamående och magbesvär. Det kan också förekomma huvudvärk och sömnbesvär samt skador på inre organ. Tegel Om bindemedel i tegel är fenol och/eller fenolharts finns ofta små mängder av ämnet som inte har reagerat till en kemisk förening och då kan fenol avges vid torkning av murade skänkar i torkstation. Även andra fenolderivater kan bildas då fenol/fenolharts utsätts för höga temperaturer. Fenolämnen är irriterande på ögon, luftvägar och slemhinnor. Dessa ämnen har dessutom obehaglig lukt redan vid låga koncentrationer. Inom kemin är derivat ett ämne som bildas ur ett annat ämne genom mindre förändringar i den kemiska strukturen. Expositiionsnivåer för skadeverkningar för dessa fenoler är mycket varierande och många av ämnena är dåligt utredda med avseende på hälsorisker. Referens = Litteratur om kemiska hälsorisker [chemfile() chemdata.dat (efter *)]
Fosforsyra är färglös och förekommer vanligen som vattenlösning. Koncentrerad fosforsyra (över 85%) är vid rumstemperatur ett fast ämne. Dimma av fosforsyra verkar frätande på andningsvägar, ögon, hud och tänder. Stänk på huden och ögon kan förorsaka svårläkta sår, och måste omedelbart spolas bort med vatten. Inandning av lägre halter under lång tid kan ge frätskador på tänderna. Vid upphetning av fosforsyra bildas fosforoxider. Vid kontakt med metaller bildas den giftiga gasen fosforväte (fosfin) och vätgas. Vätgas bildar med luft blandingar som vid antändning kan explodera. Referens = Litteratur om kemiska hälsorisker [chemfile(), file(), referens i dokument]
Gasol är en gasblandning som huvudsakligen består av propan och butan. Även propylen och butylen kan ingå. Gasol är brandfarligt och bildar explosiva blandningar med luft. Eftersom gasol är dubbelt så tung som luft har den en benägenhet att ansamlas i lågt belägna utrymmen. Inandning av höga halter gasol kan förorsaka yrsel, illamående och huvudvärk, vid högre halter förlamning och medvetslöshaet. Mycket höga halter kan undantränga luftens syre och därigenom förorsaka kvävning. Gasol förvaras flytande under tryck. Utströmmande gasol i flytandee form kan ge kylskador.
Inandning av respirabla partiklar av järn och järnoxid i rök- och damm under lång tid kan ge upphov till en form av dammlunga, som kallas järnlunga eller sideros. Referens = Litteratur om kemiska hälsorisker [chemfile() chemdata.dat (efter *)]
Kalciumhydroxid (släckt kalk, Ca(OH)2) bildas då vatten tillsätts kalciumoxid (CaO). Kalciumhydroxid verkar irriterande på andningsvägar, ögon och hud, men i betydligt lägre grad än kalciumoxid.
Kalciumkarbid är ett fast ämne. Damm av kalciumkarbid verkar irriterande och frätande på andningsvägar, ögon och hud. Då kalciumkarbid kommer i kontakt med vatten eller fuktig luft bildas kalciumhydroxid och acetylen. Kalciumhydroxid verkar irriterande på andningsvägar, ögon och hud. I ögonen kan det åstadkomma allvarliga frätskador. Acetylen är en brandfarlig gas. I trånga utrymmen kan acetylen tränga undan luftens syre och därigenom förorsaka kvävning. Kalciumkarbid är ofta förorenad med kalciumfosfat och kalciumarsenat. Då kalciumkarbid kommer i kontakt med vatten finns därför risk för bildning av de giftiga ämnena fosforväte och arsenikväte. Referens = Litteratur om kemiska hälsorisker [chemfile(), chemdata.dat, referens i dokument]
Kalciumoxid (CaO) är ett vitt fast ämne som ofta förekommer i pulverform. Vid kontakt med vatten sker en reaktion med stark värmeutveckling, varvid kalciumhydroxid (släckt kalk, Ca(OH)2) bildas. Kalciumoxid verkar starkt irriterande och frätande på andningsvägar, ögon och hud. Inanding av damm kan bl a leda till sår på nässkiljeväggen och inflammationer i andningsvägarna, i svåra fall lunginflammation. Hudkontakt kan ge upphov till irritation och sår på huden. Damm av kalciumoxid som kommer in i ögonen kan förorsaka bestående ögonskador. Särskilt gäller detta om ögonen upprepade gånger utsätts för ämnet. Referens = Litteratur om kemiska hälsorisker [chemfile() chemdata.dat (efter *)]
Kiseldioxid, SiO2 Kiseldioxid (SiO2) är en kemisk förening av kisel och syre och förekommer i naturen i flera olika former. De kan indelas i två typer, Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), chemdata.dat, referens i dokument] I naturen förekommer kiseldioxid bland annat i form av kvarts (lågkvarts), mineral med sammansättningen SiO2. Det förekommer i två modifikationer, alfa-kvarts (lågkvarts) och beta-kvarts (högkvarts). Lågkvarts är stabil vid temperaturer under 573 °C. Stabilitetsområdet för högkvarts är mellan 573 och 867 °C, varför detta mineral normalt inte förekommer inom den övre jordskorpan. Tridymit och kristobalit är högtemperatur polymorfer av kiseldioxid , vilket innebär att de har samma kemiska formel, SiO2, men med olika kristallstrukturer. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), chemdata.dat, referens i dokument]
Referens = Litteratur om kemiska hälsorisker [chemfile() chemdata.dat (efter *)]
Krom i keramiska produkter föreligger nästan alltid i form av 3-värt krom bunden som kromit, 6-värt krom (kromater) kan förekomma som förorening. Kromit (Fe2CrO4) är ett mineral som innehåller järn och 3-värt krom. Kromater är 6-värda kromföreningar och de är allergiframkallande. Det är 6-värda kromföreningar i keramiska produkter som leder till uppkomst av allergiskt kontakteksem. Mekanisk bearbetning av tegel som innehåller krom kan medföra risk för exponering för allergiframkallande kromdamm. Referens = Järnbruksförbundets skyddsblad [chemfile(), file(), referens i dokument] Den som blivit allergisk kan vid kontakt med, mycket små mängder, såväl 6-värt som 3-värt krom utlösa den allergiska reaktionen. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellstenn [chemfile(), file(), referens i dokument]
Metan Inandning av höga halter kan orsaka huvudvärk, yrsel, andnöd samt vid mycket höga halter medvetslöshet och kvävning pga att gasen tränger undan syre - Extremt brandfarligt - Gasen kan redan vid temperaturer betydligt under rumstemperatur lätt bilda explosiv blandning med luft
Nickel är en silvervit metall. Den används i legeringar som rostfritt stål. Nickel används också som legering inom stålindustrin. Nickelmetall och nickelföreningar är allergiframkallande och en del former av nickel kan ge cancer. Kemiska produkters klassificering framgår i säkerhetsdatablad sektion 2 och sammansättning i sektion 3. Nickel kan ge upphov till allergiskt kontakteksem. Allergin kan uppkomma vid t ex kontakt med nickel i legeringar. I REACH-lagstiftningen är metalliskt nickel klassificerat som cancerogen kategori 3, kemiska ämnen som misstänks vara cancerogena. Inannding av damm som innehåller nickel kan ge upphov till bestående inflammationer i näsan och näsans bihålor. Luktsinnet kan skadas och det kan gå hål på nässkiljeväggen. Det kan också ge upphov till astma av typ allergisk alveolit (inflammationer i lungans finaste förgreningar, alveolerna).
Nitrösa gaser Nitrösa gaser, kväveoxider NOx, är en blandning av flera olika kemiska föreningar mellan kväve och syre. De viktigaste är kväveoxid och kvävedioxid. Vid mätning av nitrösa gaser brukar summahalten av kväveoxid och kvävedioxid bestämmas. Nitrösa gaser är ibland färglösa, ibland gulaktiga (kväveoxid är färglös, kvävedioxid är gulbrun. Nitrösa gaser bildas ur luftens kväve och syre vid all slags förbränning. De utgör en viktig beståndsdel i motoravgaser, främst dieselavgaser. Nitrösa gasr utgör också ett vanligt arbetsmiljöproblem vid svetsning, skärbränning. Nitrösa gaser (främst kvävedioxid) påverkar lungorna redan vid låga halter. Lungfunktionen försämras och motståndskraften mot infektioner i lungorna minskas. Astmatiker förefaller att vara särskilt känsliga för effekterna på lungorna av nitrösa gaser Höga halter ger upphov till livshotande lungödem. Nitrösa gaser (främst kväveoxid) försämrar hämoglobinernas syretransporteande förmåga genom bildning av methemoglobin. Cancerframkallande nitrosaminer kan bildas genom en kemisk reaktion mellan nitrösa gaser och aminer. Aminer är en grupp ämnen som bl a bildas genom nedbrytning av kroppens proteiner. Utsläpp av nitrösa gaser till den yttre miljön bidrar till såväl försurning som övergödning. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument]
Polyaromatiska kolväten Polycykliska aromatiska kolväten, även polyaromatiska kolväten eller polyaromater, ofta förkortat PAH av engelska Polycyclic Aromatic Hydrocarbons, är en grupp ämnen som finns i stenkol och petroleum (råolja) samt bildas vid förbränning av organiskt material. Det mest kända av dessa ämnen är benso(a)pyren. Flera av PAH-ämnena är cancerframkallande, t ex benso(a)pyren. PAH-ämnen är inte flyktiga men de sprids över stora områden med partiklar. Exponering för PAH-ämnen kan medföra en ökad risk för cancer. Olika råoljeraffineringsprocesser bidrar till att koncentrationen PAH ökar i vissa slutprodukter. Det är således mycket PAH i bl a tung eldningsolja. Polyaromater förekommer också i sot, beck, asfalt, kreosot och mineraloljor. Nya oljor som är raffinerade innehåller jämförelsevis låga halter, men efter en tids användning kan halten öka drastiskt, t ex i motoroljor och hydrauloljor som varit utsatta för höga temperaturer. Mätning Enligt Arbetsmiljöverkets föreskrifter om hygieniska gränsvärden, bedöms halten polyaromater i luft utifrån mätning av halten benso(a)pyren. Det bör dock observera att benso(a)pyren bara svarar för en liten och varierande andel av den cancerframkallande effekten hos polyaromaterna. Hälsorisker Långvarig eller upprepad hudkontakt med polyaromater i t ex stenkolstjära eller använda oljor kan ge upphov till hudcancer. Inandning av polyaromater, i gasform eller de som har fastnat på partiklar, kan ge upphov till lungcancer. Yttre miljö Benso(a)pyren är bioackumulerande och svårnedbrytbart. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument] Koksverk, PAH-ämnen vid tillverkning av koks från kol Vid tillverkning av koks från kol i ett koksbatteri bildas koksgas och den orenade processgasen innehåller hög halt PAH. På koksbatteriet förekommer arbeten där luckor måste öppnas för att fylla på kol och det förekommer läckage av orenad processgas. Därför finns det risk för exponering för PAH i gasform men även för PAH som har fastnat på partiklar. PAH-ämnen har relativt låg flyktighet, vilket innebär att de inte håller sig luftburen särskilt länge utan fastnar på partiklar. Den största förekomsten av polyaromater finns i stenkolstjära, som är en biprodukt vid tillverkning av koks från kol. Risk för exponering för höga halter PAH finns på arbetsplatser där stenkolstjära tillverkas eller hanteras. PAH-ämnen i begagnade oljor och smörjfetter Begagnade oljor (t ex motoroljor, hydrauloljor) och smörjfetter som varit utsatta för höga temperaturer kan innehålla höga halter PAH som bildats vid användningen. Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
Råbensen är en flyktig organisk vätska extraherad från gasen som utvecklas vid torrdestillation av kol. Består främst av bensen (>70%), toluen (10-15%) och xylen (2-5%), kan innehålla andra kolväten i låga halter. Bensen kan ge cancer (leukemi) och finns tillsammans med 95 andra ämnen i den högsta cancerriskklassen. Klassningen är gjord av International Agency for Research on Cancer (IARC). Bensen tas lätt upp i kroppen, både vid inandning av gas och ångor samt vid hudkontakt med lösning, och förs sedan snabbt vidare till alla kroppens vävnader framförallt till fettvävnaden. Vid exponering för ämnet i höga doser påverkar bensen det centrala nervsystemet. Vid långvarig och upprepad inandning av bensen finns risk för anemi 1) och ökad infektionskänslighet. 1)
Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
Salpetersyra är en gulaktig, starkt frätande vätska med stickand lukt. Vid koncentrationer över 70% är den rödrykande, dvs avger gulbruna eller rödbruna ångor som består av nitrösa gaser (kväveföreningar). Även mer utspädd salpetersyra avger nitrösa gaser vid uppvärmning, i solljus, i fuktig luft eller vid kontakt med en del metaller. Vid hantering av salpetersyra kan det uppstå dels syra ånga, dels nitrösa gaser. Syraångorna verkar irriterande och frätande på andningsvägar, ögon, hud och tänder. Nitrösa gaser kan i höga koncentrationer ge upphov till livshotande lungskador (lungödem). Stänk i ögonen kan ge allvarliga ögonskador. Stänk av salpetersyra ger upphov till svårläkta frätsår samt till gulfärgningar av huden. Förtäring av redan små mängder kan ge inre frätskador. Salpetersyra är i sig själv inte brännbar. Däremot kan många organiska ämnen, som trä, papper och tyg samt många organiska lösningsmedel antändas vid kontakt med salpetersyra.
Saltsyra (klorvätesyra, HCl) är en färglös eller gulaktig, starkt frätande vätska. Koncentrerad syra är rykande och avger frätande ångor som består av klorväte (HCl). Vätskan och ångorna förorsakar kraftig rostangrepp på metaller. Stänk av saltsyra ger frätskador på ögon och hud. Hudskadorna yttrar sig som sveda, rodnad, blåsor och sår. Saltsyraångor verkar irriterande och frätande på andningsvägar, ögon och hud. Högre halter kan förorsaka livshotande lungödem. Inandning under längre tid kan ge frätskador på tänderna. Vid kontakt mellan saltsyra och de flesta metaller bildas vätgas, som ger exploiva blandningar med luft.
Svavel Svavel är ett grundämne som vid rumstemperatur är ett gult fast ämne. Vid antändning av svavel bildas giftig gas (svaveldioxid). Blandningar mellan luft och svaveldamm är explosiva. Inandning av svaveldamm ger upphov till inflammation i näshålan och till lungskador (emfysem 1)) med försämrad lunfunktion som följd. Hudkontakt med svavel kan orsaka irritation och svaveldamm kan ge upphov till ögonskador. 1)
Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), chemdata.dat, referens i dokument] Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), chemdata.dat, referens i dokument] Produktion svavel Svavel erhålls som en biprodukt från koksgas i koksverk vid tillverkning av koks från kol. Referens = SSAB Luleå [chemfile(), chemdata.dat, referens i dokument]
Svavelsyra (H2SO4) är en starkt frätande vätska. Ren syra är luktlös och färglös eller svagt gul. Förorenad syra kan vara brun. Svavelsyra angriper och förstör de flesta material. Vid kontakt med många kemiska ämnen bildas giftiga och brandfarliga ämnen. T ex varm koncentrerad syra är oxiderande och bildar svaveldioxid i kontakt med metaller. Dimma av svavelsyra verkar starkt irriterande och frätande på andningsvägar, ögon och hud. Mycket höga halter kan ge livshotande lungödem. Långvarig inandning av svavelsyradimma kan ge svåra frätskador på tänderna. Stänk på huden ger svårläkta frätsår. Stänk i ögonen kan ge svåra ögonskador med bestående synnedsättning, även risk för blindhet. Vid uppvärmning av svavelsyra avges syradimma och svaeltrioxid (frätande). Svavelsyra reagerar häftigt med vatten under stark värmeutveckling. Spädning måste ske genom att syran hälls i vatten, och inte tvärtom.
En syra definieras som ett ämne som kan avge protoner (eller vätejoner) (pH <7). Många ämnen har förmågan att kunna avge protoner, men i större eller mindre utsträckning. Syror delas därför in i olika grupper beroende på hur många protoner de kan avge i en lösning (oftast iakttaget i vattenlösning). Citronsyran har inte så stor benägenhet att avge protoner och kan därför ses som en svag syra, medan saltsyra avger alla sina protoner och ses då som en stark syra. Det finns även syror som kan betecknas som medelstarka syror, t ex fosforsyra. Syrors styrka anges av en syrakonstant, en form av jämviktskonstant. En syra kan tillsammans med en korresponderande bas bilda ett buffertsystem. Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), chemdata.dat, referens i dokument] [chemfile(), nC=0 nr=acid, f1=/produkt/info/html/acid.htm]
Syror är kemiska ämnen som innehåller väte och i deras vattenlösningar finns oxoniumjoner H3O+. När en syra reagerar med vatten övergår väte från syran i form av vätejoner (H+) till vattenmolekyler (H2O) och det bildas oxoniumjoner (H3O+). Det är oxoniumjonenerna som ger vattenlösningar av syror deras sura egenskaper och den sura lösningen kallas för Syror reagerar med många sk oädla metaller och det bildas Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), file(), referens i dokument] I reaktionen mellan väteklorid (HCl) och vatten lämnar protonen (vätejonen H+) HCl-molekylen och binds istället vid ett av de fria elektronparen i H2O-molekylen som blir en oxoniumjon (H3O+). Väteatomens elektron stannar kvar hos kloratomen som blir en kloridjon (Cl-). Oxoiumjoner (H3O+) och kloridjoner (Cl-) gör att lösningen kan leda elektrisk ström. Referens = Gymnasiekemi A, utgiven av Liber [chemfile(), file(), referens i dokument] 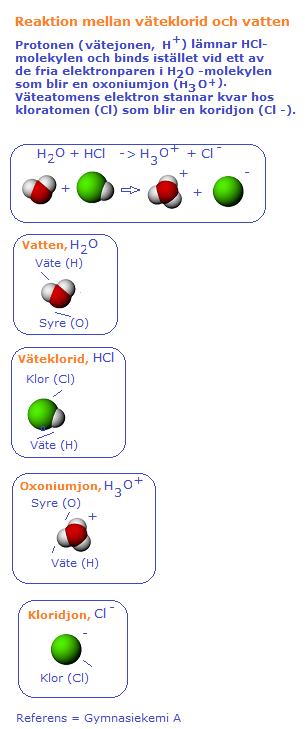
Ämne som består av molekyler eller joner som kan avge en proton (ev flera protoner) kallas Det bildas När väteklorid (HCl) löses i vatten avger praktiskt taget alla vätekloridmolekyler (HCl) sina protoner (vätejoner). Lösningen kallas Referens = Gymnasiekemi A, utgiven av Liber [chemfile(), file(), referens i dokument] Starka och svaga syror En syra är ett ämne som genom dissociation 1) kan avge protoner (vätejoner). En syra har pH-värde lägre än 7. Syror delas in i starka och svaga syror, beroende på i hur hög grad de dissocieras.
Den korresponderande basen till en syra är den bas som uppkommer när en syra protolyserats (avger en vätejon) och den korresponderande syran till en bas är den syra som uppkommer när en bas tar upp en vätejon. Syran är saltsyra (HCl), och när en vätejon lämnat molekylen kvarstår en kloridjon (Cl-), kloridjonen är den korresponderande basen till saltsyra. Ammoniak (NH3) är en bas och vill dra åt sig en vätejon, och när den gjort det har den bildat en ammoniumjon (NH4+), ammoniumjonen är den korresponderande syran till ammoniak. Om en syra är stark eller svag beror på hur många vätejoner som syran avger då den löses i vatten. I en stark syra frigör nästan alla syramolekyler vätejoner. I en svag syra frigör kanske bara 1/10 av syramolekylerna vätejoner. T ex citronsyra har inte så stor benägenhet att avge protoner (vätejoner) och betecknas därför som en svag syra, medan saltsyra avger alla sina protoner och betecknas därför som en stark syra. Koncentrerade och utspädda syror Koncentrationen av syra beror på hur mycket vatten den löses i. Om mycket syra löses i lite vatten, blir syran koncentrerad. Om lite syra löses i mycket vatten, blir syran utspädd. Både starka och svaga syror kan vara koncenterade eller utspädda. 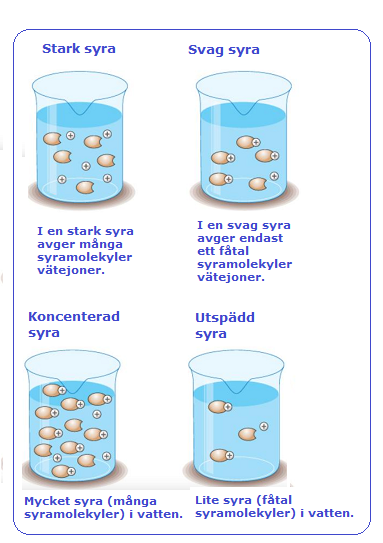
Referens = Kemi Direkt, Gidhagen, Åberg [chemfile(), file(), referens i dokument] Saltsyra, HCL (aq) Då väteklorid (HCl) löses i vatten, bildas saltsyra HCl (aq). Om så mycket väteklorid som möjligt löses i vatten, bildas koncentrerad saltsyra. Den innehåller ca 37% väteklorid (HCl). Salpetersyra, HNO3 Salpetersyra är en färglös frätande vätska, som protolyseras 1) fullständigt i vatten. 1) [chemfile(), nC=0 nr=fdiv, f1=/produkt/info/html/fdiv.htm]
Då mycket utspädd salpetersyra reagera med vatten bildas vätgas. Utspädd salpetersyra och koncentrerad salpetersyra reagerar med de flesta metaller, då bildas giftiga nitrösa gaser kväveoxid (NO) och rödbrun kvävedioxid (NO2). Koncentrerad salpetersyra bör förvaras i mörka glasflaskor. Syran sönderfaller under inverkan av ljus och det bildas kvävedioxid (NO) som färgar syran gul. Svavelsyra, H2SO4 Svavelsyra är en färg- och luktlös vätska, i koncentrerad form är den tung och tjockflytande. En svavelsyramolekyl kan avge två protoner, den är tvåprotonig. Vid reaktion med vatten sker protolysen med i två steg. I det första steget är protolysen fullständig medan i det andra steget endast en del av vätesulfatjonerna protolyseras.
svavelsyra + vatten -> oxoniumjon + vätesulfatjon H2SO4(l) + H2O -> H3O+(aq) + HSO4-(aq) Protolys 2 vätesulfatjon + vatten -> oxoniumjon + sulfatjon HSO4- + H2O -> H3O+(aq) + SO42-(aq) Då koncentrerad svavelsyra och vatten blandas utvecklas värme. Värmeutvecklingen kan bli så stor att kokpunkten för vatten överskrids. Därför måste försiktighet iaktagas vid utspädning av koncentrerad svaelsyra. Regeln är att syran ska hällas i vatten och inte tvärtom. Syran som har högre densitet än vatten sjunker då ner och blandas med vatten. Om vatten hälls i koncentrerad svavelsyra, är det risk att blandningen stänker. Kolsyra, H2CO3 När koldioxid (CO2) leds i vatten bildas en sur lösning som kallas kolsyra. Det är en tvåprotonig syra som protolyseras i två steg.
CO2(g) + H2O -> H2CO3(aq) Protolys 1 kolsyra + vatten -> oxoniumjon + vätekarbonatjon H2CO3(aq) + H2O -> H2O+(aq) + HCO3-(aq) Protolys 2 vätekarbonatjon + vatten -> oxoniumjon + karbonatjon HCO3-(aq)+ + H2O -> H3O+ + CO32-(aq) Starka och svaga syror Koncentrerade syror Skilj mellan begreppen stark och koncenrerad. Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), file(), referens i dokument]
Vätejoner är av grundläggande betydelse vid beskrivning av syror. En vätejon är en jon som består av en positivt eller negativt laddad väteatom. Väteatomen består av en proton och en elektron. En positiv vätejon (H+) är en väteatom där elektronen saknas och består endast av en proton. En negativ vätejon (H-) har två elektroner och kallas för hydridjon. I praktiken bildas vätejoner bl a vid upplösning av syror eller sura salter i protiska lösningsmedel (lösningsmedel som har väte som är bundet till kväve eller syre t ex vatten). Vätejoner kan dock ej existera någon längre tid i fritt tillstånd utan binds snabbt, solvatiseras, till lösningsmedlet, som då fungerar som en bas. I vatten bildas snabbt sk oxoniumjoner (H3O+). Koncentrationer av vätejoner i en lösning brukar användas som mått på dess aciditet eller surhetsgrad, ju högre koncentration desto surare lösning. Eftersom vätejoner inte i någon högre grad kan existera fria som sådana i lösning är den egentliga koncentrationen svår att bestämma. I stället mäts den sk Att vätejoner bara består av en proton gör dem väldigt reaktiva. Vätejoner bildas då det finns vissa ämnen (syror) som har förmågan att avge vätejoner, och om det samtidigt finns andra ämne (baser) som omedelbart kan ta upp den igen. Syror Defintionen av Det som händer när en vätejon avges, är att väteatomen lämnar molekylen utan att ta med sig sin elektron, vilket får vätet att bli en positivt laddad vätejon, medan kloret, som plötsligt har ett överskott på en elektron, blir en negativt laddad kloridjon. 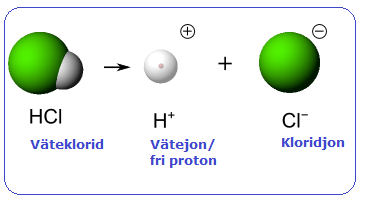
Vätejoner är reaktiva och existerar inte fritt någon längre stund. För att de inte ska hoppa tillbaka till kloridjonerna måste det finnas något annat ämne som kan ta upp dem i närheten. Ett typiskt sådant ämne är vatten. Om väteklorid löses i vatten sker en reaktion enligt den här modellen. 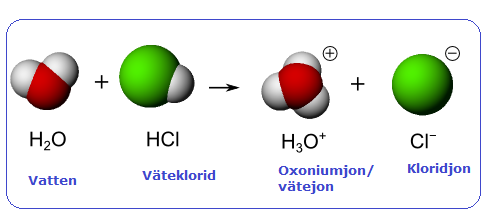
Vätejonen fäster på vattenmolekylen och bildar vad man kallar för en Principen är exakt den samma för syror som löses i vatten. De ger bort en vätejon till vattenmolekylerna, som blir till oxoniumjoner, och bildar själva en negativt laddad jon, en sk syrarest. Ett annat exempel på en syra är ättiksyra, som ger ättika dess sura smak. Det är en lite större molekyl än väteklorid, men principen är densamma. När det kommer vattenmolekyler i närheten av en ättiksyramolekyl kan en vätejon lossna från syramolekylen och i stället fästa på vattenmolekylen. Det bildas en positivt laddad oxoniumjon och en negativt laddad ättiksyrarest. 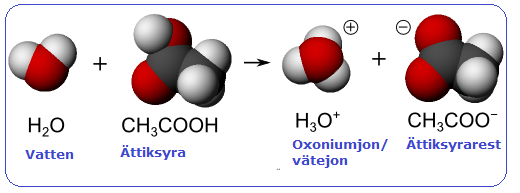
Oxoniumjonerna (H3O+) är mycket stabilare än helt fria vätejoner (H+), men är fortfarande väldigt reaktiva. Får de möjlighet att avge sina extra vätejoner till andra molekyler kommer de mer än gärna ta den möjligheten. Detta är det som ligger bakom de speciella, kemiska egenskaperna hos vattenlösningar av syror. Syrors egenskaper Syror kan ge mat sur smak och det är genom att oxoniumjoner kan ta sig in i smakcellerna och där få andra positiva joner att flytta på sig, vilket ger upphov till nervsignaler som hjärnan sedan i sin tur tolkar som sur smak. Syror kan vara frätande och skada naturen. Även det har med oxoniumjonerna att göra. Bl a kan de byta ut andra positivt laddade joner som sitter fast i marken och som exempelvis kan vara gifitiga tungmetalljoner. Att syrorna är frätande beror på att det i kroppen finns ämnen som är mer benägna att ta upp vätejoner än vatten. Spill av syralösning på t ex händer innebär att just sådana ämnen tar upp vätejoner och därmed får ändrad struktur och funktion. Eftersom molekylerna inte länge fungerar som de ska uppkommer en skada och kroppen varnar genom att skicka smärtsignaler när det blir för mycket oxoniumjoner på samma ställe. Surhetsgraden Det är ofta intressant att veta hur stor koncentration oxoniumjoner, dvs hur många oxoniumjoner per liter, det finns i en lösning. Medan en lösning med låg koncentration oxoniumjoner på sin höjd kanske smakar surt, kan en lösning med hög koncentration vara mycket frätande. Ju högre koncentrationen av oxoniumjoner är, desto surare är lösningen. I artikeln om pH-värde berättar vi mer om hur man mäter hur sur en lösning är. Men just nu ska vi i stället reda ut vad som påverkar hur sur en lösning blir. En sak som är lätt att inse direkt, är att det spelar roll hur många syramolekyler vi har löst upp i varje liter lösning, det vill säga hur stor koncentrationen av själva syran är. Många syramolekyler kommer ju naturligtvis att ge många oxoniumjoner. 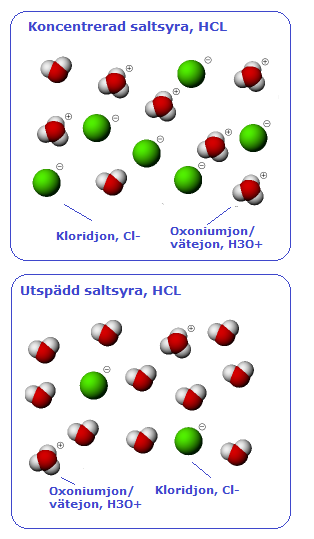
Vissa syror är Andra syror, som t ex 
Vanliga syror Referens = naturvetenskap.org [chemfile(), file(), referens i dokument]
Råbensen innehåller 10-15% toluen. Referens = SSAB Luleå [chemfile(), chemdata.dat, referens i dokument] Toluen irriterar och torkar ut huden. Ångorna verkar irriterande på andningsvägar och ögon. Toluen tränger med lätthet in i kroppen både vid inandning och hudkontakt. Akut förgiftning yttrar sig i huvudvärk, yrsel, trötthet och illamående. Vid höga halter kan toluen ge upphov till omtöckning och medvetslöshet. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), chemdata.dat, referens i dokument]
Plaster Skillnaden mellan termoplaster och härdplaster är att termoplasternas molekyler är långa kedjor medan härdplasternas molekyler har nätstrukturer eller är ännu mer komplicerade. De flesta termoplaster kan värmas så att de blir mjuka och kan formas om. Det är omöjligt med en härdplast. När härdplasten värms tillräckligt mycket bryts den ner och polymeren sönderdelas, s k termisk sönderdelning. Vid nedbrytningen frigörs gaser, ångor och partiklar som kan vara hälsofarliga. Exempel på härdplaster är akrylat-, amino-, epoxi-, feno-, polyester- och polyuretanplast. 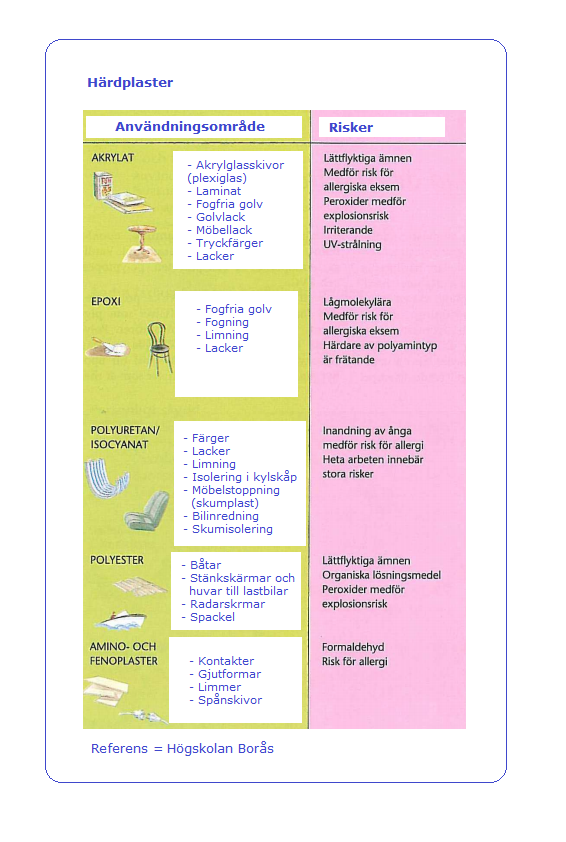
Referens = Högskolan Borås [chemfile(), file(), referens i dokument] Härdplaster Några vanliga härdplaster är Referens = Arbetsmiljöupplysningen [chemfile(), file(), referens i dokument] Arbetsmiljöupplysningen ägs av Prevent, en ideell förening som ägs av Svenskt Näringsliv, LO och PTK.
Akrylater och cyanoakrylater Akrylater används vid tillverkning av akrylatplast men ingår också i lim och UV-härdande akrylatlack. Arbete med akrylater innebär risk för allergi. Vid arbete med vissa akrylater inklusive cyanoakrylater 1) (härdplaster som ingår i vissa härdande limmer, lacker och andra härdande material) finns därför krav på - Utbildning - Läkarundersökning 1)
Cyanoakrylatlim Cyanoakrylatlim är ett mycket starkt lim som härdar i kontakt med luftfuktigheten på några sekunder. Cyanoakrylater som ingår i snabbhärdande cyanoakrylatlimmer är starkt hudirriterande och arbete med dessa limmer innebär risk för allergiskt kontakteksem. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument] Information om risker och skyddsåtgärder De som arbetar med eller leder arbete med allergiframkallande ämnen måste få information om riskerna och hur arbetet ska utföras och vilka åtgärder som ska vidtas för att undvika kontakt med de allergiframkallande ämnena. Utbildning Utbildning krävs för de som arbetar med eller leder arbete där - Metakrylater eller akrylater som är märkta med H317 eller H334 används 2) - Kemiska produkter används som innehåller etyl-2-cyanoakrylat eller metyl-2-cyanoakrylat om arbetet sammanlagt pågår mer än 30 minuter per vecka 2)
H334 = Kan orsaka allergi- eller astmasymtom eller andningssvårigheter vid inandning Alla som utför arbeten, men också de som är arbetsledare för dem, måste ha utbildning om riskerna i arbetet och om vilka skyddsåtgärder som kan behövas för att arbetet ska kunna göras på ett säkert sätt. Läkarundersökning Läkarundersökning krävs för alla som arbetar med eller kommer att arbeta med kemiska produkter som innehåller Arbetsmiljöverkets föreskrifter (regler) Regler om hur akrylater ska hanteras på arbetsplatser finns i Arbetsmiljöverkets föreskrifter om Kemiska arbetsmiljörisker. Hygieniska gränsvärden finns i Arbetsmiljöverkets före skrifter om Hygieniska gränsvärden. Referens = Kemiguiden, Prevent [chemfile(), file(), referens i dokument] (regler)
Här menas inte det som i målarbranschen benämns som akrylatfärg som är vanlig målarfärg där eventuell allergiklassning beror på tillsats av konserveringsmedel. Referens = Kemikalieinspektionen [chemfile(), file(), referens i dokument]
Akrylater Akrylater är kemiska föreningar (akrylestrar) som bildas då akrylsyra (C2H3COOH) eller akrylsyraföreningar reagerar med alkoholer. Akrylatfärger innehåller någon form av akrylat som bindemedel. Det kan vara polyakrylat, multifunktionella akrylater, tri- eller difunktionella akrylater samt monomera akrylatföreningar. I färg som innehåller härdande akrylat kan det finnas tillsatser av oorganiska peroxider för att påskynda polymerisationen (accelator vid härdningen) varigenom produkten härdar till en hård plast, Akrylatfärgerna kan indelas i
Akrylatfärger, förutom latexfärger, är härdande färger och de används bl a inom tryckerier och möbelindustrin. Latexfärger är vattenburna och de flesta innehåller dessutom en liten mängd lösningsmedel. Den här typen av färger är icke-härdande och stelnar istället genom att lösningsmedlet avdunstar. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument]
Epoxi och syraanhydrider Epoxi ingår i bl a lim och lack. Vid arbete med epoxi används ofta härdare som består av syraanhydrid. Arbete med epoxi innebär risk för allergi. Vid arbete med Krav på utbildning gäller för allt arbete med epoxiplastkomponenter och syraanhydrider, dvs de ämnen (bas och härdare) som blandas då epoxilim och epoxilack används. Utbildning Utbildning krävs för alla som arbetar med eller leder arbeten där epoxiplastkomponenter eller syraanhydrider används. Läkarundersökning Läkarundersökning krävs för alla som arbetar med eller kommer att arbeta med kemiska produkter som innehåller syraanhydrider. Anställda som arbetar med produkter som innehåller epoxiplastkomponenter ska erbjudas läkarundersökning. Arbetsmiljöverkets föreskrifter Regler om arbete med epoxi finns i Arbetsmiljöverkets föreskrifter om Kemiska arbetsmiljörisker. Referens = Kemiguiden, Prevent [chemfile(), file(), referens i dokument]
Kemiska produkter av typ epoxi består av - Epoxiharts - Härdare - Tillsatsmedel, t ex acceleratorer som påskyndar härdningen - Lösningsmedel Epoxiplast är en Epoxiharst och härdare ingår ofta som bindemedel i - Lim - Fogmaterial - Färger - Golvbeläggning - Isoleringsmaterial Andra användningsområden för epoxi - Formgodslim - Gjutharts - Isolering av elkomponenter - Laminat - Ytbeläggning - Båtskrov - Kretskort Riskinformation Epoxi är allergiframkallande. Det finns risk för hudallergi vid arbete med epoxiprodukter. Olika typer av epoxiprodukter har olika förmåga att framkalla allergi. Flytande epoxiharts är mycket allergiframkallande. Även härdarna kan vara allergiframkallande. Vissa typer av härdare kan ge luftvägsallergier. Lösningsmedlet kan ge upphov till hudirritation och kontakteksem. Det finns risk att bli allergisk mot epoxi redan första gången som exponering sker. Det är också möjligt att klara arbeta med epoxi under lång tid och sedan plötsligt bli allergisk. Epoxiplast som härdat kan innehålla 5-20% allergiframkallande monomerer, som vid t ex slipning kan ge upphov till allergiframkallande damm. Monomerer är epoxiharts som inte reagerat med härdaren. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument]
Isocyanater Isocyanater används vid tillverkning av skumplast och ingår också i t ex polyuretanlack och polyuretanlim. Arbete med isocyanater innebär risk för allergi. För produkter som är märkta med faroangivelserna H334 eller H317 finns krav på utbildning och läkarundersökningar 1). 1)
H334 = Kan orsaka allergi- eller astmasymtom eller andningssvårigheter vid inandning Utbildning Utbildning krävs för alla som arbetar med eller leder arbete där isocyanater (diisocyanater) används. Läkarundersökning Läkarundersökning krävs för alla som arbetar med eller kommer att arbeta med kemiska produkter som innehåller isocyanater (diisocyanater). Arbetsmiljöverkets föreskrifter Regler om hur isocyanater ska hanteras på arbetsplatser finns i Arbetsmiljöverkets föreskrifter om Kemiska arbetsmiljörisker. Hygieniska gränsvärden finns i Arbetsmiljöverkets före skrifter om Hygieniska gränsvärden. Referens = Kemiguiden, Prevent [chemfile(), file(), referens i dokument]
Isocyanaterna kan delas upp i fyra olika typer - Monoisocyanater - Diisocyanater - Prepolymeriserade isocyanater - Blockerade isocyanater. Isocyanater är en grupp kväveföreningar som är mycket reaktiva ämnen och de har en omfattande teknisk användning och gemensamt för dessa är att de medför hälsorisker framförallt vid inandning. Det är isocyanatgruppen/grupperna, som består av kväve, kol och syre, som gör dessa ämnen så reaktiva och farliga. Eftersom Prepolymeriserade isocyanater För att minska avdunstningen (ångtrycket) och därmed förbättra arbetsmiljön används även diisocyanater som prepolymeriserats. Då är diisocyanaten delvis förpolymeriserad (reagerat till korta kedjor) och får härda färdigt efter applicering på plats i t ex i färg och lim. Andra exempel på produkter av den här typen är isoleringsskum i sprayburkar som används för att isolera mellan vägg och fönster- och dörrkarmar. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument]
Isocyanater Isocyanat är ett kemiskt ämne som innehåller gruppen -N=C=O på en alkylkedja eller en aromatisk ring 1). 1)
Isocyanater används som råvara vid framställning av polyuretan (PUR) som förekommer i plast och som bindemedel i lim, färg och lack. Polyuretan bildas efter en reaktion mellan diisocyanat och en förening med flera hydroxylgrupper, en polyol. Indelning Ämnesgruppen isocyanater kan indelas i mono-, di- och polyisocyanater beroende på antalet isocyanatgrupper. Diisocyanater, som har två reaktiva isocyanatgrupper, är de mest använda och vanligast är difenylmetandiisocyanat, toluendiisocyanat, hexametylendiisocyanat och isoforondiisocyanat. Farlighet Isocyanater förekommer både som vätskor och som pulver. Vätskorna kan avge ångor som är farliga redan vid rumstemperatur. Generellt gäller att isocyanater kan ge allergier vid hudkontakt eller inandning, skador i andningsorganen vid inandning av ångor eller aerosoler. Vissa isocyanater kan orsaka cancer. En del är också klassificerade som miljöskadliga, eftersom de är giftiga för vattenlevande organismer. Arbetsmiljö Problemen i arbetsmiljön kan minskas genom att göra diisocyanaterna mindre flyktiga eller reaktiva. Det finns två sätt att göra det på, antingen genom att prepolymerisera eller förreagera diisocyanaterna, eller genom att blockera dem. I båda fallen framställs en större molekyl. Det förekommer dock alltid rester av fri diisocyanat i prepolymeriserade eller blockerade produkter. Referens = Kemikalieinspektionen [chemfile(), file(), referens i dokument]
Polyester Polyester är en typ av polymer som finns både som härdplast (i omättad form) och som termoplast (i mättad form). De kallas även esterplaster. Polyester används som harts tillsammans med armeringsmaterial som kolfiber, aramid- eller glasfiber i plastkompositer (båtbyggen, bilkarosser, flygplan mm), som gjutmassa i produktionsindustrin och som konstfiber i textilier, kläder och kardborreband, ofta i friluftskläder (t ex polyesterfleece), eftersom materialet har låg vattenupptagning. Polyester framställs genom blandning av omättad polyesterharts (styren) och en härdare (en peroxid). För att påskynda reaktionen (härdningen) brukar också tillsättas en accelerator, i regel en kemisk förening där kobolt ingår. Polyester i kemiska produkter Plastic padding och polyesterlim innehåller styren och peroxid som härdare. Arbetsmiljö Styren är irriterande på andningsvägar och ögon samt irriterar och torkar ut huden. Den tränger med lätthet in i kroppen både vid inandning och hudkontakt. Vid upprepad hudkontakt kan huden bli uttorkad och inflammerad och icke-allergiskt kontakteksem kan uppstå. De flesta organiska peroxider verkar starkt iriterande på ögon, andningsvägar och slemhinnor och de flesta är också klassificerade som hälsofarliga. Arbetsmiljöverkets föreskrifter Regler om hur kemiska produkter som innehåller polyester (styren) och peroxider ska hanteras på arbetsplatser finns i Arbetsmiljöverkets föreskrifter om Kemiska arbetsmiljörisker. Hygieniska gränsvärden finns i Arbetsmiljöverkets föreskrifter om Hygieniska gränsvärden.
Användning Tegel används för murning av infordringen i skänkar, gjutlådor och torpedon. LD-konverten har en tjock infodring av ett speciellt keramiskt tegel. Tegel och tapphål slits och måste bytas ut med jämna mellanrum. Torpedo är en cylinderformad tegelinfodrad järnvägsvagn som används för att transportera flytande råjärn Tillverkning Tegel framställs från oorganiska ämnen (leror, aluminiumoxid, magnesiumoxid, blandning av magnesiumoxid och kromoxid, kiseldioxid, karbider). Vid framställning av tegel från leror som huvudsakligen innehåller vatten, aluminiumoxid och kiseldioxid fås ett material som kallas Tillsätts extra aluminiumoxid fås ett tegel som benämns Tegel som tål högre temperaturer än chamotte- och aloxidtegel består i regel av oxider och karbider, t ex magnesiumoxid eller blandningar av magnesiumoxid och kromoxid. Tillsättning av tjära eller beck till tegel görs för att uppnå en viss kolhalt i materialet. Kolet har bl a till uppgift att stoppa infiltration av ämnen som kan skada teglet. Vidare reducerar det järnoxider till metalliskt järn som inte är lika skadligt för teglet. Tegel kan delas upp i - Tegel utan kemiska tillsatser - Tegel med tjära eller beck - Tegel med fenolharts - Tegel med kromit, utan kemiska tillsatser Hälsorisker Risk för exponering för silikosframkallande kvartsdamm vid dammande hantering, t ex mekanisk bearbetning av tegel eller rivning av murad keramik. Kvartsdamm kan också finnas som ett pulver på tegel vid leverans. Kvarstformer av kiseldioxid, SiO2 Vid tillverkning av tegel från lera som innehåller kiseldioxid (SiO2) bildas kvartsformerna av kiseldioxid (alfa-kvarts, kristobalit och tridymit). Det innebär att dammande hantering t ex mekanisk bearbetning av tegel eller rivning av murad keramik i skänkar, gjutlådor, torpedon eller infodringar, kan medföra risk för exponering för kvartsdamm. Exponering för respirabelt kvartsdamm under lång tid kan förorsaka silikos. Dammpartiklar betecknas som respirabla (inandningsbara) om de är så små att de kan nå till lungans finaste förgreningar, respirabla partiklar har i allmänhet en diameter som är mindre än 0,005 mm. Krom [chemfile(), nC=0 nr=krom, f1=/produkt/info/html/krom.htm] Krom i keramiska produkter föreligger nästan alltid i form av 3-värt krom bunden som kromit, 6-värt krom (kromater) kan förekomma som förorening. Kromit (Fe2CrO4) är ett mineral som innehåller järn och 3-värt krom. Kromater är 6-värda kromföreningar och de är allergiframkallande. Det är 6-värda kromföreningar i keramiska produkter som leder till uppkomst av allergiskt kontakteksem. Mekanisk bearbetning av tegel som innehåller krom kan medföra risk för exponering för allergiframkallande kromdamm. Referens = Järnbruksförbundets skyddsblad [chemfile(), file(), referens i dokument] Den som blivit allergisk kan vid kontakt med, mycket små mängder, såväl 6-värt som 3-värt krom utlösa den allergiska reaktionen. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellstenn [chemfile(), file(), referens i dokument] Tjära eller beck Tegel till slagglinjen kan innehålla bindemedel av typ Fenolharts Fenol och fenolämnen är irriterande på ögon, luftvägar och slemhinnor. Dessa ämnen har dessutom obehaglig lukt redan vid låga koncentrationer. Tegeldamm Tegeldamm har en uttorkande effekt vilket kan ge upphov till hudirritation. Referens = Järnbruksförbundets skyddsblad [chemfile(), file(), referens i dokument]
(RH)
RH-processen RH-processen är uppkallad efter de två företag, Ruhrstahl och Heraeus, som utvecklade den. 1)
ppm (parts per million) är en förkortning för miljondel på samma sätt som procent för hundradel och promille för tusendel. För att omvandla lufthalter av gaser och ångor mellan ppm och mg/m3 går det att räkna ut ett omvandlingstal genom att dividera ämnets molekylvikt med 24. T ex är molekylvikten 97 för diklormetylen (C2H2Cl2) och omvandlingstalet är då 4,0. För att omvandla från ppm till mg/m3 multipliceras ppm med omvandlingstalet. T ex är 20 ppm diklormetylen 20*4=80 mg/m3. För att omvandla från mg/m3 till ppm ska mg/m3 divideras med omvandlingstalet. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument] Referens = Jernkontoret, Stockholm [chemfile(), file(), referens i dokument] Tillsatsen av legeringar kan ske automatiskt eller manuellt. Det finns en legeringssluss för tillsats av legeringar under vakuum. Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
LD LD-konvertern består av en yttre mantel av stål som omsluter infodringen, dvs de keramiska materialen. Väggarna och bottnen i konvertern är infodrade med eldfast tegel med en begynnelsetjocklek på 0,6 - 1 m. Tegel Tegel och tapphål slits och måste bytas ut med jämna mellanrum. Olika varmsprutningsprodukter används för underhåll av botten, tapp och tapphål i konvertern. Infodringarna utsätts för olika påfrestningar beroende på det berörda området. Korrosion och slaggpenetration i botten, termisk avspaltning i den övre koniska delen (området vid dysor, formor och där material chargeras), nötning och mekaniska skador i chargeringsområdet. Olika keramiska material används för underhåll och reparationer av slitfodret. Närmast manteln ligger ett bakfoder med en tjocklek på 150 mm, som består av ett keramiskt lager av tegel, t ex magnesittegel. Efter bakfodret finns ett slitfodret som består av tegel, t ex tjärbunden kolmagnesit tegel med kolhalter på 10 mm i väggar och 15 mm i botten. Slitfodret i väggar har en tjocklek på 650 mm och i botten är slitfodret 1000 mm. LD-slagg Eftersom LD-slagg är basiskt utgörs infodringen av basiska material för att förhindra att aggressiv slagg reagerar med teglet och därmed ökar slitaget. LBE - Lance Bubbling Equipment Som ett komplement till syrgasblåsning i LD-konverter finns bottenspolning med syrgas, LBE - Lance Bubbling Equipment, för att bl a uppnå en mer effektiv omrörning. Den här tekniken tillämpas av SSAB och består av spolelementen som har en tjocklek på 1100 mm och består av tegel, t ex fenolhartsbunden magnesit tegel med en kolhalt på 14%. Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
Stålskänkens uppbyggnad Stålskänken har en toppdiameter på 3,5 m och en bottendiameter på 3,2 m. Mantelplåten är 30 mm tjock i väggen och 55 mm tjock i botten. Vägg och botten Väggen och botten är infodrade med en 5 mm tjock isolerduk. Därefter muras botten ett varv med ett 32 mm tjockt isolertegel. Ovanpå detta muras ett 53 mm tjockt säkerhetstegel. Efter att dessa två tegelvarv i botten murats, muras väggen med samma sorts isolertegel och med en annan sorts säkerhetstegel. Tjockleken på säkerhetsteglet i väggen är 32 mm. När säkerhetsteglet murats i både botten och vägg gjuts botten med ett 300 mm tjockt slitfoder. Då detta har torkat gjuts väggens slitfoder. Tjockleken på detta är 170 mm. Slagglinjen När gjutningsprocessen är klar och keramiken har torkat muras slagglinjen. Slagglinjen består av 8 varv tegel t ex kolmagnesittegel. Tegel till slagglinjen kan innehålla bindemedel av typ Spolstenar I botten på skänken finns 2 stycken spolstenar som sitter i ett megablock. Genom spolstenarna spolas argon under skänkmetallurgibehandling. Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
En torpedovagn (torpedo) är en cylinderformad tank för flytande råjärn formad som en torped och fodrad med 120 ton tegel. Torpedovagnen fylls med 300 ton råjärn från masugnen och transporteras på järnväg till stålverket med ett lok. Efter att råjärnet har hällts över i skänkar transporteras den tömda torpedovagnen tillbaka till masugnen. [chemfile(), nC=0 nr=1212-1, f1=/produkt/info/html/1212-1.htm] Tegel till torpedon kan innehålla bindemedel av typ fenolharts. [chemfile(), nC=0 nr=fenol_t, f1=/produkt/info/html/fenol_t.htm] Om bindemedel i tegel eller murad keramik innehåller fenol/ fenolharts finns ofta små mängder av ämnet som inte har reagerat till en kemisk förening och då kan vid torkning av murad keramik, t ex vid torkning av skänkar i torkstation, fenol avges i början av torkningsprocessen. Även andra fenolderivater 1) kan bildas då fenol/fenolharts utsätts för höga temperaturer. Expositionsnivåer för skadeverkningar för dessa fenoler är mycket varierande och många av ämnena är dåligt utredda med avseende på hälsorisker. 1)
Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
Med hydrauloljor överförs kraft i många olika slags fordon och arbetsmaskiner. Hydraulolja består vanligen av mineralolja, men i en del fall används syntetiska och vegetabiliska oljor. I många fall gör brandrisken det nödvändigt att använda mineralolja, som är betydligt mindre brandfarlig. Vid hög brandrisk kan specialoljor användas, som kan vara vattenburna eller baserade på brandhärdiga ämnen som fosfatestrar. Användningen av hydraulvätskor bidrar till att spara energi. Hydraulvätskor kan dock oavsiktligt läcka ut i miljön. Referens = Arbetsmiljö från A till Ö [chemfile(), file(), referens i dokument]
En hydraulvätska har många krav som den ska uppfyllas. Överföra energi Ska så effektivt som möjligt överföra energi från pump till motorer och cylindrar. Täta Vätskan ska kunna täta mellan spalter och spel i motorer, ventiler och pumpar. Smörja Utveckla en stabil smörjfilm vid höga belastningar, smörja vid höga hastigheter samt ge gränsskiktssmörjning vid låga hastigheter och tunn oljefilm. Kyla Vätskan ska transportera bort värmen som uppstår på grund av förluster och avge den i kylare och tank. Korrosionsskydd En viktig uppgift för oljan är att korrosionsskydda komponenter både under drift och lagring. Luftavskiljning Oljan ska kunna transportera luft från komponenter till tank och där snabbt avge luften. Vattenavskiljande Allt fritt vatten ska bort från systemet och lämnas på botten av tanken eller i filter (gäller inte vattenbaserande vätskor). Kemiskt stabil Inte brytas ner i systemet och skapa föroreningar eller angripa tätningsmaterial. Referens = Institutet för tillämpad hydraulik, Örnsköldsvik [chemfile(), file(), referens i dokument]
Den vanligaste hydrauloljan, som består av mineralolja, kan ge upphov till oljeakne. De huvudsakliga hälsoriskerna med hydrauloljor härrör dock ofta inte från basoljan utan från olika tillsatsmedel. Referens = Arbetsmiljö från A till Ö [chemfile(), file(), referens i dokument]
En svensk standard, SS 15 54 34, har utarbetats av SIS1 som bl a ställer miljökrav på hydraulvätskor/oljor. 1SIS, Swedish Standards Institute, är en medlemsbaserad, ideell förening som är specialiserad på nationella och internationella standarder. Hydraulvätskor/oljor bör uppfylla samtliga miljöegenskapskrav enligt svensk standard 15 54 34. Miljökraven innebär att hydraulvätskor ska bl a vara biologiskt nedbrytbara samt ge minimerad vattentoxicitet. Kraven innebär också bl a en kontroll av allergiframkallande ämnen samt ämnen med särskilt hälso- och miljöfarliga egenskaper (CMR, PBT2). 2 CMR = Cancerframkallande, Mutagena och Reproduktionsstörande PBT = Persistent (svårnedbrytbart), Bioackumulerande (som ansamlas i levande organismer) och Toxisk (giftigt) Referens = SP, Sveriges Tekniska Forskningsinstitut, Borås [chemfile(), file(), referens i dokument]
Rengöringsmedel innehåller förutom vatten en blandning av en mängd kemikalier. Det kan vara tensider, frätande syror/alkalier, lösningsmedel, konserveringsmedel, slipmedel, färg och parfym. Blanda aldrig olika sorters rengöringsmedel. Starkt sura och starkt alkaliska lösningar reagerar häftigt med varandra och det kan bildas giftiga gaser. pH är ett värde för surhet och mäter aktiviteten av vätejoner i en lösning. pH-skalan går från 0 till 14, pH 0 är surt, pH 7 neutralt och pH 14 basiskt. För rengöringsmedel brukar alkaliskt användas istället för basiskt. Ju längre från pH 7 produkten hamnar desto aggressivare är lösningen. pH är ett logaritmiskt mått på surhet, dvs på aktiviteten av vätejoner (H+) i en lösning (egentligen hydroniumjoner, H3O+, en vattenmolekyl med en extra proton dvs en extra H+). Lösningar med låga pH-värden är sura, och de med höga kallas basiska. Neutrala är ämnen som har pH 7 (vid rumstemperatur). En stark syra med hög koncentration (egentligen aktivitet) har ett pH-värde på runt 0, en stark bas med hög koncentration (egentligen aktivitet) har pH ungefär 14. Lågt pH är surt. Ju lägre pH-värde, desto surare är det. Ämnet svavel har pH-värdet 1, väldigt surt. Citronen har pH-värde 3, ganska surt. pH-värdet 7 är neutralt. Det är varken surt eller basiskt (basiskt är motsatsen till surt). Neutralt vatten har ett pH-värde på 7. Om vattnet har pH 6 är det väldigt surt. I pH-skalan är en enhet mindre 10 gånger surare, pH=6 är 10 gånger surare än pH=7, pH=5 är 100 gånger surare än det neutrala pH=7. Referens = Svenska Golvrådet, Förlags- och Konferens AB, Stockholm [chemfile(), file(), referens i dokument]
Vid rengöring är det fördelaktigare ur hälso- och miljösynpunkt att använda så neutrala medel som möjligt. Produkten blir aggressivare från bägge hållen ju längre från pH-värde 7 den är. För varje gradering från 7 ökar styrkan i produkten med 10. Vilket innebär t ex att pH=8 är 10 gånger mer alkaliskt än pH=7. 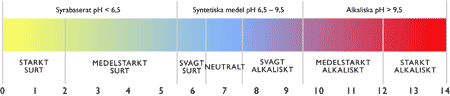
Referens = Svenska Golvrådet, Förlags- och Konferens AB, Stockholm [chemfile(), file(), referens i dokument]
Alkaliska avfettningsmedel är de mest använda. De består normalt av alkaliska salter såsom hydroxider, karbonater, silikater och fosfater samt av tensider där anjon- och nonjontensiderna är de vanligaste. De alkaliska salterna ger avfettningsmedlet ett högt pH. Fosfater kan dessutom fungera som antiredepositionsmedel1) och komplexbildare1) och silikater kan verka korrosionsskyddande. Tensider verkar emulgerande1) och kan dessutom ha en skumdämpande effekt. 1)
Komplexbildare = kemisk förening som har förmåga att komplexbinda metalljoner Emulgator = ett ämne som stabiliserar en emulsion, en emulsion är en dispersion där båda faserna är vätskor Dispersion = en blandning av två faser där den ena bildar partiklar eller vätskedroppar i den andra sammanhängande fasen Sur avfettning kan användas vid lindrigt smutsat gods. Ett surt avfettningsmedel kan bestå av en syra, fosfater, tensider och korrosionsinhibitorer. Exempel på syror är fosforsyra, citronsyra och oxalsyra. Vanligt pH är 2,5-5,5. Förutom avfettande verkan kan ett surt avfettningsmedel även avlägsna rost eller ge en fosfatbeläggning (järnfosfatering). Neutral avfettning är liksom sur avfettning lämplig för lindrigt nedsmutsat gods, och där flera olika metaller ska avfettas. Avfettninsmedlet består främst av en blandning av olika tensider. Vattenbaserad avfettning är överlägsen organiska lösningsmedel när det gäller att tvätta bort oorganiska ämnen, partiklar och filmbeläggning. Den kan anpassas till aktuell situation genom att sammansättning, koncentration och temperatur varieras. Referens = Allmänna råd från Naturvårdsverket som vägledning vid val av avfettningsutrustning [chemfile(), file(), referens i dokument]
Alkaliska ämnen används mest vid rengöring, eftersom de löser fett. Några exempel är lut (natriumhydroxid) i propplösare, målarsoda (natriumkarbonat) som löser fett före målning. Alkaliskt avfettningsmedel används i diskmaskin, men är inte så effektiv på asfalt och tjära. Kännetecknande för alkalisk avfettningsmedel är att de är vattenbaserade, har ett pH-värde över 7 (oftast över 10) samt ska spädas med vatten innan användning. Kalium- och natriumhydroxid är exempel på alkalier som kan ingå i rengöringsmedel av typ alkaliska rengöringsmedel och förekommer i t ex propplösare. Ämnet natriumhypoklorit finns i klorin. Alkaliska rengöringsmedel används för att avlägsna olja, fett, sot, vägsmuts. Produkterna är vattenbaserade och späds ut med vatten. Referens = Hygienteknik AB, Västerås [chemfile(), file(), referens i dokument] Referens = Kemi A, Engström, Backlund, Berger, Grennberg [chemfile(), file(), referens i dokument] Svagt alkaliska rengöringsmedel (pH 8 - 9,5) Används vanligen i den dagliga städningen. Grovrengöring, polishborttagning, rengöring av kök och för industrirengöring. Medelstarkt alkaliskt rengöringsmedel (pH 9,5 - 12) Ett smedel som är lämpligt för fet smuts och hårt smutsade ytor där smutsen sitter fast eller smutsgraden är hög. Kräver vanligtvis eftersköljning. Starkt alkaliska rengöringsmedel (pH 12 - 14) Används för att ta bort fet och ingrodd smuts och för industrirengöring. Kräver vanligtvis eftersköljning. Referens = Svenska Golvrådet, Förlags- och Konferens AB, Stockholm [chemfile(), file(), referens i dokument] Hälsorisker Alkalier är liksom syror frätande och kemiska produkter som innehåller alkalier irriterar därmed hud och ögon och kan även ge frätskador. I säkerhetsdatablad rubrik 3 framgår vilka ämnen som finns i kemiska produkter. Produktens klassificering finns i rubrik 2 och är beroende på mängd ingående ämnen och deras klassificering. Hälsofarligheten med alkaliska rengöringsmedel är beroende på mängd alkalier som ingår i produkten. I Kemikalieinspektionens föreskrifter, KIFS 2005:7, finns formler för beräkning av kemiska produkters klassificering utifrån ingående ämnens klassificering. Referens = CLP-förordningen, förordning (EG) nr 1272/2008 om klassificering av kemiska ämnen [chemfile(), file(), referens i dokument]
Referens = Dahbergs Bilservice AB, Sundsvall [chemfile(), file(), referens i dokument] 1) 2)
Aromatiska kolväten innehåller ringformade kolkedjor av typ bensen, vanlig lacknafta innehåller ca 10-20% aromatiska kolväten, ju mer aromatiska kolväten ett lösningsmedel inndehåller desto hälsofarligare Referens = Arbetsmiljö från A till Ö [chemfile(), file(), referens i dokument] Användningsområden för petroleumavfettningar är fet smuts, såsom olja, fett och tjära/asfalt. Petroleumavfattning är inte vattenspädbar, vilket gör att den måste användas på torra ytor för att ge full effekt. Referens = Dahbergs Bilservice AB, Sundsvall [chemfile(), file(), referens i dokument] Hälsorisker Lacknafta irriterar och torkar ut huden och kan ge upphov till icke allergiskt kontakteksem. Ångorna verkar irriterande på ögon och andningsvägar. Lågaromaisk lacknafta innehåller betydligt mindre andel aromatiaka kolväten, sådan lacknafta är fördelaktigare med avseende på hälsorisker. Referens = Arbetsmiljö från A till Ö [chemfile(), file(), referens i dokument]
Kallavfettning är den typ av avfettningsmedel som används för avfettning vid tvättning av t ex bilar. Avfettningsmedel av den här typen innehåller ca 90-95% lösningsmedel och resten är ytaktiva ämnen (emulgatorer). Kallavfettning löser fett, olja, asfalt och vax. Beroende på vilket lösningsmedel som produkten innehåller har den olika snabb effekt. Ett starkt lösningsmedel kräver mindre verkningstid för att ha samma effekt som ett mindre starkt lösningsmedel. Ju mer det luktar, desto effektivare är produkten, men även mer skadligt för miljön och hälsan. Vanliga lösningsmedel i kallavfettningsmedel är lacknafta (White spirit), lågaromatiska naftor, iso- och normalparaffiner. Kallavfettningsmedel ska inte blandas med vatten. Om den blandas med vatten bildas en vit sörja som ganska snabbt separerar. Eftersom kallavfettning inte är blandbar med vatten, kan lösningsmedlet separeras från vattnet i en oljeavskiljare i t ex biltvättar. Referens = Kemi A, Engström, Backlund, Berger, Grennberg [chemfile(), file(), referens i dokument] Hälsorisker Hälsoriskerna med kallavfetnningsmedel är beroende på typ av lösningsmedel som produkten innehåller. Lacknafta irriterar och torkar ut huden och kan ge upphov till icke allergiskt kontakteksem. Ångorna verkar irriterande på ögon och andningsvägar. Lågaromaisk lacknafta innehåller betydligt mindre andel aromatiska kolväten1), sådan lacknafta är fördelaktigare med avseende på hälsorisker. Undvik att använda lösningsmedel som innehåller n-Hexan. 1)
Miljörisker Många typer av lösningsmedel är toxiska för vattenlevande organismer, svårnedbrytbara och kan ackumuleras i biologiskt material. Exempel är etylbensen, xylener, trimetylbensener och cyklohexan. Referens = Arbetsmiljö från A till Ö [chemfile(), file(), referens i dokument]
I en Mikroemulsion finns lite av den alkaliska avfettningens rengörande egenskaper, t ex sot och pigmentsmuts, där finns även lösningsmedel från kallavfettningen som ger bra olje-och asfaltlösande egenskaper. Vid avfettning med mikroemulsioner förenas principerna för avfettning med vattenbaserade system och lösningsmedelssystem. Referens = Kemi A, Engström, Backlund, Berger, Grennberg [chemfile(), file(), referens i dokument] Mikroemulsioner 1), även kallade mikroavfettningar, är en kombination av alkalisk avfettning och kallavfettning och innehåller både alkaliska ämnen, lösningsmedel och tensider. Löser effektivt upp asfalt, tjära och vägsmuts. Mikroemulsioner som används för avfettning innehåller organiskt lösningsmedel (10-30%) dispergerat i vatten. Dispersionen 1) fås genom en tillsats av tensider (7-25%) och löslighetsförmedlare. Den organiska fasen kan t ex bestå av alifatiska kolväten, terpener eller mjölksyraestrar. Exempel på andra kemikalier som förekommer är komplexbildare och korrosionsinhibitorer. 1)
Emulsion = en dispersion där båda faserna är vätskor I mikroemulsioner är de dispergerade dropparna betydligt mindre och mängden tensid ofta betydligt högre än i andra emulsioner. Mikroemulsioner kan spädas med vatten, men inte lika mycket som en alkalisk avfettning. Vintertid inte mer än 1:1 för att ha kvar den avfettande förmågan. Övriga årstider går det att späda 1:3-1:5. Vid avfettning med mikroemulsioner har valet av lösningsmedel betydelse för hur allvarlig hälso- och miljöpåverkan blir. Alla lösningsmedel innebär en påverkan ur miljö- och hälsosynpunkt. Hälsorisker Lösningsmedel i mikroemulsioner kan vara irriterande på luftvägarna. Flertalet lösningsmedel kan vid långvarig hudkontakt framkalla irritation, sprickbildning samt i vissa fall eksem. Aromatiska kolväten1) som toluen och xylen kan i relativt låga halter påverka det centrala nervsystemet. 1)
Miljörisker Många typer av lösningsmedel är toxiska för vattenlevande organismer, svårnedbrytbara och kan ackumuleras i biologiskt material. Exempel är etylbensen, xylener, trimetylbensener och cyklohexan. Referens = Allmänna råd från Naturvårdsverket som vägledning vid val av avfettningsutrustning [chemfile(), file(), referens i dokument]
Syra som rengöringsmedel används för sanitetsrengöring. Det kan vara t ex citronsyra eller fosforsyra. Sura rengöringsmedel kan också användas för att ta bort kalkfläckar i t ex handfat i toaletter och i duschrum. Sura rengöringsmedel används också för att avlägsna oxidbeläggningar på fälgar till bilar. Produkterna kan även användas för borttagning av industrinedfall och järnoxider. Det finns även produkter för borttagning av kalk, cement, rost och järnfläckar. Sura avfettningar används även för betning av stål för t ex avlägsning av ytrost eller glödskal. Produkterna lämpar sig även för systemrengöring av t ex indunstaranläggningar och ytbehandlingsanläggningar. Sura rengöringsmedel har ett lågt pH-värde, under 7. Vissa produkter ska spädas med vatten. Tänk på att hälla syran i vattnet, inte tvärtom. Referens = Chemstore Scandinavia AB, Göteborg [chemfile(), file(), referens i dokument] Syrarengöringsmedel kan inte innehålla tvål, utan istället används syrastabila tensider (ytaktiva ämnen som ger resultat som liknar tvål) och kanske en typ av organiskt lösningsmedel som löser upp fett och ändå är lösligt i vatten.
Referens = Thord Ohlssons Kemiska AB, Luleå [chemfile(), file(), referens i dokument] Starkt sura rengöringsmedel (pH 0-2) Används för att ta bort kalk, rost och för sanitetsrengöring. Kräver eftersköljning. Medelstarkt och svagt sura rengöringsmedel (pH 2-6,5) Används för lättare rengöring i sanitetsstädning samt där hårt vatten förekommer. I förebyggande syfte, förhindrar att kalkbeläggningar sätter sig. Referens = Svenska Golvrådet, Förlags- och Konferens AB, Stockholm [chemfile(), file(), referens i dokument] Hälsorisker Hälsofarligheten med rengöringsmedel som innehåller syror är beroende på mängd syra som ingår i produkten. Syror är liksom alkalier frätande och kemiska produkter som innehåller syror irriterar därmed hud och ögon och kan även ge frätskador. I säkerhetsdatablad rubrik 3 framgår vilka ämnen som finns i kemiska produkter. Produktens klassificering finns i rubrik 2 och är beroende på mängd ingående ämnen och deras klassificering. Referens = Kemikalieinspektionen [chemfile(), file(), referens i dokument]
Referens = CLP-förordningen, förordning (EG) nr 1272/2008 om klassificering av kemiska ämnen [chemfile(), file(), referens i dokument]
Det lägre pH-värdet, jämfört med alkaliska rengöringsmedel, gör även att produkterna är lämpliga vid avfettning av känsliga metaller som aluminium och förzinkat 1) material. Neutral rengöringsmedel innhåller mjukgörare och tensider 2). 1) 2)
[chemfile(), nC=0 nr=tensid, f1=/produkt/info/html/tensid.htm] En tensid är ett ytaktivt ämne som kan modifiera ytspänningen hos en fasgränsyta, vilket betyder att en del av molekylen är löslig (lyofil) i vatten medan den andra är olöslig (lyofob) I neutrala avfettningsmedel har den traditionella lut-komponenten ersatts med kraftfulla tensidpaket och korrosionsinhibitorer. I praktiken innebär det en produkt med mycket låg salthalt som bidrar till att, om rengöringsmedlet används i en anläggning, hålla anläggningen ren och fri från avlagringar. Vid avfettning av stål med neutrala rengöringssmedel tillförs även ett temporärt korrosionsskydd till metallytan. Neutrala rengöringsmedel kan användas till de flesta ytor som tål vatten. Löser oljor, fett och sot. Referens = Ytteknik, Göteborg [chemfile(), file(), referens i dokument]
I vattenlösningar sträcker sig pH-värdena från -1 i en mycket sur lösning (t ex koncentrerad saltsyra) till ungefär 15 i en starkt basisk lösning (t ex koncentrerad natriumhydroxidlösning). I vattenlösningar finns alltid vätejoner (H+) 1) och hydroxidjoner (OH-). I sura lösningar är det överskott på Neutrala lösningar har 1)
Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), file(), referens i dokument]
pH-värde Det finns ett mått som anger hur sur eller basisk en vattenlösning är och det är Symbolen p i pH anger den negativa 10-logaritmen 1) av vätejonaktiviteten och pH är ett logaritmiskt mått på surhet, dvs på aktiviteten av vätejoner (H+) 2) i en lösning (egentligen oxoniumjoner, H3O+, en vattenmolekyl med en extra proton, dvs en extra H+).
2) Förenklat kan beskrivas att en syra bildar H+ i vattenlösning, H+ är väteatomens kärna och utgörs av en enda proton. Men egentligen är det H3O+ som bildas, eftersom H+ plockas upp av en vattenmolekyl (H2O) och ger H3O+. Ju lägre värde på pH, desto fler H3O+ i lösningen och desto surare. pH-skalan brukar täcka in området mellan 0 och 14, men det kan vara ännu surare (till exempel pH = -2) eller ännu mer basiskt (till exempel pH = 17). Vid pH = 7 är lösningen En Eftersom pH-skalan är logaritmisk innebär det att om det är en skillnad på 1 i pH mellan två lösningar så är skillnaden en faktor 10 i koncentrationen H3O+. Lösningar med låga pH-värden är sura och kallas syror, och de med höga kallas En Vid pH = 1 är vätejonaktiviteten {H+} = 1x10-1. Vid pH = 7 är vätejonaktiviteten {H+} = 1x10-7. Vid pH = 14 är vätejonaktiviteten {H+} = 1x10-14. Mätning av pH-värdet görs vanligen med en kombinationselektrod. Det kan också grovt mätas med pH-indikatorer, kemiska föreningar som har olika färg vid olika pH. Referens = skolverket.se [chemfile(), file(), referens i dokument] Sur lösning En lösnings sura egenskaper beror på en enda positiv jon (laddad atom), nämligen vätejonen H+. Ju högre koncentration av vätejoner desto surare är en lösning. Syror innehåller vätejoner som frigörs när syran hamnar i vatten. Det blir fler vätejoner än hydroxidjoner i lösningen, då blir lösningen sur. Saltsyra kallas för en stark syra därför att alla vätejoner, H+, släpper från sina molekyler, pH är ungefär 0 i saltsyra. Ättiksyra kallas en svag syra. I ättiksyra släpper bara ca 1/1000 av alla vätejoner, H+, när syran blandas med vatten. Därför har en ättiksyralösning inte lika lågt pH som saltsyra. Kolsyra är en ännu svagare syra än ättika, ca 1/10000 av vätejonerna avges. Om en syra är stark eller svag har alltså att göra med hur lätt syrorna delar sig i joner, H+ och OH-, när de blandas med vatten. Basisk lösning Basiska egenskaper beror på hydroxidjonen OH-, en negativ jon. Neutral lösning En sur lösning kan göras neutralt genom att tillsätta hydroxidjoner, t ex natriumhydroxid. En basisk lösning kan göras neutralt genom att tillsätta vätejoner, dvs en syra. Då kommer hydroxidjoner och vätejoner att slå sig ihop till vattenmolekyler och det blir åter lika många väte- och hydroxidjoner. Vatten Uttryckt på vanligt sätt är antalet vätejoner mycket stort i vatten, trots den lilla andelen vattenmolekyler som delar upp sig. Redan i en liter neutralt vatten finns tio miljoner miljarder vätejoner.
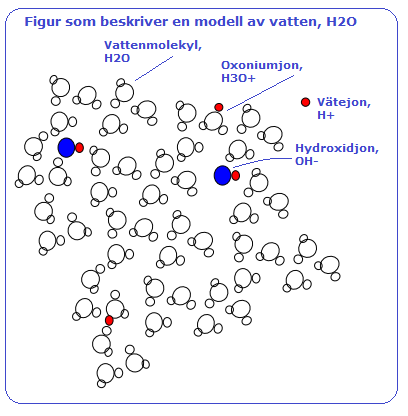
Även rent vatten innehåller vätejoner, en mycket liten andel av vattenmolekylerna (H2O) delar upp sig i en vätejon (H+ dvs oxoniumjon H3O+), och en hydroxidjon (OH-). Vatten är I en liter vatten finns 50x1024 vattenmolekyler (H2O) (50 med 24 nollor efter). Referens = Resurscentrum för kemi, Stockholms Universitet [chemfile(), file(), referens i dokument] För att slippa hantera sådana stora tal infördes pH som ett mått på surt och basiskt. Enligt matematiken1 bakom pH-värdet är pH=7 neutralt. Men ju lägre pH är, desto surare. Högre pH än 7 betyder basiskt. När pH=6 finns det 10 gånger fler vätejoner än när pH=7, pH=5 betyder 100 gånger fler vätejoner än när pH=7, pH=4 betyder 1000 gånger fler osv. För varje steg nedåt i pH blir det alltså 10 gånger surare. 1 [chemfile(), nC=0 nr=fdiv, f1=/produkt/info/html/fdiv.htm]
Vanlig Vid Om En stark lösning av Referens = Resurscentrum för kemi, Stockholms Universitet [chemfile(), file(), referens i dokument]
Isocyanaterna kan delas upp i fyra olika typer - Monoisocyanater - Diisocyanater - Prepolymeriserade isocyanater - Blockerade isocyanater. Isocyanater är en grupp kväveföreningar som är mycket reaktiva ämnen och de har en omfattande teknisk användning och gemensamt för dessa är att de medför hälsorisker framförallt vid inandning. Det är isocyanatgruppen/grupperna, som består av kväve, kol och syre, som gör dessa ämnen så reaktiva och farliga. Eftersom Prepolymeriserade isocyanater För att minska avdunstningen (ångtrycket) och därmed förbättra arbetsmiljön används även diisocyanater som prepolymeriserats. Då är diisocyanaten delvis förpolymeriserad (reagerat till korta kedjor) och får härda färdigt efter applicering på plats i t ex i färg och lim. Andra exempel på produkter av den här typen är isoleringsskum i sprayburkar som används för att isolera mellan vägg och fönster- och dörrkarmar. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument]
Isocyanater Isocyanat är ett kemiskt ämne som innehåller gruppen -N=C=O på en alkylkedja eller en aromatisk ring 1). 1)
Isocyanater används som råvara vid framställning av polyuretan (PUR) som förekommer i plast och som bindemedel i lim, färg och lack. Polyuretan bildas efter en reaktion mellan diisocyanat och en förening med flera hydroxylgrupper, en polyol. Indelning Ämnesgruppen isocyanater kan indelas i mono-, di- och polyisocyanater beroende på antalet isocyanatgrupper. Diisocyanater, som har två reaktiva isocyanatgrupper, är de mest använda och vanligast är difenylmetandiisocyanat, toluendiisocyanat, hexametylendiisocyanat och isoforondiisocyanat. Farlighet Isocyanater förekommer både som vätskor och som pulver. Vätskorna kan avge ångor som är farliga redan vid rumstemperatur. Generellt gäller att isocyanater kan ge allergier vid hudkontakt eller inandning, skador i andningsorganen vid inandning av ångor eller aerosoler. Vissa isocyanater kan orsaka cancer. En del är också klassificerade som miljöskadliga, eftersom de är giftiga för vattenlevande organismer. Arbetsmiljö Problemen i arbetsmiljön kan minskas genom att göra diisocyanaterna mindre flyktiga eller reaktiva. Det finns två sätt att göra det på, antingen genom att prepolymerisera eller förreagera diisocyanaterna, eller genom att blockera dem. I båda fallen framställs en större molekyl. Det förekommer dock alltid rester av fri diisocyanat i prepolymeriserade eller blockerade produkter. Referens = Kemikalieinspektionen [chemfile(), file(), referens i dokument]
Cyanoakrylatlim Cyanoakrylatlim är ett mycket starkt lim som härdar i kontakt med luftfuktigheten på några sekunder. Cyanoakrylater som ingår i snabbhärdande cyanoakrylatlimmer är starkt hudirriterande och arbete med dessa limmer innebär risk för allergiskt kontakteksem. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument]
Anaeroblim (låsvätskor) Anaeroblim härdar i frånvaro av luft vid kontakt med metall. De kallas även för låsvätska, eftersom de främst används vid fixering av gängade förband. Innehåller akrylater som härdar med peroxider. Akrylater är ett samlingsnamn för kemiska föreningar och innehåller monomerer som är irriterande och allergiframkallande. Monomer är utgångsämne vid polymerisation. Polymerisation är en kemisk reaktion där monomerer sammanfogas till långa kedjor som bildar en polymer. Peroxider är kraftigt irriterande på hud, ögon, slemhinnor. Stänk av peroxid kan ge vävnadsskada. Arbetsmiljöverkets föreskrifter Vid arbete med härdplaster, t ex akrylater, måste Arbetsmiljöverkets föreskrift om härdplaster, AFS 2005:18, tillämpas. Det innebär bl a att de som ska arbeta med härdplaster (isocyanater, epoxi, akrylater, cyanoakrylater) ska ha genomgått utbildning. Medicinsk kontroll krävs för de som årligen arbetar med mer än totalt 500 gram härdplastprodukter/år. Medicinsk kontroll krävs också vid arbete med mindre mängder, om riskbedömning visar att det finns hälsorisker med hanteringen.
[chemfile(), nC=0 nr=5400l, f1=/produkt/info/html/5400l.htm] Limmer Lim eller klister är samlingsnamnen på det bindemedel i flytande form som används för att foga tillsammans två eller flera fasta kroppar. Lim för papper, folier och andra tunna eller mjuka kroppar kallas ofta för klister. Lim binder samman föremål genom adhesion till de ytor som ska sammanfogas tillsammans med kohesion inom limfogen, och består ofta av stora molekyler som hänger samman. Det går att dela in lim beroende på deras funktion - Torkande lim, som verkar genom att lösningsmedlet avdunstar - Smältlim, plaster som värms upp till flytande form och som efter avsvalning stelnar och fungerar som ett lim - Härdande lim, lim som verkar genom att det reagerar kemiskt Härdande lim härdar antingen under inflytande av ultraviolett ljus eller värme om det är enkomponentlim, eller genom att baskomponent och härdae reagerar kemisk, dvs ett tvåkomponentlim. Enkomponentlim Enkomponentlim är den vanligaste typen av lim och klister. Allt som behövs för limningen finns i samma tub, burk eller flaska. Oftast härdar limmet genom att dess lösningsmedel dunstar bort i luften och limbasen blir kvar i fogen. Det finns även speciella typer av enkomponentlim, t ex sådana som härdas av ultraviolett ljus eller värme. Somliga häftämnen härdar genom kemisk reaktion med luftens syre eller fuktighet, dvs vatten. Egentligen kan dessa ämnen anses vara tvåkomponentlim, eftersom särskilt härdämne inte behöver tillsättas utan tas från den omgivande miljön. Exempel är silikonlim. Exempel på enkomponent lim är - Trälim - Limstift - Karlssons klister - Superlim (cyanoakrylatlim) - Kontaktlim. Superlim Superlim är produktnamnet för enkomponentlim baserat på cyanoakrylat. Limmet är mycket lättflytande och härdar snabbt, särskilt då det ligger i ett tunt skikt mellan två sammanpressade ytor. Hållfastheten är hög, men förmågan att fylla ut ojämnheter i de sammalimmade ytorna är dålig. Denna egenskap gör dock att en limfog mellan ytor med god passform blir nästan osynlig. Med hjälp av tillsatsämnen kan limmet både göras trögflytande och utfyllande. Superlim fäster bra på de flesta hårda material samt på vissa mjuka material, t ex mellan fingrar. Superlim som inte härdat färdigt kan lösas med aceton. Tvåkomponentlim Limmet består av baskomponent och härdare som förvaras i var sin behållare och som blandas i önskad mängd innan applicering. Oftast är båda komponenterna trögflytande vätskor eller geléer, men pulver/vätska förekommer också. Tvåkomponentlim behöver normalt inte luft för att stelna då en kemisk reaktion inträffar mellan de ingående ämnena. Den tid ett tvåkomponentlim är användbart från blandningstillfället är begränsad och det hjälper inte att förvara blandat lim i slutet kärl för att förhindra härdning. Ett tvåkomponentlim som börjat härda kan inte lösas igen genom att tillsättning av lösningsmedel eller tillförsel av mer av någon av de ingående komponenterna. De flesta tvåkomponentlim krymper inte särskilt mycket när de torkar vilket gör att limmet också kan användas som spackel. Tvåkomponentlim brukar dessutom vara vattenbeständiga. En speciell form av tvåkomponentlim är de limmer där man penslar härdare på den ena ytan och baskomponent på den andra innan ytorna pressas ihop. Det kan vara svårt att lösa upp en limmad fog men limmet kan fås att släppa om man värmer fogen, förutsatt att de sammanlimmade materialen tål det. Efter värmningen har limmet förlorat mycket av sin styrka och man bör inte försöka fästa ihop ytorna igen genom att värma upp limmet. Tvåkomponentlim är lämpligt för porslin, glas, stengods och sten. Exempel på tvåkomonentlim är epoxilim (handelsnamn Araldit, Plastic Padding m fl) och isocyanatlim. Epoxi och isocyanat används som baskomponent i bindemedlet i epoxi- resp isocyanatlimmer. Baskomponenten reagerar med härdaren och bildar limfogen. Vissa material kan sammanfogas genom påpensling av lösningsmedel, som löser upp själva materialet. Exempel på detta är plexiglas, som kan sammanfogas genom påpensling av isättika. Isättikan bidrar inte själv till sammanhållningen, utan sedan den avdunstat återstår bara en fullständigt homogen rymd av plexiglas. Egentligen är denna fogmetod inte limning även om man i dagligt tal kallar det för att limma med isättika.
Den viktigaste beståndsdelen i ett lim är bindemedlet. Som bindemedel kan bl a användas cellulosaprodukter, stärkelse och kemiskt framställda polymerer (plaster). De flesta limmer innehåller späd- eller lösningsmedel, som kan vara vatten eller organiska lösningsmedel. Dessutom brukar limmer innehålla tillsatsmedel av olika slag. En del limmer binder genom att lösningsmedlet avdunstar. Tvåkomponnetlimmer härdar kemiskt genom tillsats av en härdare. Organiska lösningsmedel är hälsofarliga vid inandning och vid hudkontakt. Hälsofarliga ämnen kan finnas i bindemedlet, i härdaren eller som tillsatsämne.
- bindemedel (30%) - lösningsmedel (vatten eller organiska lösningsmedel, 40%) - pigment och fyllnadsmedel (30%) - tillsatsmedel eller additiv (1-3%) Organiska lösningsmedel och olika tillsatsmedel kan medföra hälso- och miljörisker. Benämnningen lack används om särskilda produkter, utan pigment, t ex klarlack består enbart av - bindemedel - lösningsmedel - eventuellt tillsatsmedel Bindemedlet har till uppgift att hålla samman färg- eller lackskiktet och ge det vidhäftning till underlaget. Exempel på bindemedel är - akrylatharts - alkydharts - epoxiharts - polyuretaner (isocyanater) - polyestrar - melaminer - olja eller gummi De olika typerna av färg ges ofta namn efter bindemedlet i färgen, t ex alkydfärg, epoxifärg. Pigmenten ger målarfärgen dess kulör och fyllmedel används för att få en bättre täckförmåga. Lösningsmedlets roll är att göra färgen lättflytande så att den kan appliceras på underlaget. Additiven är tillsatta för att påverka egenskaper som torktid, konsistens, vätförmåga, skinnbildningsförmåga eller skumning, men additiven kan även vara emulgeringsmedel, konserveringsmedel eller pH justerande. I linoljefärg är linolja bindemedel och i vissa linoljefärger är nafta eller terpentin tillsatt som lösningsmedel i färgen. Detta höjer färgens inträngningsförmåga men även dess innehåll av flyktiga organiska ämnen (Volative Organic Compound). Linoljan är ett kemiskt torkande bindemedel, med detta menas att bindemedlet härdar (polymeriseras) genom en oxidationsprocess. Linolja består av triglycerider av fettsyrorna oljesyra, linolsyra, linolensyra, palmitinsyra samt stearinsyra. Dessa fettsyror är delvis omättade, oxidationen av de omättade kolatomerna ger tvärbindningar mellan kolkedjorna, ett polymert nätverk bildas och linoljan härdar. Vattenbaserade färger har ett fysikaliskt torkande bindemedel, här klibbar de dispergerade bindemedelspolymererna ihop då lösningsmedlet avdunstar. I latexfärger kan bindemedlet bestå av polyvinylacetatlatex eller akryllatex. De pigment som används kan vara oorganiska pigment där titandioxid är det dominerande vita pigmentet, till detta kommer fyllmedel som bestå av polyvinylacetatlatex eller akryllatex. De färgade pigmenten kan vara organiska pigmen (syntetiska) eller t ex järnoxider. Linoljefärgen innehåller mangansickativ (mangankarboxylat CAS-nr = 13434-24-7) i en koncentration på 0,07 mg/liter. Ämnet är tillsatt för att påskynda oxidationen av linoljan. Vattenbaserade färger kan innehålla konserveringsmedlen 1,2-benzisotiazol-3(2H)-on, kathon och bronopol. Gemensamt för dessa är att de är mycket giftiga för vattenlevande organismer och att de alla är allergena vid hudkontakt. De konserveringsmedel som förekommer i latexfärger kommer ut i naturen vid rengöring av penslar och rollers och kan på så vis ge upphov till systematiskt ökande koncentrationer av ämnen. De vattenburna färgernas konserveringsmedel kan vara toxiska för vattenlevande organismer och kan orsaka skadliga långtidseffekter i vattenmiljön. Ur miljösynpunkt är linoljefärgen ett bättre alternativ än den vattenbaserade latexfärgen eftersom de konserveringsmedel som finns i latexfärger är skadliga för vattenlevande organismer. I användningsskedet ger linoljefärgen högre emission av flyktiga organiska föreningar än vad den vattenbaserade latexfärgen ger. Latexfärgens innehåll av allergena ämnen samt ämnen med toxisk verkan på vattenorganismer gör att det ändå finns risker i användningsskedet. När färgen torkat är syftet att de kemiska föreningarna ska vara fasthållna av bindemedlet, men även lågemitterande färger har visat sig inte vara helt emissionsfri. Hos utomhusfärger har man i vissa fall sett att det sker en migration och urtvättning av fungicider och konserveringsmedel från färgen. Ångorna från organiska lösningsmedel medför hälsorisker. Vattenbaserade färger kan innehålla små mängder organiska lösningsmedel. Pigment består av finkornigt pulver som bl a ger färgen kulör ochh täckförmåga. Det finns tusentals olika ämnen som kan förekomma som färgpigment. Vid målning med pensel medför pigmenten normalt inga hälsoproblem, eftersom de är mycket svårlösliga i vatten och binds till bindemedlet. Vid sprutmålning ingår emellertid pigmenten i sprutdimman och kan medföra hälsorisker vid inandning. Sådana risker finns också vid slipning och svetsning av målade ytor. Tillsatsmedel finns i alla lacker och färger. För att ge en bättre yta tillsätts t ex glykoler i vattenburna färger. För att justera surhetsgraden tillsätts ammoniak eller aminer. Som mjukgörare kan ftalater ingå. Vattenburen färg innehåller tillsatsmedel för att skydda färgen mot mögel, bakterier och frost samt för att skydda burken mot rost. En del av de konserveringsmedel som används i vattenburen färg kan ge upphov till allergiskt kontakteksem. Vidare kan de antimögel- eller träkonserveringsmedel som ingår i en del lasyrfärger medföra hälsorisker. Lasyr är ett transparent färglager, främst av oljefärg eller akrylfärg, men även vattenfärg förekommer. Epoxifärg I epoxifärger används epoxiharts och en härdare som bindemedel. Referens = Arbetsmiljö från A till Ö och litteratur om teknisk kemi [chemfile(), file(), referens i dokument]
Referens = Arbetsmiljö från A till Ö och litteratur om teknisk kemi [chemfile(), file(), referens i dokument]
Den stora principiella skillnaden mellan olika bindemedel handlar om på vilket sätt färgen torkar. Oljefärger torkar genom en kemisk reaktion med luften, de oxiderar, en relativt långsam process som innebär att oljemolekyler hinner tränga in i träet. Färgtyper baserade på vatten eller organisk lösningsmedel torkar genom att vattnet eller lösningsmedlet avdunstar, en relativt snabb process där färgskiktet helt lägger sig på ytan. Det finns en mängd av emulsionsfärger som i varierande grad kombinerar dessa torkningsegenskaper. Emulsioner innebär att ett emulgeringsmedel har tillsatts färgen, vilket gör att två olika bindemedel som normalt inte löser sig med varandra kan blandas. Latexbindemedel torkar fysikaliskt genom avdunstning av lösningsmedlet vatten. De har normalt inga negativa miljöeffekter och bryts ner långsamt i naturen. De framställs ur bergolja eller naturgas. Proteiner (från kasein och ägg) som kan förekomma i speciella färgtyper, kan vid nedbrytning i färgskiktet under fuktpåverkan avge ämnen som irriterar andningsvägarna och ger obehaglig lukt. Linolja och modifierade oljebindemedel (på linolja, sojaolja och tallolja), sk alkyder, torkar genom kemisk omvandling, luftoxidation. Vid torkprocessen kan flyktiga oxidationsprodukter bildas, som kan verka irriterande på andningsvägarna. Detta gäller speciellt linolja men även andra luftoxiderande oljor och alkyder. Bindemedel baserade på vegetabiliska oljor bryts ned relativt snabbt i naturen. I alkyderna ingår en mindre del av råvaror som har sitt ursprung från bergolja eller naturgas. Andra kemiskt torkande bindemedel är silikat och kalk. Härdlacker (2-komponentsfärger), t ex epoxilacker och isocyanatlacker, ger mycket starka och hållbara ytskikt. Dessa produkter kräver speciella skyddsåtgärder för säker arbetsmiljö. Pigment ger färgen dess kulör och gör att den täcker underlaget.
Pigment, som inte är täckande eller ger någon kulör, kallas fyllnadsmedel. De består av finmalda mineraler, t ex kalksten, krita eller dolomit. Titandioxid är idag det dominerande vita pigmentet. Det är mycket beständigt och har god täckförmåga. Titandioxid är inert ur hälso- och miljösynpunkt och används bl a i tandkräm och andra kosmetiska produkter. Zinkvitt används numera endast i oljefärg, där dess viktigaste uppgift är att ta hand om linoljans nedbrytningsprodukter i utomhusfärger och därmed förbättra hållbarheten. Zink i alla former utgör en negativ belastning på miljön varför man försöker undvika användning av zink i färger. Järnoxidpigment innebär normalt sett inga hälsorisker. Undantaget är pigmentet i Falu rödfärg vilket innehåller små mängder bly samt även koppar och kvarts. Inandning av damm vid ned borstning av Falu rödfärg ska därför undvikas. De syntetiska organiska pigmenten framställs i huvudsak från petroleumprodukter och används till blå, gröna och klara gula, orange och röda kulörer. De ger vid framställningen upphov till de miljöproblem som är förknippade med oljeutvinning, medan de vid normal användning i färg är så komplexbundna att de inte direkt påverkar miljön. Ett vanligt rostskyddspigment är zinkfosfat. Zink används idag som alternativ till blymönja som tidigare var vanligt förekommande. Genom att ersätta tidigare blypigment med zink har man minskat den negativa miljöpåverkan betydligt. I dagsläget får färg med blymönja inte säljas för konsumentbruk, utan endast till yrkesmän för speciella applikationer. Fyllnadsmedel i färg används för att ge bättre täckförmåga, bättre filmtjocklek och påverka konsistens och glans eller hållfastheten i färgskiktet. De fyllnadsmedel som förekommer är normalt inerta material utan särskilda hälso- eller miljöeffekter. Dock kan inandning av slipdamm verka irriterande på ögon och andningsvägar och skall undvikas.
Organiska lösningsmedel är ett av de största miljöproblemen, när det gäller färger. Det vanligaste organiska lösningsmedlet är alifatnafta, som är en blandning av alifatiska kolväten. Latexfärg, som är den mest använda färgtypen, har vatten som lösningsmedel. Ibland kan det förekomma små mängder organiska lösningsmedel i latexfärg, vanligtvis någon glykol, som är tillsatt för att fungera som filmbildare eller göra den mer lättapplicerad. Inandning av organiska lösningsmedel i större mängd kan ge obehag som huvudvärk och illamående. Alifatnafta är något mindre skadlig än aromathaltig lacknafta. Alifatnafta är mer lättnedbrytbar än aromatisk lacknafta och därför mer skonsam ur miljösynpunkt. Ofta upprepad inandning av lösningsmedel kan ge bestående skador på centrala nervsystemet. Lösningsmedlen avdunstar när färgen torkar och påverkar då inomhusluften. Om färgen innehåller lösningsmedel, som avdunstar mycket långsamt, kan inomhusmiljön påverkas längre eller kortare tid efter det att färgen torkat. Det finns idag standardmetoder för att mäta avdunstning (emissioner) till inomhusmiljön. Flyktiga organiska ämnen som lösningsmedel, kan tillsammans med kväve oxider från t ex trafik och solljus medverka till bildandet av så kallad marknära ozon. Detta gäller främst organiska lösningsmedel som är olösliga i vatten, såsom lacknafta och andra kolväten. Vattenlösliga organiska lösningsmedel som t ex vissa alkoholer och glykoler i latexfärger har däremot mindre påverkan på ozonbildningen, då de lättare tvättas ur atmosfären med nederbörd. Förhöjda ozonhalter i vår närmiljö kan vara irriterande för luftvägarna samt påverka byggnads material och växtlighet negativt. Därför är det viktigt att i första hand försöka välja färger med sålåg halt av lacknafta/alifatnafta som möjligt. De organiska lösningsmedel, som i dag används i färger, utvinns huvudsakligen ur petroleumprodukter, dvs. från icke förnyelsebara råvaror såsom bergolja och naturgas. Vegetabiliskt framställda organiska lösningsmedel som t ex etanol från trädråvara utgör endast en liten del i dagsläget.
Torkmedel (sickativ) påskyndar torkförloppet hos luftoxiderande oljor. Kobolt och zirkonium är vanligast. Tidigare innehöll torkmedel ofta bly, vilket idag har ersatts med andra alternativ. Konsistensmedel, ofta förtjockningsmedel, används för att förbättra färgens arbetsegenskaper. Exempel är cellulosaprodukter och bentonitleror. Dessa ämnen är inerta och medför ingen särskilda hälso- eller miljöpåverkan. Vätmedeleller emulgatorer hjälper till att finfördela och/eller blanda ut pigment och bindemedel i färgen så att den blir homogen och stabil. Tidigare kunde användning av nonylfenoletoxilater (APEO) förekomma, dessa är svårnedbrytbara och skadliga för organismer framförallt i vattenmiljön. Idag har man ersatt dessa med andra miljömässigt bättre alternativ, t ex olika fettalkoholer. De flesta vattenburna färger (utom de starkt alkaliska) behöver en tillsats av bakteriedödande medel (konserveringsmedel) för att kunna förvaras och lagras utan att funktionen försämras. I stort sett alla utomhusfärger behöver innehålla något mögelhindrande ämne (fungicid). Eftersom konserveringsmedel och fungicider har till uppgift att förhindra växt av mikroorganismer, alger och svampar kan de också påverka hälsa och miljön negativt. Normalt förekommer dessa ämnen i halter som är lägre än de där hälso- eller miljöeffekter kan uppstå. Andra typer av tillsatsmedel används t ex för att motverka skinnbildningeller skumning. Som antiskinnmedel i oxidativt torkande färger används ämnen som är allergiframkallande på huden, dock i halter som är mycket låga. Som pH (surhets-) reglerande ämne kan ammoniak förekomma, som avdunstar vid färgens torkning och har en speciell lukt. I inomhusfärger används därför ofta andra, ej flyktiga, ämnen för pH-reglering.
Som bindemedel används ett akrylatharts (polyakrylat). Akrylhartset kan innehålla sk restmonomerer, dvs små mängder av akrylamid, akrylsyra, metakrylat, etylakrylat eller metylmetakrylat. Akrylamid kan tränga in genom huden och förorsaka skador på nervsystemet. Många akrylater kan ge allergiskt kontakteksem. Därför ska hudkontakt med den våta färgen undvikas. Många akrylater innehåller ftalater som mjukgörare. Vattenburen akrylatfärg kan innehålla glykoler eller glykoletrar. Referens = Litteratur om kemiska hälsorisker [chemfile(), file(), referens i dokument] Med akrylatfärg går det inte att få fram riktigt samma släta och fina yta som med alkydfärg. Men vid målning med akrylatfärg slipper man den fräna lukten från lösningsmedelet i alkydfärg. Det är ett par av de väsentligaste orsakerna till att akrylatfärg är den mest använda färgtypen. En annan är att penslar och redskap både snabbt och lätt tvättas rena i vatten. Och skulle man spilla, kan den våta färgfläcken lätt torkas bort med fuktig trasa. Akrylatfärg innehåller miljontals små kulor av plasten akrylat, som har blandats med vatten. När vattnet har dunstat, bildas en mjuk, tunn och lite seg yta som tål normal rengöring när färgen så småningom har härdat. Även om akrylat är en plast ska akrylatfärg inte förväxlas med plastfärg. Det är två mycket olika färger med olika egenskaper. Korrekt beteckning för plastfärg är PVA-färg (polyvinylacetat), som är billigare än akrylatfärg. Akrylatfärg ska målas rätt snabbt, för redan efter två minuter blir ytan seg. Om man drar i den med pensel blir den randig efter penselborsten. Har du glömt en liten fläck, måste du vänta tills hela ytan är torr innan du kan lägga på mer färg. Den mjuka ytan vid målning med akrylatfärg är inte lika stark som den som målats med alkydfärg. Egenskaperna gör att du kan få problem, t ex om du målar dörrar, fönsterbänkar, bord, fönster eller handledare på räcken med akrylatfärg. Ytan blir snabbt smutsig och känns klistrig efter en tid. Välj i stället en lackfärg på akrylatbas. Den är dyrare, men bildar en hårdare, starkare och jämnare yta, alltså precis som alkydfärgen. Det är lätt att arbeta med akrylatfärg och vid användning av vattenburen akrylatfärg försvinner lukten snabbt. Men färgen har sina begränsningar, och du bör undvika att använda den på föremål som utsätts för hårt slitage och på två föremål som ligger an mot varandra. Den är ett utmärkt val på och i garderober, på räcken, socklar och paneler. Referens = Tidskriften Gör Det Själv [chemfile(), file(), referens i dokument]
Akrylatfärger innehåller någon form av akrylat som bindemedel. Det kan vara polyakrylat, multifunktionella akrylater, tri- eller difunktionella akrylater samt monomera akrylatföreningar. Akrylatfärgerna kan indelas bl a i - elektronstråle-härdande lack - UV-härdande lackfärg - värmehärdande lacker - latexfärger De används bl a inom tryckeri- och möbel-industrin. Latexfärger har egen rubrik och behandlas ej här. Dessa är icke-härdande och stelnar istället genom att lösnings-medlet avdunstar.
UV-härdande akrylatfärger består bl a av bindemedel, reaktivt spädmedel och fotoinitiator. Elektronhärdande akrylatfärger består bl a av bindemedel och reaktivt spädmedel. UV-härdande tryckfärg kan bestå av reaktiva akrylat-föreningar (50-70%), fotoinitiator (5-20%), pigment (10-30%) samt andra tillsatsmedel t ex inhibitorer, tensider och vaxer. Exempel på ingående ämnen i akrylatfärger, härdande - Acceleratorer - Peroxider - Bindemedel akrylater (prepolymera) med mer än 10 viktsprocent akrylatmonomerer - Epoxiakrylater - Inerta icke reaktiva polymerer - Melamin-formaldehydhartser - Monofunktionella akrylater - Multifunktionella akrylater - Polyesterakrylater Fotoinitiatorer - Acetofenonderivat - a-akryloximestrar - Bensilketaler - Bensofenon - Bensoinetrar - Bensil - Balogensubstituerade alkylketoner - Halogensubstituerade arylketoner - Kinonderivat - 2-klorotioxanton - Michlers keton (synonym 4,4'-bis(dimetylamino)bensofenon) - Tioxanton Fotosynergister - Alifatiska aminer - N-metyl-dietanolamin - Trietanolamin - Aromatiska aminer - n-butoxi-etyl-4-dimetylaminobensoat - 4,4'-dietylaminobensofenon - etyl-4-dimetylaminobensoat Fyllmedel - Kalciumkarbonat Inhibitorer (15 - 400 ppm) - Enoler - Hydrokinon - Hydrokinonderivat - 2,5-di-tert-butylhydrokinon - p-metoxifenol - Mono-tert-butylhydrokinon - Toluhydrokinon Färgämnen / Pigment Katalysatorer - Metalljoner Lösningsmedel Reaktiva spädmedel - Multifunktionella akrylatestrar - Monofunktionella akrylatestrar Tensider Vaxer Övriga ämnen - Aminer
UV-härdande akrylatfärger innehåller kraftigt allergiframkallande ämnen. På vissa tryckerier där denna typ av färg använts har det inträffat att hälften av arbetarna fått allergiska eksem. Riskerna för allergiska reaktioner är störst vid hantering av ohärdade produkter eftersom halterna av de allergiframkallande substanserna är höga. Efter härdning kan det finnas tillräckligt med oreagerad utgångssubstans kvar för att detta ska kunna medföra risker. Följande akrylatföreningar har i tester visats vara starka allergen - bis-EMA (synonym 2,2-bis(4-(2-metakryl- - oxietoxi)-fenyl)-propan) - bis-MA (synonym 2,2-bis(4-metakryl- - oxifenyl)-propan) - BUDA (synonym 1,4-butandioldiakrylat) - epoxiakrylat - HDDA (synonym hexandioldiakrylat) - NPGDA (synonym neopentylglykoldiakrylat) - TMPTA (synonym trimetylolpropantriakrylat) - TPGDA (synonym tripropylenglykoldiakrylat) Svaga kontaktallergen från tester är bl a - bis-GMA, linjär (synonym 2,2-bis(4-(2- - hydroxi-3-metakryloxipropoxi)- - fenyl)-propan) - bis-PMA (synonym 2,2-bis(4-(3-metakryl- - oxipropoxi)-fenyl)-propan) - etylenglykoldiakrylater - metakrylater - multifunktionella metakrylatföreningar - NPGDMA (synonym neopentylglykoldi-metakrylat) - uretanmetakrylater Vissa akrylatföreningar är cancerframkallande. Akrylamid och akrylnitril är klassificerade som cancerframkallande. Etylakrylat är klassificerat som cancerframkallande av IARC. Ytterligare hälsorisker kan tillkomma från olika tillsatsmedel.
Tillsatsmedel kan bidra till att ge produkten större miljöbelastande egenskaper t ex olika fenoler.
Lösningsmedelsburen alkydfärg luktar starkt och avger hälsoskadliga ångor. Alkydfärg torkar genom oxidation av ingående omättade fettsyror i bindemedlet alkyd, en reaktion som kan påskyndas genom tillsats av ett sickativ (torkande ämne). Alkydfärg är rätt trögflytande, men vid målning flyter den ut bättre än akrylatfärg. Det luktar fränt under målning med alkydfärg (och något dygn efteråt). Alkydfärg består primärt av olja och bindemedel av typ alkyd, som är ett syntetiskt hartslim gjort av råolja. Alkyden och oljan (och alla färgpartiklar) har blandats med lacknafta till färg. När färgen har strukits ut på en yta dunstar lacknaftan och alkyden suger till sig syre. Resultatet är en tjock, spröd men ändå slitstark yta. Denna process är orsaken till alkydfärgens fördelar och nackdelar. Att färgen härdar långsamt innebär att man har lång tid på dig att stryka ut den. Efter 20 minuter är den så klistrig att den inte längre kan bearbetas. Den långsamma processen gör också att färgen själv flyter ut och ger en slät yta. Den största nackdelen med lösningsmedelsburen alkydfärg är inandning av ångor, från lösningsmedlet, som har orsakat stora problem för målare. Lacknafta avdunstar rätt snabbt och det innebär att under målning avges stora mängder ångor från lösningsmedlet. Om man vill slippa lacknafta, och ändå dra nytta av alkydfärgens fördelar, ska man välja en vattenspädbar alkydfärg. En sådan färgtyp kallas oljeemulsion eller bara emulsionsfärg. Färgen kan bearbetas i upp till sju minuter, så ytan blir ganska slät, men inte lika stark som den vid målning med alkydfärg. Den starka ytan är ett viktigt argument för att välja alkydfärg på ytor som ska tåla slitage, t ex fönsterbänkar, trappräcken, bord, foderlister och andra ställen där det krävs slitstarka ytor. Referens = Tidskriften Gör Det Själv [chemfile(), file(), referens i dokument] Bindemedlet alkydharts har inga kända hälsorisker. Koboltföreningar brukar tillsättas för att påskynda torkningen. Kobolt ger allergiskt kontakteksem. Referens = Litteratur om kemiska hälsorisker [chemfile(), file(), referens i dokument]
Alkydoljefärg kräver mer lösningsmedel än linoljefärg. Färgen kan också göras vattenburen genom att alkydoljebindemedlet emulgeras eller löses i vatten. Tekniska egenskaper Finns både som lösningsmedelsburen (alifatnafta) och vattenburen. Torkar långsammare än latexfärg men snabbare än linoljefärg. Har god inträngning i underlaget och hög vattentålighet. Ger bra skydd som grundfärg för trä utomhus. Kritningstendensen är lägre än för linoljefärg men högre än för akrylatfärg. Alkalibeständigheten är låg, varför speciellt alkalibeständig färg behövs på förzinkade ytor. Arbetsmiljö Inomhus är det organiska lösningsmedlet en belastning för arbetsmiljön. Lackfärg av alkydoljefärgstyp används numera sällan inomhus. De oxidationsprodukter som avges vid torkningen kan verka irriterande på ögon och andningsvägarna. färgstyp används numera sällan inomhus. De oxidationsprodukter som avges vid torkningen kan verka irriterande på ögon och andningsvägarna.
Epoxifärger finns lösta i lösningsmedel eller emulgerat i vatten. Epoxifärger utmärks av mycket hög slitstyrka och vatten/kemikalieresistens. Epoxifärg används främst på betonggolv i utsatta miljöer. Det är viktigt att underlaget som skall målas är torrt och inte utsatt för fukt underifrån. Epoxifärg bör inte användas utomhus eftersom den kritar snabbt och kraftigt. Referens = Beckers Färg [chemfile(), file(), referens i dokument]
Epoxi Hälsorisker Epoxi är hudirriterande och allergiframkallande. De som arbetar med ej uthärdade epoxiprodukter riskerar att få hudallergi. Olika typer av epoxiprodukter har olika förmåga att framkalla allergi. Flytande epoxiharts är mycket hudallergiframkallande. Även härdarna kan vara allergiframkallande. Speciellt farlig är härdare av typ anhydrider som kan ge luftvägsallergier. Det finns risk att bli allergisk mot epoxi redan första gången man kommer i kontakt med det. Det är också möjligt att klara att arbeta med epoxi under lång tid och sedan plötsligt blir allergisk. Den som ska arbeta med epoxi ska läkarundersökas innan arbetet påbörjas. Personer med allergiska hudproblem får inte arbeta med epoxi. För den som ska arbeta med eller arbetar med härdare av typ anhydrider gäller dessutom särskilda krav på läkarundersökning. Läs i föreskrifterna om härdplaster AFS 2005:18. Den som en gång blivit allergisk mot epoxi får omedelbart allergiska eksem vid kontakt med mycket små mängder av epoxi. Epoxiplast Epoxiplast bildas genom en kemisk reaktion (härdning) mellan ett epoxiharts och en härdare. Som härdare används bl a aminer såsom dietylentriamin, dipropylentriamin och trietylentetramin. I många epoximaterial, särskilt lim, ingår också något lösningsmedel såsom metyletylketon, aceton, toluen eller xylen. Arbete med epoxi är en vanlig orsak till allergiskt kontakteksem. Allergin uppstår i regel inom några veckor eller månader, i enstaka fall först efter flera år. Eksemet yttrar sig som klåda, rodnad, millimeterstora knottror och eventuella blåsor. I regel är eksemt lokaliserat till händer och underarmar. Den som fått eksem kan inte fortsätta arbeta med epoxi. Allergiskt kontakteksem kan också framkallas av härdaren. Lösningsmedlet kan ge upphov till hudirritation och kontakteksem. Epoxiplast som härdats vid rumstemperatur innehåller 5-20% allergiframkallande monomerer, som vid t ex slipning kan ge upphov till allergiframkallande damm. Monomerer är epoxi som inte reagerat med härdaren. Referens = Litteratur om kemiska hälsorisker [chemfile(), file(), referens i dokument]
Uretanfärg används främst inom måleriet vid golvmålning på mycket hårt utsatta ytor. Det är viktigt att ytor som ska målas är torra och inte utsatta för underifrån kommande fukt. Eftersom uretanfärg innehåller isocyanater måste Arbetsmiljöverkets föreskrifter om härdplaster tillämpas. Det innebär bl a att den som ska måla med uretanfärg måste ha genomgått utbildning om härdplaster. Referens = Beckers Färg [chemfile(), file(), referens i dokument]
Kalkfärg används på putsade fasader och andra liknande ytor på byggnader både inomhus och utomhus. Färgen hårdnar genom att luftens koldioxid omvandlar kalken till kalciumkarbonat (kalksten). Utan tillsatts av pigment är kalkfärgen vit, men olika kulörta pigment kan tillsättas för att få fram andra färger. Den vita färgen beror på den ingående kalciumhydroxiden och det bidrar också till färgens bindande egenskaper. Proportionerna mellan vatten och kalk är 80-85% vatten och 15-20% kalk. Tekniska egenskaper Kräver yrkeskunnande vid applicering. Används huvudsakligen utomhus (ej på ytor som målats med annan färgtyp). Arbetsmiljö Starkt alkalisk. Risk för ögon- och hudskador vid oförsiktig användning. Är etsande på glas.
Latexfärg är den mest använda färgtypen vid inomhusmålning, men det finns även många latexfärger för utomhusbruk. Tekniska egenskaper Vattenburen, lättmålad, snabbtorkande och hållbar, men ej lämplig på lösa och kritande ytor. Våtrumsfärg skall uppfylla speciella kvalitetsnormer enligt Måleribranschens Våtrumskontroll. Akrylatfärg har mycket god väderbeständighet men bör inte användas direkt på ogrundat trä. Den rekommenderas oftast inte till snickerier och andra trädetaljer utomhus, som behöver extra bra skydd mot vatten. På mycket hållfast puts kan akrylatfärg användas. På betong bör akrylatfärg användas för att ge karbonatiseringsskydd, så att armeringsjärnen inte börjar rosta och spränger betongen. Arbetsmiljö Viss lukt, som inomhus kan verka något irriterande, speciellt om organiska lösningsmedel ingår. Detta varierar mellan de olika färgtyperna.
Tekniska egenskaper Vattenburen. Jämfört med latexfärg är limfärg mer svårarbetad. Den kan färga av sig vid beröring och är mer smutskänslig. Vid ommålning kan krävas nedtvättning av tidigare färglager. Arbetsmiljö Inga speciella problem, förutom att nedtvättning av gammal limfärg är ett krävande arbete.
Tekniska egenskaper Färgen har mycket god inträngning i underlaget. Den torkar långsamt � detta måste speciellt beaktas när den används som grundfärg. Den har även god vattenbeständighet. Den har bra hållbarhet även som täckfärg, men inte helt i nivå med alkydoljefärg. Ej alkalibeständig. Arbetsmiljö Organiska lösningsmedel (alifatnafta) är en belastning vid arbeten inomhus. Oxidationsprodukter, som avges till luften vid torkning, kan verka irriterande på ögon och andningsvägar.
Med hjälp av emulgeringsmedel tillverkas vattenspädda linolje- och alkydoljeprodukter, som fungerar även för utomhusbruk. Högre fuktkänslighet, sämre slitstyrka och inträngning kan vara problem jämfört med lösningsmedelsburen färg, men ofta målas dessa färger i system där man grundar med penetrerande olja och grundfärg. Färger av den här typen är generellt miljöanpassade men man bör se upp med tillsatser. Äggallergi förekommer, terpentin är allergiframkallande och syntetiska emulgeringsmedel kan vara miljöstörande. Referens = Publikation från Sveriges Byggindustrier [chemfile(), file(), referens i dokument] Alkydoljefärg baseras på kemiskt modifierad olja (t ex tallolja, sojaolja eller linolja). Den torkar genom att det organiska lösningsmedlet (eller vattnet) avdunstar och oljedelen oxideras av luftens syre. Alkydoljefärg kräver mer lösningsmedel än linoljefärg. Färgen kan också göras vattenburen genom att alkydoljebindemedlet emulgeras eller löses i vatten. Referens = Sveriges Färgfabrikanters Förening (Sveff) [chemfile(), file(), referens i dokument]Bindemedlet är linolja, talloljeester eller annan olja som emulgeras i vatten ibland med hjälp av kasein (kaseintempera). Färgtypen används huvudsakligen som väggfärg. I äggoljetempera emulgeras bindemedlet i vatten med hjälp av ägg. Äggoljetempera rekommenderas av tradition till snickerier inomhus (träpaneler, möbler etc). Under senare år har färgen använts på väggytor, vilket avråds från av hälsoskäl och tekniska skäl. Tekniska egenskaper Torkar långsamt. Speciellt äggoljetempera kan blankas genom polering eller nötning. Arbetsmiljö Oxidationsprodukter, som avges till luften vid torkning, kan verka irriterande vid inandning. Referens = Toxinfohandbok [chemfile(), file(), referens i dokument]
Vinylacetat verkar irriterande på hud, ögon och andningsvägar. I kroppen sönderdelas vinylacetat till ättiksyra och acetaldehyd. Både vinylacetat och acetaldehyd är misstänkt cancerogena, men några säkra belägg för detta finns inte för närvarande.
Tekniska egenskaper Färgen är något svårare att applicera än latexfärg. Skiktet har hög fuktgenomsläpplighet. Latexbindemedel ingår för att ge bra strykbarhet. Arbetsmiljö Alkalisk, kan skada ögon och hud vid oförsiktig användning. Är etsande på glas.
Tekniska egenskaper Ger en vattenavvisande färgyta som gör att fukten inte tränger in i underlaget vilket är en betydelsefull egenskap vid målning av puts och lättbetong. Samtidigt har färgskiktet stor diffusionsöppenhet som tillåter inifrån kommande vattenånga att passera. Färgen hindrar inte karbonatisering av putser. Dvs putsen hårdnar genom att luftens koldioxid omvandlar kalken till kalciumkarbonat (kalksten). Silikonhartsfärg är applicerbar på mineraliska underlag, tidigare målade med organiska och oorganiska färger. Arbetsmiljö Används huvudsakligen utomhus.
Falu Rödfärgspigmentet, som framställs ur mineralrester från brytningen av kopparmalm, har en mycket komplex sammansättning med silikater och järnoxid som viktigaste beståndsdelar. Tekniska egenskaper Rekommenderas endast till ohyvlat obehandlat eller tidigare slamfärgsmålat trä. God hållbarhet på vertikala ytor. Fuktgenomsläpplig färg med matt yta, som så småningom färgar av sig vid beröring. Torkar snabbt. Förhindrar ej träsprickor. Arbetsmiljö Beroende på innehåll av bly, koppar och kvarts i Falu Rödfärg skall andningsskydd användas vid nedborstning av denna färg före ommålning.
Tekniska egenskaper Färgen har god kemisk beständighet och lämpar sig väl för metaller som zink, koppar och aluminium. Den har god vidhäftning även på olika kemiska ytbehandlingar. Lösningsmedelshalten är relativt hög. Färger för puts av denna typ förekommer, men andra färger utan lösningsmedel bör hellre användas av miljöskäl. Arbetsmiljö Eftersom produkten normalt används utomhus finns det inga speciella arbetsmiljöproblem.
Tekniska egenskaper Det finns tre typer av träolja. Lösningsmedelsfri (som alltså innehåller 100% olja) och vattenburen där oljan är emulgerad i vatten. Det finns också Lösningsmedelsburen med ca 55% lacknafta eller mer. Ingår lacknafta bör man i första hand välja en aromatfri variant. Oljan tränger in i träytan och härdar långsamt genom oxidation med luftens syre. Arbetsmiljö Organiska lösningsmedel, där det ingår, belastar arbetsmiljön vid arbeten inomhus, liksom oxidationsprodukter, som bildas vid oljans torkning. Oljeindränkta trasor kan självantända och skall hanteras med försiktigt (vattenindränkas).
Fyllnadsmedel är dolomit- och kalkstensmjöl. Tidigare användes ofta finkornig sand (sandspackel). Till golv används cementbaserat spackel, ofta sk flytspackel. Vid industriell träbehandling kan andra typer av spackel användas. Tekniska egenskaper Målerispackel är normalt fria från organiska lösningsmedel. Spackel till väggar och tak baserad enbart på cellulosalim förekommer också i speciella fall. Dessa har fördelen att bindemedlet är förnyelsebart, däremot blir nackdelen att vattenbeständigheten är sämre. Arbetsmiljö I många vägg- och takspackel ingår luftfyllda mikrosfärer som fyllmedel. Dessa ger många för delar, spacklet blir lättare att bära och applicera, det blir mer lättslipat samt fyller bättre utan att spricka. Mikrosfärer kan framställas av plast, keramiska material, mineralet perlit eller förgasad kolaska. Vid slipning kan dessa ge upphov till slipdamm som irriterar ögonen och andningsvägarna samt kräver ögonskydd och vid behov andningsskydd.
[chemfile(), nC=0 nr=oljor-v, f1=/produkt/info/html/oljor-v.htm] Skärvätskor Skärvätskor används vid metallbearbetning för att kyla och smörja samt för att transportera bort spån. Typer av skärvätskor - Skäroljor - Skäremulsioner - Syntetiska skärvätskor Skäroljor Skäroljor består oftast av mineralolja, men kan även bestå av vegetabilisk olja. De kan inte blandas med vatten. Skäremulsioner Framställs genom att till oljan tillsätta en emulgator, dvs ett ämne som gör att oljan kan blandas med vatten. I emulsionen hålls små droppar av olja svävande i vatten. Syntetiska skärvätsjor Innehåller inte mineralolja, utan består av kemiska ämnen som är lösta eller emulgerade i vatten. Tillsatsmedel I skäremulsioner uppstår lätt tillväxt av bakterier eller svamp. De framkallar en obehaglig doft och försämrar vätskans tekniska egenskaper. Det är vanligt att istället för att byta vätska att tillsätta en baktericid eller fungicid, dvs ett bakterie- eller svampbekämpande ämne. Baktericid är ett bekämpningsmedel mot bakterier. Fungicid är ett bekämpningsmedel mot svampar. Skärvätskor kan också innehålla många andra slags tillsatsmedel, t ex formaldehyd, nitriter och aminer. Hälsorisker Kontakteksem framkallas ofta av skäremulsioner, mera sällan av skäroljor. Eksemenen drabbar främst händer och underarmar. I regel är eksemen icke-allergiskt, dvs det beror på irritation och uttorkning av huden. Vissa av ämnena som tillsätts skäremulsioner kan framkalla allergiskt kontakteksem, t ex konserveringsmedel som etylendiamin, formaldehyd och formaldehydavgivare. Formaldehydavgivare är ett ämne som reagerar med bakterier i skärvätskan och det bildas formaldehyd, som fungerar som bakteriebekämpande medel. Vid arbete med hårdmetall och en del nickellegeringar kan allergiframkallande metaller (kobolt, krom eller nickel) lösas ur arbetsstycket och ge upphov till allergiskt kontakteksem. Oljeakne förekommer främst hos de som arbetar med skäroljor, mera sällan hos de som arbetar med skäremulsioner. De brukar vara lokaliserade till de ställen där oljeindränkta kläder skaver mot huden. Vid skärande bearbetning med mineraloljor och om det uppstår kraftig uppvärmning finns risk för att det bildas polyaromatiska kolväten (PAH), av vilka många är cancerframkallande. I skäroljor, skäremulsioner och syntetiska skärvätskor kan det förekomma att nitriter och aminer förekommer samtidtigt (t ex trietanolamin och natriumnitrit). Då kan cancerframkallande nitrosaminer bildas genom en kemisk reaktion i vätskan. Vattenblandbara skärvätskor innehåller ofta trietanolamin. Inandning av olja i form av ånga, rök eller dimma ger upphov till irritation på luftvägarna. Oljedroppar som är mindre än 0,005 mm tränger ända ner till lungans finaste förgreningar, lungblåsorna. Vid höga halter kan det uppstå en form av lunginflammation (oljelunga). Referens = Arbetsmiljö från A till Ö [chemfile(), file(), referens i dokument]
[chemfile(), nC=0 nr=oljor, f1=/produkt/info/html/oljor.htm]
Smörjmedel är en produktgrupp med olika användningsområden. T ex har hydraulvätskor den huvudsakliga uppgiften att överföra kraft. Som smörjmedel kan också räknas bl t motoroljor, turbinoljor, cirkulationsoljor, formoljor och smörjfetter. Gemensamt för smörjmedel är att de innehåller en basolja med tillsats av mindre mängder av olika additiv vilka ger smörjmedlet eftersträvade tekniska egenskaper. Smörjmedel kan dock oavsiktligt spridas till miljön. Därför finns det i två svenska standarder särskilda miljökrav på hydrauloljor (SS 15 54 34) och smörjfetter (SS 15 54 70). Referens = Referens = SP, Sveriges Tekniska Forskningsinstitut, Borås [chemfile(), file(), referens i dokument]
Petroleumprodukter som framställs ur råolja Råolja är en tunnflytande mörk vätska som naturligt förekommer i delar av berggrunden. Denna vätska är en blandning av hundratals olika kolväten. Petroleumprodukter från råolja har en rad användningsområden däribland som bränsle för motordrivna fordon, i form av bensin. Den process råoljan behöver gå igenom för att kunna delas upp den i gasol, bensin, flygbränsle, diesel- och villaolja, tunga eldningsoljor, asfalt (bitumen) kallas raffinering och sker i ett raffinaderi. Principen för ett raffinaderi är att ta vara på den speciella egenskap att varje kolväte innehar en viss kokpunkt. Tack vare denna egenskap hos kolvätena kan råoljan separeras med hjälp av temperaturskiftningar i olika produkter. De lättaste ämnena går ut ur ledningar som är belägna högst upp på fraktioneringskolonnen, först gasol, därefter bensin osv. Med en process som kallas termisk krackning går det att av de tyngre råoljeprodukterna skapa andra produkter t ex bensin. Termisk krackning går ut på att bryta ner de långa kolväte-molekylerna till kortare och därmed skapa en mer lättflytande olja som möjliggör större bensinutvinning. Krackning är ett samlingsnamn för en rad olika processer som möjliggör mer varierad eller önskad oljeproduktion.
En schematisk bild av destillationsprocessen. 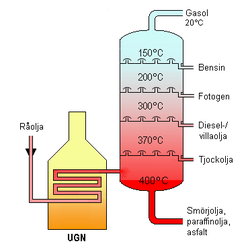
Gasfraktionen Gasfraktionen kallas den fraktion som vid 20 °C är gasformig och består till största delen av metan (>75%), etan (6-10%), propan och butan (5-8%). Gasen tas ofta direkt vid borrning men betydande kvantiteter erhålls även vid destillation. Gasfraktion används ofta till bränsle och kallas då naturgas eller gasol. Råbensin Råbensinen eller nafta kallas den näst mest lättkokade fraktionen i petroleum och den består till största del av kolväten med mellan 5 till 12 kolatomer. Råbensinen brukar innehålla en hel del svavel och måste genomgå ytterligare rening innan den kan användas. Efter ytterligare destillation kan råbensin delas upp i petroleumeter, lättbensin som används som lösningsmedel och bensin som används som motorbränsle. Råfotogen Liksom råbensin måste råfotogen renas från svavelföreningar och destilleras ytterligare. Ur denna fraktion framställs bland annat flygbränsle, fotogen och lösningsmedel som lacknafta och thinner. Brännoljor Ur denna fraktion framställs bland annat dieselolja och brännolja. En hel del destillat av denna fraktion behandlas i en process som kallas krackning där kolvätena bryts ner till mindre kolväten. Smörjoljor Denna fraktion används bland annat till framställning av smörjoljor som till exempel motoroljor och paraffinoljor. Destillat som är i fast form vid rumstemperatur kan användas till att framställa smörjfetter, vaxer, paraffin och vaselin (petrolatum). Liksom med brännoljorna används mycket av denna fraktion till krackning. Destillationrest Destillationresten är den tjockflytande olja som blivit kvar efter destillationen. De mer lättflytande delarna av denna fraktion används som brännolja, de delar som är i fast form kan blandas med grus (singel) till asfalt och användas som vägbeläggning. Övriga petroleumprodukter Alkener och alkyner som erhålls från krackningen kan bland annat användas till framställning av plaster, eten kan bland annat omvandlas till polyetenplast eller etanol, propen används bland annat till tillverkning av polypropen och propanol. Petroleum kan även vara rikt på aromatiska föreningar exempelvis bensen och toluen, och dessa tas till vara och används som utgångsämnen i kemisk industri.
Petroleum, även kallat mineralolja, bergolja, råolja och ibland nafta, är en tunnflytande mörk vätska som naturligt förekommer i delar av berggrunden och är en blandning av hundratals olika kolväten. Petroleum har en rad användningsområden och genom fraktionerad destillation kan råoljan separeras i olika produkter, t ex som smörjoljor och smörjfetter. Principen för ett raffinaderi är att ta vara på den speciella egenskap att varje kolväte innehar en viss kokpunkt. De lättaste ämnena går ut ur ledningar som är belägna högst upp på fraktioneringskolonnen, först gasol, därefter bensin osv
Både mineraloljor och syntetiska oljor görs av råolja som utvinns ur berggrunden. Skillnaden är att de syntetiska oljorna tillverkas med mer avancerade förädlingsprocesser och att de är renare och högklassigare än de konventionella mineraloljorna. Genom att avlägsna flera föroreningar ur råoljan, blir det också möjligt att skräddarsy enskilda molekyler för att uppfylla olika motorers behov. Referens = Litteratur om teknisk kemi [chemfile(), file(), referens i dokument] Ett syntetiskt smörjmedel innehåller fler förädlade basämnen än de konventionella mineraloljorna. Både konventionella mineraloljorna och syntetiska oljor görs av råolja som utvinns ur berggrunden. Skillnaden är att de syntetiska oljorna tillverkas med mer avancerade förädlingsprocesser och att de är renare och högklassigare än de konventionella mineraloljorna. De konventionella mineraloljorna har fler orenheter, såsom svavel, reaktiva och instabila kolväten samt andra oönskade orenligheter som inte helt kan avlägsnas i konventionell förädling. Referens = ExxonMobil Sverige AB [chemfile(), file(), referens i dokument]
Vegetabiliska oljor, t ex rapsolja, tallolja och linolja, framställs ur olika växtdelar. Linolja och tallolja kan självantända t ex i kontakt med sågspån eller trassel, eller då oljan är indränkt i en trasa. Referens = Arbetsmiljö från A till Ö [chemfile(), file(), referens i dokument]
Flerfassystemet ger produkten en lämplig konsistens så att den stannar kvar där den ska vara. Detta säkerställer en effektiv smörjning och tätning samtidigt som de aktiva ämnen i additiven förs fram till de rörliga ytorna i maskinerna. Under drift utsätts fettet för betydande skjuvningskrafter, förvandlas till en flytande vätska som ger den smörjning som krävs, och sedan återgår till den ursprungliga fasta konsistensen när skjuvningen upphör. Referens = Lubentum, Upplands Väsby [chemfile(), file(), referens i dokument] ASTM, American Society forTesting and Materials, har definierat smörjfett som en fast till halvflytande produkt bestående av ett förtjockningsmedel i ett flytande smörjmedel där även andra ingredienser med speciella egenskaper kan inkluderas. Ett annat, enklare sätt att beskriva smörjfett är att likna det vid en tvättsvamp. Förtjockningsmedlet är svampen och basoljan är vattnet. Förtjockningsmedlet i fettet har till funktion att skapa en matris som håller basoljan på plats i en solid struktur och ger fettet dess konsistens. När fettet utsätts för olika driftsförhållanden som temperatur, belastning eller skjuvning, så skapas ett viskoelastiskt flöde i smörjfettet. Hårdheten hos fettet, dess konsistens, brukar anges med ett nummer enligt NLGI-systemet. Från halvflytande (00) till fast (2) är mest förekommande. Referens = Circle K (Statoil) [chemfile(), file(), referens i dokument]
Oljetypen kan vara mineralolja, syntetisk olja eller vegetabilisk olja. Syntetiska basoljor har de bästa låg- och högtemperaturegenskaperna Referens = Circle K (Statoil) [chemfile(), file(), referens i dokument]
Fetter klassificeras beroende på vilket typ av förtjockningsmedel som använts för att ge struktur och konsistens. Fett baserade på förtjockningsmedel av typ metalltvålar är mest förekommande, men andra typer av förtjockningsmedel förekommer. Referens = Lubentum, Upplands Väsby [chemfile(), file(), referens i dokument] De vanligaste typerna av smörjfett har tvål av litium (Li) som förtjockningsmedel. Referens = Circle K (Statoil) [chemfile(), file(), referens i dokument] Kalciumfetter Smörjfetter med förtjockare av typ kalciumfett används för mindre krävande applikationer. Smältpunkten för kalciumbaserade fetter är omkring 100 °C. Kalciumfett tillverkas med en liten vattenrest som stabiliserar tvålkomponenten och på detta sätt ger förtjockaren den önskade strukturen. Under vissa driftsförhållanden då temperaturen konstant ligger över 50°C, kan vattnet förångas så att hela fettstrukturen förstörs och det övergår i flytande form. Konventionella kalciumfetter har goda vidhäftande egenskaper och är extremt vattentåliga. Natriumfetter Natriumbaserade tvålar, liknande de tvålar som används för tvätt och hygien, har en högre smältpunkt än kalciumtvålarna. Natriumfett fungerar upp till temperaturer kring 110 °C. Nackdelarna är att de är vattenlösliga precis som tvättvålar och de har en tendens att hårdna vid lagring. Dessutom (beroende på den stora fiberstorleken hos traditionella natriumtvålar) bidrar de knappast till själva smörjförmågan hos fettet. Aluminiumfetter Aluminiumbaserat fett utvecklades samtidigt som natriumfett när teknikerna strävade efter bättre smörjning av ångmaskinerna. Förtjockningsmedel baserade på aluminium och speciellt på aluminiumstearat erbjöd ett fett med god vattenresistens och som klarade höga temperaturer. Aluminiumbaserade fetter har en väsentlig svaghet i och med att de är extremt skjuvningskänsliga. De bryts lätt ner mekaniskt och förlorar både konsistens och smörjförmåga. Smörjfett på aluminiumstearatbas används fortfarande enkla glidlager där skjuvningen är låg och i smörjning av chassis, men har generellt blivit ersatta av modernare produkter. Litiumfetter Tidigare tillverkades litiumfett av ren stearinsyra,. Nu är nästan alla litiumfetter baserade på ett speciellt ricinoljederivat, 12-hydroxy-stearinsyra (i enlighet med Clarence Earles patent). Litiumfett har god mekanisk stabilitet, en god vattenresistens samt en relativt god förmåga att tåla höga temperaturer upp till 120 °C. Litiumfett är den vanligaste typen av smörjfett, för smörjning av rullningslager och allmän smörjning. Vattenfria kalciumfetter En senare utveckling av kalciumfett är den som inte alls är vattenstabiliserad. Den klarar en maximal kontinuerlig driftstemperatur upp till 110°C, samma som både natrium och litiumfett. Utöver fördelen med temperaturen erbjuder dessa vattenfria kalciumfett samma fördelar som traditionella kalciumfetter, en utomordentlig adhesionsförmåga vid låga temperaturer och resistens mot vatten. De vattenfria kalciumförtjockarna baseras normalt på 12- hydroxy-stearinsyra, som i litiumfett och motsvarande fettyper uppvisar en utmärkt mekanisk stabilitet. Dessa används ofta för appliceringar inom den marina sektorn, inom jord- och skogsbruk samt för entreprenadmaskiner. Litiumkalciumfetter Komplexfett som används i vissa specialappliceringar. Aluminiumkomplexfetter Har en droppunkt över 240°C och är mycket vattenresistenta samt smörjer bra vid höga temperaturer. Dessutom krävs små mängder av förtjockaren för att erhålla den önskade fettkonsistensen vilket ger en utmärkt pumpbarhet. Denna kombination av egenskaper har t ex inneburit att aluminiumkomplexfett blivit populärt som smörjmedel inom stålindustrin. Nackdelarna är att de hårdnar under skjuvning och att de inte är lika mekaniskt stabila som litiumfett. I dessa hänseenden är de likvärdiga med konventionella aluminiumstearatbaserade fetter. Kalciumkomplexfetter Utvecklades samtidigt som aluminiumkomplexfett och jämfört med dessa har de en bättre lastupptagningsförmåga och klarar högre tryck. Högtemperaturegenskaperna ligger i paritet med aluminiumkomplexfett, med en droppunkt över 250°C. Den extrema trycktålighet är ett resultat av komponenter inbyggda i tvålstrukturen. Kalciumacetat, kalciumsulfonat och motsvarande kalciumderivater kan samkristalliseras in i förtjockarens struktur. I direkt motsats till aluminiumkomplexfett krävs en mycket hög tvålhalt för önskad konsistens, vilket i sin tur försämrar pumpbarheten. Kalciumkomplexfett har också en tendens att hårdna vid lagring. Litiumkomplexfetter Har droppunkter på över 300°C och dessa fetter kan klara temperaturtoppar på upp till 240°C. Denna egenskap att utstå höga temperaturer beror på en hög smältpunkt i kombination med tvålens mycket tjocka fiberstruktur. Lera Med lera som förtjockningsmedel erhålls ett fett som varken smälter eller mjuknar vid höga temperaturer. Avsaknad av en fibrös struktur begränsar emellertid stabiliteten hos lerbaserade fett. Vidare kan basoljan vid förhöjd temperatur utsättas för skadeverkningar pga oxidation. Oxidation och en kraftig läckage av olja från fettet kan dessutom resultera i att lera fälls ut och fungerar som ett slipmedel på lagerytorna. Trots detta används leror som förtjockare av högviskösa basvätskor som asfalt för tillverkning av t ex smörjmedel för öppna kugghjul. Grafit Fett baserade på grafit används nästan uteslutande i appliceringar där extremt höga temperaturer förekommer. Grafiten fungerar som själva smörjmedlet och vätskan är här enbart en bärare som bryts ned eller avdunstar under drift. De mest använda vätskorna är polyglykoler. Lagringsstabiliteten är dålig eftersom materialet har en tendens att hårdna. Typiska appliceringar är ugnslager och andra processutrustningar i stålverk. Perfluoropolyetrar (PTFE) Inerta basvätskor såsom perfluoropolyetrar (PTFE) används som smörjmedel i aggressiva miljöer och kräver en PTFE förtjockare som är lika inert. Bland appliceringar finns sådana där det förekommer aggressiva lösningsmedel samt starka syror och baser. Sådant fett används också för smörjning av pumpar för syre där kontakt med andra sorters fett skulle kunna innebära risk för brand eller explosion. Komponenter av känsligt reaktionsbenäget plast, gummi eller keramer kan också smörjas med denna typ av fluorinerat fett. Referens = Lubentum, Upplands Väsby [chemfile(), file(), referens i dokument]
Några vanliga additiv och deras funktion
Referens = Circle K (Statoil) [chemfile(), file(), referens i dokument]
Inandning av olja i form av ånga, rök eller dimma ger upphov till irritation på luftvägarna. Oljedroppar som är mindre än 0,005 mm tränger ända ner till lungans finaste förgreningar, lungblåsorna. Vid höga halter kan det uppstå en form av lunginflammation (oljelunga). Vid långvarig eller ofta upprepad hudkontakt med oljor finns risk för kontakteksem, som drabbar främst händer och underarmar. Långvarig eller ofta upprepad hudkontakt med oljor kan också ge upphov till oljeakne och de brukar vara lokaliserade till de ställen där oljeindränkta kläder skaver mot huden. Smörjoljor innehåller dessutom ofta olika tillsatsmedel. För att bedöma hälsoriskerna krävs noggrann information om tillsatsmedlen. Oljedimma bildas genom att olja finfördelas t ex av utströmmande tryckluft eller roterande maskindelar. När det finns oljedimma i en lokal, lägger den sig på huden. I mineraloljor som utsatts för höga temperaturer kan det ha bildats polyaromatiska kolväten (PAH), av vilka många är cancerframkallande. Referens = Arbetsmiljö från A till Ö [chemfile(), file(), referens i dokument] Ingen oljeprodukt kan betraktas som helt ofarlig för hälsan. Hur hälsofarlig oljan är påverkas bland annat av hur ren den är. Även tillsatserna påverkar hälsofarligheten. Begagnade oljor kan innehålla hälsofarliga ämnen som bildats vid användning. En begagnad olja bör alltid hanteras som om den vore hälsofarlig. Det sätt som oljan hanterar på har stor betydelse. En felaktig hantering ökar riskerna. Finfördelad olja som kan spridas i luften bildar oljedimma, som kan t ex ge oljelunga. Hudkontakt Olika typer av hudpåverkan är uttorkning, irritation, icke-allergiskt och allergiskt kontakteksem, oljeakne och i sällsynta fall hudcancer. Inandning Olja i form av ånga, rök eller dimma verkar irriterande på andningsvägarna. Vid inandning kan det ge sveda i näsa och hals, hosta och heshet. Vid exponering för mycket kraftig oljerök eller oljedimma finns risk för oljelunga, vilket är en slags lunginflammation. Ögonkontakt Stänk i ögonen kan, beroende på oljans sammansättning och grad av förorening, ge allt ifrån sveda till frätsår. Det är lätt att överföra oljan genom att gnugga sig i ögonen med oljenedsmutsade fingrar. Nedsväljning Vid nedsväljning av olja och samtidig kräkning finns risk för att oljan kommer ned i lungan. Om det är en tunnflytande mineralolja kan det ge upphov till sk kemisk lunginflammation. Oljan är farlig, vid nedsväljning, genom sin förmåga att breda ut sig om den kommer ner i lungan. Referens = Arbetsmiljöverket, information om risker med oljor [chemfile(), file(), referens i dokument]
Ångorna kan ha irriterande inverkan på ögon, slemhinnor och andningsvägar. Tallolja innehåller kolofonium, som kan ge allergiskt kontakteksem. Referens = Arbetsmiljö från A till Ö [chemfile(), file(), referens i dokument]
En svensk standard, SS 15 54 70, har utarbetats av SIS1 som bl a ställer miljökrav på smörjfetter. 1SIS, Swedish Standards Institute, är en medlemsbaserad, ideell förening som är specialiserad på nationella och internationella standarder Smörjfetter bör uppfylla samtliga miljöegenskapskrav enligt svensk standard 15 54 70. Miljökraven innebär att smörjfetter ska bl a vara biologiskt nedbrytbara samt ge minimerad vattentoxicitet. Kraven innebär också bl a en kontroll av allergiframkallande ämnen samt ämnen med särskilt hälso- och miljöfarliga egenskaper (CMR, PBT 2). 2 CMR = Cancerframkallande, Mutagena och Reproduktionsstörande PBT = Persistent (svårnedbrytbart), Bioackumulerande (som ansamlas i levande organismer) och Toxisk (giftigt) Referens = SP, Sveriges Tekniska Forskningsinstitut, Borås [chemfile(), file(), referens i dokument] [chemfile(), nC=0 nr=i-oljor, f1=/produkt/info/html/i-oljor.htm]
Smörjolja är ofta mineraloljebaserad. Den delas in i olika klasser beroende på sin viskositet. Syntetisk olja är antingen en mineralolja som har manipulerats genom diverse tekniska processer, så att den har fått förbättrade egenskaper eller en syntetiskt framställd olja, t ex från råvaran etylen. Syntetiska oljor har ett betydligt högre pris än standardoljor. Dessa är vidare indelade i ett specifikt klassningssystem API, ILSAC, ACEA. Viskositeten eller tätheten för oljans främsta verkningsområde mäts med siffror, tex 5w10 till 15w50. Den första oljan är tunn och den sista mer trögflytande. Referens = Litteratur om teknisk kemi [chemfile(), file(), referens i dokument] Formoljor är avsedda att underlätta att formen släpper den härdade betongen vid gjutning av betongelement och andra detaljer samt att betongen får en slät och blåsfri yta. Referens = Texaco smörjmedel [chemfile(), file(), referens i dokument] Gejderoljor används för att smörja glidytor (gejdrar) på verktygsmaskiner. Referens = Texaco smörjmedel [chemfile(), file(), referens i dokument] Hydrauloljor finns i ett flertal varianter och är utvecklade för att klara olika typer av driftsförhållanden. Exempelvis varierande temperaturer, känsliga miljöer, platser där brandrisken är stor eller vid hantering av livsmedel. Oljorna ska skydda mot korrosion och slitage. Referens = Texaco smörjmedel [chemfile(), file(), referens i dokument] Industriväxeloljor används för tryck-, bad- och stänksmörjning av slutna växlar och transportkedjor med tillhörande lager. De är avsedda att smörja och skydda mot höga yttryck och belastningar. För att klara de höga yttrycken finns speciella högtryckstillsatser, EP (Extreme Pressure) i alla industriväxeloljor. Referens = Texaco smörjmedel [chemfile(), file(), referens i dokument] Kompressoroljor är avsedda att smörja, ge rostskydd och täta komprimeringen av luft. Referens = Texaco smörjmedel [chemfile(), file(), referens i dokument] Kylkompressoroljor får vid smörjning inte reagera med kylmedlet och ska också ha goda flytegenskaper även vid mycket låga temperaturer. Referens = Texaco smörjmedel [chemfile(), file(), referens i dokument] Luftverktygsoljor är avsedda för luftsmörjning genom att små oljedroppar bildas som följer med luftströmmen. Dessa bildar en oljefilm som smörjer verktygets utsatta delar samt skyddar delarna mot korrosion. Referens = Texaco smörjmedel [chemfile(), file(), referens i dokument] Metallbearbetningsoljor är ett samlingsbegrepp på de smörjmedel som används inom verkstadsindustrin vid tillverkning av metalldetaljer, dels via skärande bearbetning och dels via plastisk formförändring. Gemensamt för oljorna är att de ska ha rätt smörjande och skyddande egenskaper. Referens = Texaco smörjmedel [chemfile(), file(), referens i dokument] Processoljor används som råvaror vid kemisk-teknisk tillverkning, de utgör viktiga komponenter vid tillverkning av bland annat plast, trycksvärta, skokräm och sprängmedel. Referens = Texaco smörjmedel [chemfile(), file(), referens i dokument] Rostskyddsoljor måste kunna fästa och tränga in i sprickor och hålrum för att ge ett skyddande mjukt eller fast skikt. Skiktet ska skydda mot luft och fukt. Oljorna ska vara lätta att applicera och i förekommande fall också vara lätta att tvätta bort. Referens = Texaco smörjmedel [chemfile(), file(), referens i dokument] Sågkedjeoljor ska bilda en tunn men mycket tålig oljefilm som smörjer kedjans länkar och nitar. Vidhäftningsförmågan måste vara god eftersom kedjan snurrar med hög hastighet. Referens = Texaco smörjmedel [chemfile(), file(), referens i dokument] Transformatoroljor ska fungera som isolator och stoppa elektriska genomslag mellan lindningarna i en transformator. De ska också avleda värmen som uppstår av det elektriska motståndet i lindningar och kärna. Referens = Texaco smörjmedel [chemfile(), file(), referens i dokument] Turbinoljor används för att smörja turbinernas lager, kuggväxlar och reglerutrustning. Cirkulationsoljor pumpas runt i systemet för att smörja de ställen som kräver smörjning. Oljorna måste ha god oxidationsstabilitet och kunna ge skydd mot slitage och korrosion. Referens = Texaco smörjmedel [chemfile(), file(), referens i dokument] Värmeöverföringsoljor används främst för indirekt värmeöverföring i slutna system, exempelvis för uppvärmning av cisterner och i torkanläggningar. Referens = Texaco smörjmedel [chemfile(), file(), referens i dokument] Smörjfett är i första hand indelade i grupper efter sitt användningsområde, i andra hand efter vilken tvåltyp som används. Fetter som har tillägget EP (Extreme Pressure) har tillsatser för att klara smörjning av utsatta delar som arbetar under höga tryck. Använndingsområdet är framförallt i kul- och rullager, men även i glidlager, växellådor och öppna kuggväxlar. Smörjfett består oftast av komponenterna - Basolja (80-90%) - Förtjockare ca 10% - Tillsatsmedel ca 5% Referens = Circle K (Statoil) [chemfile(), file(), referens i dokument] Smörjfett är ett halvflytande smörjmedel bestående av en smörjolja förtjockad med olika typer av förtjockare. Smörjfettets konsistensen mäts i så kallade NLGI-klasser. Den vanligaste konsistensklassen, NLGI 2, är tixotrop, dvs fast då fettet inte utsätts för någon yttre mekanisk påverkan vilket gör att fettet till skillnad från smörjolja stannar vid smörjstället. När fettet dras in i det smorda kontaktområdet får det egenskaper motsvarande en smörjolja (flytande) för att, när rörelsen upphör, återta sin fasta form. Smörjfett minimerar slitage på rörliga delar. När friktionen minskar blir motorer och maskiner effektivare. Smörjfett ska även skydda mot korrosion. NLGI-talet är ett klassifikationsschema för smörjfetter. Det har fått sitt namn efter National Lubricating Grease Institute. Det mäter smörjfetters konsistens, ett mått på relativ hårdhet/mjukhet. NLGI-talet säger ingenting om ett fetts dynamiska viskositet eller smörjförmåga, men används bl a som instrument för produktionskontroll. Ju högre NLGI-tal desto styvare konsistens.
Viskositet är en fysikalisk egenskap hos smörjfetter som betecknar deras tjockhet eller interna motstånd mot flöden, och kan ses som ett mått på friktionen. Referens = Litteratur om teknisk kemi [chemfile(), file(), referens i dokument] Kuggfetter är avsedda för smörjning av öppna kuggväxlar, grova kedjor, vajrar och glidytor som arbetar i dammiga och fuktiga miljöer. Referens = Texaco smörjmedel [chemfile(), file(), referens i dokument] Glidytessmörjfett används för att smörja glidlager, leder och glidytor på fordon och i industriella applikationer. Referens = Texaco smörjmedel [chemfile(), file(), referens i dokument] Lagerfett finns i flera varianter och har många användningsområden. De är bland annat lämpliga till rull-, kul- och glidlager som är utsatta för hård belastning, både i fordon och inom industrin. Referens = Texaco smörjmedel [chemfile(), file(), referens i dokument]
Järnproduktion i masugn följt av stålproduktion i syrgaskonverter. Slutprodukten är tunnplåt som framför allt används i byggindustrin och för tillverkning av fordon och maskiner. 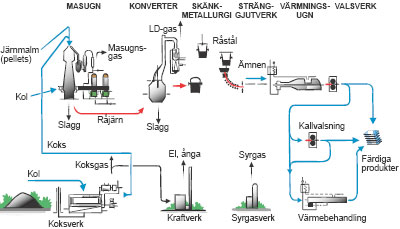
Referens = Jernkontoret [chemfile(), file(), referens i dokument]
[chemfile(), nC=0 nr=ironw, f1=/produkt/info/html/ironw.htm] Järnproduktion i masugn följt av stålproduktion i syrgaskonverter. Slutprodukten är tunnplåt som framför allt används i byggindustrin och för tillverkning av fordon och maskiner. 
Referens = Jernkontoret [chemfile(), file(), referens i dokument] Råvaror Vid tillverkning av stål krävs järnråvara i form av Vid tillverkning av Järnmalm Rent järn förekommer ytterst sparsamt i jordskorpan. Däremot finns det järn som är kemiskt bundet, i förening med andra grundämnen som syre och svavel. Jordskorpans vanligaste grundämnen är i nämnd ordning syre, kisel, aluminium och järn. För utvinning av järnmetall är föreningarna med syre, oxider, de helt dominerande. Järnmalmsmineralen kallas för magnetit (svartmalm) eller hematit (blodstensmalm) beroende på vilken typ av oxid som ingår. Magnetit har fått sitt namn genom sina magnetiska egenskaper. Om den repas mot en ofärgad yta så bildas ett svart streck. Dess kemiska beteckning skrivs ofta Fe3O4, men eftersom den är en blandoxid är det mer korrekt att skriva FeO(Fe2O3). Hematit eller blodstensmalm, Fe2O3, har fått sitt namn av det blodröda streck som bildas om den repas. I Sverige bryts järnmalm i Kiruna och Malmberget av LKAB, som är Europas största järnmalmsproducent. Efter brytningen krossas materialet och därefter avskiljs malmen från gångarten, sk anrikning. Med magnetitmalm sker det genom magnetisk separation. Den anrikade produkten kallas slig. Sligen kan sedan formas och agglomereras till pellets, små runda kulor med bestämd sammansättning, storlek och hållfasthet. Pelletskulor är den huvudsakliga järnråvaran vid svensk tillverkning av malmbaserat stål. Den svenska järnmalmen består huvudsakligen av magnetiter, vilket har den fördelen att vid pelletstillverkningen kan den kemiska energi som finn i magnetitmalmen utnyttjas. När pelletsen bränns oxiderar magnetit till hematit vilket frigör energi. Den energi som behövs i processen kommer till 70 procent från malmen. Den färdiga pelletsen innehåller cirka 65 procent järn. Skrot Järn- och stålskrot används som råvara både i den skrotbaserade och den malmbaserade ståltillverkningen. Skrotet sorteras i olika klasser och stålverken använder en blandning av de skrotsorter som passar det stål som man vill tillverka. Stålskrot Stålskrot är en värdefull järnråvara. Skrot kan delas in i tre grupper beroende på typ. Kol Stenkol kan inte användas direkt i masugnarna. Därför koksas stenkolet, vilket innebär att vatten och flyktiga ämnen tas bort. Koksen får på så sätt den hållfasthet som krävs i masugnen. Kolets funktion vid järnframställning är främst som reduktionsmedel för att omvandla järnoxiden till järn. Koksen bär upp masugnens innehåll, höjer kolhalten i järnet och tillför energi. Kalk Kalk används som slaggbildare vid järn- och ståltillverkningen. Slaggen har flera funktioner, men främst är den en aktiv komponent i de metallurgiska processerna. Slaggen binder ämnen som inte önskas i stålet. På så sätt kan stålets ämnessammansättning styras och därmed ge stålet förbättrade egenskaper. Legeringsämnen Stål är en legering med järn som basmaterial. I allt stål ingår låga halter av t ex kol, kisel och mangan. Under tillverkningsprocessen tillsätts legeringsämnen, t ex krom, nickel, molybden och vanadin, ofta i form av ferrolegeringar (ferrokisel, ferromangan, ferrokrom ferrovanadin, etc). På så sätt skapas förutsättningar för att ge stålet önskade egenskaper, exempelvis korrosionsbeständighet, hårdhet, slitstyrka och seghet. Tillsatserna av legeringsämnen är större i höglegerat stål, t ex rostfritt stål. Ett vanligt rostfritt stål innehåller 18-20% krom och 8-10% nickel. Bestick, kastruller och diskbänkar är ofta tillverkade av denna stålsort som brukar kallas för 18/8-stål. När skrot används som råvara vid tillverkningen av råstål används, så långt det är möjligt, skrot som innehåller de legeringsämnen som det nya stålet ska bestå av. Under tillverkningsprocessen analyseras det smälta stålet och för att det ska få exakt rätt sammansättning tillsätts även legeringsämnen. Referens = Jernkontoret [chemfile(), file(), referens i dokument]
Skänkmetallurgi, CAS-OB (cas-ob) (cas-ob)
I Referens = Jernkontoret, Stockholm [chemfile(), file(), referens i dokument] Här sker den sista kemiska- och termodynamiska finjusteringen på stålet för att uppnå de analys- och temperaturkrav som gäller för den stålsort som ska produceras. Vid SSAB i Luleå är CAS-OB en skänkmetallurgianläggning med trådmatning och bulkmatning av legeringar. Här behandlas stålet till rätt temperatur och kemisk analys för leverans till stränggjutningen. Utrustning - Ferromangan (FeMn), - Ferrokisel (FeSi), - Kiselkarbid (SiC), - Ferroniob (FeNb), - Ferrovanadin (FeV), - Ferromolybden (FeMo), - Ferrotitan (FeTi) , - kol - Aluminium (Al), - Ferrobor (FeB), - Kalciumkisel (CaSi) - Instrument för mätning av temperatur och syreaktivitet - Utrustning för provtagning av stål - Processtyrningsutrustning - System för tillsättning av kylskrot - System för gasspolning via spolsten alternativt spollans - Tråd hasplas på i stora haspeltrummor och tillförseln av tråd ner i smältan kan ske med ett vanligt trådmatarverk Process - Skänken placeras i position - Argonspolning startas för att lösa upp hård slagg och för att homogenisera stålet i skänken - Nedsänkning av skyddsklockan - Temperaturmätning och första provet tas för kemisk analys - Eventuell justering av temperatur - Tillsats av legeringar enligt tillverkningsföreskrifter, t ex niob (Nb), mangan (Mn), titan (Ti), bor (B), aluminium (Al), och argonspolning. - Ny temperaturmätning och prov för kemisk analys - Då stålet i skänken har rätt temperatur och kemisk analys skickas den vidare till stränggjutning Processoperatören styr så att chargen (skänken) har rätt mängd legeringsämnen och temperatur för gjutning i stränggjutningen. Under större delen av processen spolas argon i botten av skänken för omrörning så att blandningen blir homogen samt för att transportera oönskade inneslutningar till slaggen. Vid SSAB i Luleå har varje stålsort ett unikt recept som måste följas exakt. Operatörerna använder datorer och laboratoriesvar från analysprover för att kontrollera att stålet innehåller rätt mängd av rätt ingredienser och har rätt temperatur. Legeringar I CAS-OB justeras stålet till rätt temperatur och kvalitet genom tillsatser av legeringsämnen och genom homogenisering. För att homogenisera stålet blåses argon in genom en spolsten i botten på skänken. Stålet kan värmas med syrgas och tillsats av aluminium eller kylas med stålskrot. Temperaturen justeras i skänken genom att samtidigt tillsätta aluminium och syrgas som ger en exoterm reaktion där aluminiumoxid (Al2O3) bildas. I den exoterma reaktionen när aluminium oxideras avges nödvändig energi direkt in i stålet. En exoterm reaktion är en kemisk reaktion där energi (oftast värme) avges. Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
RH-processen RH-processen är uppkallad efter de två företag, Ruhrstahl och Heraeus, som utvecklade den. 1)
ppm (parts per million) är en förkortning för miljondel på samma sätt som procent för hundradel och promille för tusendel. För att omvandla lufthalter av gaser och ångor mellan ppm och mg/m3 går det att räkna ut ett omvandlingstal genom att dividera ämnets molekylvikt med 24. T ex är molekylvikten 97 för diklormetylen (C2H2Cl2) och omvandlingstalet är då 4,0. För att omvandla från ppm till mg/m3 multipliceras ppm med omvandlingstalet. T ex är 20 ppm diklormetylen 20*4=80 mg/m3. För att omvandla från mg/m3 till ppm ska mg/m3 divideras med omvandlingstalet. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument] Referens = Jernkontoret, Stockholm [chemfile(), file(), referens i dokument]
Tillverkning av koks, SSAB Luleå Koks behövs i masugnen som reduktionsmedel för att få ut järn ur järnpellets. En mindre mängd köps in som färdig koks, men huvudsakligen SSAB tillverkar koks i koksverket av importerat stenkol. Vid koksningen, som är en torrdestillation utan lufttillförsel, avdrivs flyktiga föreningar som gas, sk rågas. Den färdiga koksen trycks ut på en släckvagn och kyls med vatten. Efter kylningen transporteras koksen vidare med band till masugnen. Gasen renas i flera steg. Vid gasreningen utvinns biprodukterna tjära, råbensen och svavel. Den renade koksgasen används som bränsle för bl a uppvärmning och det som inte används i koksverket distribueras till masugnen och till blandgasklockan. Från kokstillverkningen faller en avsiktad fin andel av koks (koksgrus). Övrig restmaterial som uppkommer i produktionen återförs tillbaka med kolet Råvaran till koks är kol av ett flertal kvaliteter. Från produktionen erhålls en energirik koksgas som till en del (ca 40-45%) används för att värma upp batteriet. Överskottet av koksgas används till uppvärmning inom övriga egna verksamheter och det som inte används internt distribueras i processgasledningar till blandgasklockan. I blandgasklockan lagras blandgas som är en blandning av koksgas, masugnsgas och LD-gas. Blandgasen distribueras i processgasledningar och säljs till Lulekraft AB (LUKAB) och den mängd som LUKAB inte kan ta emot säljs till Luleå Enerig AB (LEAB). LUKAB producerar elkraft, ånga och hetvatten i sitt kraftvärmeverk. LEAB använder gasen för att producera el, som distribuerars till hushåll och företag inom Luleå kommun. Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
Masugnsprocessen Masugnen består av ett schakt, där järnbärare, slaggbildare och koks tillsätts överst. I nede delen blåses blästerluft 1) in. Syret i luften reagerar med kolet i koksen och bildar koloxid (CO), som strömmar uppåt, möter och värmer den nedåtgående besckickningen. SSAB i Luleå använder malmpellets från LKAB för tillverkning av råjärn och som reduktionsmedel används både koks och kolpulver. LKAB-pellets tillverkas av magnetitmalm och har hög järnhalt, över 66%. För att omvandla malmpellets till råjärn i masugnen måste syret i malmpelletsen tas bort. Det kallas för reduktion. Masugnsprocessen är en smältreduktionsprocess. Järn i malmpelletsen är bundet till syre som magnetit med den kemiska beteckningen Fe3O4. Fe är den kemiska beteckningen för järn och O den kemiska beteckningen för syre. Siffrorna anger antalet atomer. Ett reduktionsmedel måste tillsättas som kan reagera med syret under hög temperatur. Som reduktionsmedel används kol, med kemisk beteckning C, i form av koks och kolpulver. Masugnen matas dygnet runt med järnmalmspellets, slaggbildare, koks och tillsatsämnen (t ex kvartsit och ferromangan) från masugnens topp. Koksen bär upp den stora pellets- och kokspelaren inuti masugnen. Koksens styckeform släpper igenom smält råjärn som kan droppa ned och tillåter gas att stiga upp genom masugnen. En del av koksen kan ersättas med injektion av kolpulver i masugnens blästerluft 1). Blästerluft 1) tillsätts under högt tryck genom ett antal grova munstycken under masugnen där kolpulver samtidigt injiceras. Blästermunstyckena kallas formor. Blästerluften värms upp i höga murade torn, cowprar eller varmapparater, med återvunnen energi från masugns- och koksgas. Materialbalans masugn - Järnmalmpellets - Kalksten - LD-slagg - Manganmalm - Koks - Kolpulver - Blästerluft 1) - Råjärn - Slagg - Hyttsot - Masugnsgas Principen för kemiska reaktioner Reduktionsprocessen sker inuti den keramiskt infodrade masugnen. I översta delen av masugnen sker inga reaktioner, gasen värmer endast materialet. Vid ca 400oC börjar järnoxiderna reduceras genom att magnetit reagerar med koloxid. Reduktion med koloxid kallas för Längre ned i masugnen är temperaturen högre och järnoxid reagerar direkt med kol. Den reaktionen kalals för Järnet smälter vid cirka 1500oC. När järnet reducerats och har smält droppar det ned och samlas upp i masugnens botten, det så kallade stället. Masugnen tappas i jämn takt. Tappningarna pågår under 2 timmar och därefter görs ett uppehåll på 40-50 minuter innan nästa tappning äger rum. I nedersta delen av masugnen är temperaturen så hög att järnet smälter och genom upptagning av kol får en kolhalt på 3,5 - 5%. Processgaser Då malmpellets reduceras med kol bildas kolmonoxid (CO) och koldioxid (CO2) som leds från masugnen via grova rör till en reningsanläggning. Kolmonoxiden är energirik. Masugnsgasen återvinns som energi dels till masugnens egna processer, dels till andra anläggningar och dessutom för elproduktion och till fjärrvärme hos externa kunder. Slagg Kalk tillsätts i masugnsprocessen för att samla upp kisel och andra oönskade ämnen till en slagg. När råjärnet tappas ur masugnen följer också slaggen med. Slaggen består huvudsakligen av kisel och kalk. Kisel är rester från det gråberg som omgivit malmkropparna. Slaggen ligger ovanpå det flytande råjärnet. Den skiljs av i tapprännan och tappas separat. Slagg återvinns som Elproduktion För LUKAB producerar elkraft, ånga och hetvatten i sitt kraftvärmeverk. LEAB använder gasen för att producera el, som distribuerars till hushåll och företag inom Luleå kommun. 1)
Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
Stränggjutning Strängjutning av avancerade stålsorter, s k nischstål, kräver god kontroll av både maskin och process. Vid gjutningen används gjutpulver vars sammansättning och därmed egenskaper har stor betydelse för möjligheten att gjuta dessa stålsorter utan processtörningar och allvarliga ytdefekter. Stålet transporteras till gjutstationen i en skänk. Från skänken tappas stålet i en gjutlåda. Tappningen görs genom botten av skänken genom en dysa, även kallad tärning. Stålflödet regleras i regel med hjälp av en skivtärning. I och med att man har några minuters uppehållstid av stålet i gjutlådan kan man växla till en ny skänk efter att en skänk har gjutits färdig. Man brukar tala om att gjuta i sekvenser. Från gjutlådan flyter stålet genom en dysa (tärning) ner i kokillen. För att skydda smältan från att ha luftkontakt när den transporteras från skänk till gjutlåda och från gjutlåda ner i kokill används gjutrör. I gjutlådan skyddas överytan mot luft med I kokillen tillsätts När stålet hamnat i den vattenkylda kopparkokillen stelnar ett skal och strängen kan transporteras ut genom botten av kokillen. För att stålet inte ska fastna rör sig kokillen i en oscillerande rörelse som minskar friktionen mellan kokill och skal. Strängen dras ut med drivrullar under kokillen. När stålskalet lämnat kokillen kommer det ut i en rad kylzoner med sprayvattenkylning. Fortfarande är inte ämnet genomstelnat utan det finns en smälta kvar i mitten. Denna smälta kallas ofta för sumpen och dess slutspets sträcker sig normalt 30 till 35 meter ner i strängen. Det viktiga är att det är stelt innan kapning sker. Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
[chemfile(), nC=0 nr=452-b, f1=/produkt/info/html/452-b.htm] Rågas, koksgas Vid koksningen, som är en torrdestillation utan lufttillförsel, avdrivs flyktiga ämnen i kolet som gas, sk Rågasen renas i flera steg. Den renade rågasen ( Koksningsprocessen Vid koksningsprocessen avger kolet sina flyktiga beståndsdelar i form av rågas, med följer även vattenångan från fukten i kolet. Den största delen av rågasen består av vätgas och metangas, men den innehåller även ämnen som bensen, svavel, tjära samt en mängd olika kolväteföreningar t ex cyanider. Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
[chemfile(), nr=630-08-0, f1=/produkt/chemdata.dat] Koloxid bildas Koloxid (kolmonoxid) är en färglös, luktlös och mycket giftig gas. Den bildas vid förbränning med låg syretillförsel (ofullständig förbränning). Ju lägre syretillförsel, desto mer koloxid bildas. Koloxid är brandfarligt och bildar explosiva blandningar med luft. Inverkan av koloxid på kroppen I de röda blodkropparna finns det särskilda molekyler (hemoglobin) som har till uppgift att ta upp syre från luften i lungorna och transportera till kroppen olika delar. Koloxid binder sig mycket starkt till dessa molekyler och förhindrar dem då att transportera syre. Koloxidförgiftning är en form av inre kvävning. Redan mycket låga halter av koloxid i luften kan förorsaka syrebrist i kroppen. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), chemdata.dat, referens i dokument]
[chemfile(), nC=0 nr=1003-064, f1=/produkt/info/html/1003-064.htm] LD-gas 1) 1)
LD är en förkortning för Linz-Donawitz, efter de orter där tekniken först användes i fullskaledrift, och det är en process inom kategorin BOS (Basic Oxygen Steelmaking) med syrgasblåsning via lans. Referens = Jernkontoret, Stockholm [chemfile(), file(), referens i dokument] LD-gas bildas i LD-konvertern då råjärn färskas till råstål. Färskning är den process inom järnmetallurgin vid vilken kolhalten i råjärn sänks genom oxidation till de nivåer som gör järnet smidbart. Råjärnet som kommer direkt från masugnen innehåller vanligtvis ca 4-5% kol och är för sprött för att smidas, valsas eller härdas. Genom färskningen sänks kolhalten till under 2%, och järnet blir då smidbart. Genom en lans blåses 99% rent syrgas i konvertern och kolet som är löst i råjärnet reagerar med syre till koloxid (CO) och koldioxid (CO2) och råjärnet övergår i råstål då kolhalten har sänkts till under 2%. Gasen sugs från konvertern till gasreningssystemet med ett kraftigt fläktsystem. Luft från omgivningen sugs även med processgaserna till gasreningssystemet, vilket innebär att en del av koloxiden reagerar med luftens syre till koldioxid (CO2). I gasreningssystemet som är av typ våtgasrening renas gasen från stoft som följer med från konvertern. Som ett komplement till syrgasblåsning i LD-konverter finns bottenspolning med kvävgas (N2) eller argon (Ar), LBE - Lance Bubbling Equipment, för att bl a uppnå en mer effektiv omrörning. Halten av löst kväve i stålet bestämmer vilken spolgas, kvävgas (N2) eller argon (Ar), som används. En vanlig metod är att spola med kvävgas (N2) i början då kvävehalten i stålet är låg, för att sedan växla till argon (Ar) i slutet av blåsningen. Processgasen som bildas kallas för Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
[chemfile(), nC=0 nr=1193-1, f1=/produkt/info/html/1193-1.htm] Masugnsgas SSAB i Luleå använder malmpellets från LKAB för framställning av råjärn i masugn. För att omvandla malmpellets till råjärn i masugnen måste syret i pelletsen tas bort. Det kallas för reducering. Masugnsprocessen är en smältreduktionsprocess. Som reduktionsmedel används kol, med kemisk beteckning C, i form av koks och injektionskol. I reduktionsprocessen i masugnen reagerar syret i pelletsen och kolet till gas, kolmonoxid (CO) och koldioxid (CO2). Den bildade masugnsgasen innehåller ca 20-24% koloxid och ca 20-24% koldioxid. Masugnsgasen innehåller även ca 50% kvävgas och 2-4% vätgas och gasen leds från masugnen via grova gasrör till en gasreningsanläggning. Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
Svaveldioxid [chemfile(), nC=0 nr=SO2, f1=/produkt/info/html/SO2.htm] Svaveldioxid (SO2) är en färglös gas med stickande lukt. Om gasen löses i vatten bildas svavelsyrlighet, som är en färglös och frätande syra, som är svagare än svavelsyra. Då svaveldioxid kommer i kontakt med fuktigheten i ögon och andningsvägarnas slemhinnor bildas svavelsyrlighet, som är starkt irriterande och frätande. Svaveldioxid som sugits upp i kläderna och förenats med vatten fräter på huden. Vid inandning påverkar svaveldioxid luftvägarna redan vid relativt låga halter, t ex ökar andningsmotståndet i luftvägarna. Astmatiker är särskilt känsliga för svaveldioxid. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument] Råjärn [chemfile(), nC=0 nr=SO2-056, f1=/produkt/info/html/SO2-056.htm] SSAB Kalk tillsätts i masugnsprocessen för att samla upp kisel och andra oönskade ämnen till en slagg. Slaggen består huvudsakligen av kisel och kalk samt aska från koks och kol. Kisel är rester från malmens gråberg. Askan i slaggen kan bl a innehålla sulfater (svavelföreningar) från kol och koks. Slaggen ligger ovanpå det flytande råjärnet. När råjärnet och slaggen tappas ur masugnen kan det bildas Referens = SSAB Luleå [chemfile(), file(), referens i dokument] Svaveldioxid [chemfile(), nC=0 nr=SO2, f1=/produkt/info/html/SO2.htm] Svaveldioxid (SO2) är en färglös gas med stickande lukt. Om gasen löses i vatten bildas svavelsyrlighet, som är en färglös och frätande syra, som är svagare än svavelsyra. Då svaveldioxid kommer i kontakt med fuktigheten i ögon och andningsvägarnas slemhinnor bildas svavelsyrlighet, som är starkt irriterande och frätande. Svaveldioxid som sugits upp i kläderna och förenats med vatten fräter på huden. Vid inandning påverkar svaveldioxid luftvägarna redan vid relativt låga halter, t ex ökar andningsmotståndet i luftvägarna. Astmatiker är särskilt känsliga för svaveldioxid. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument]
Svavelväte [chemfile(), nC=0 nr=svavelv, f1=/produkt/info/html/svavelv.htm] Svavelväte, vätesulfid (H2S), är en kemisk förening av svavel och väte. Det är en giftig gas med en lukt som påminner om ruttna ägg. I höga koncentrationer kan gasen förorsaka snabbt medvetslöshet och vara livshotande. I koncentrationer över 150 ppm 1) bedövas luktsinnet och då fungerar inte längre lukten som varningssignal. Vid lägre koncentrationer av svavelväte visar sig verkningarna i form av trötthet och irritation i luftvägarna. Vid halter om ca 50-100 ppm 1) uppstår svår ögonirritation, ofta med synrubbningar. Med stigande halter påverkas hjärnan och nervsysyemet allt mer. Luktsinnet förlamas, omdömesförmågan minskar, balansförmågan försämras. Det kan också uppstå livshotande lungskador (lungödem). Vid mycket höga halter uppstår snabbt medvetslöshet. Hos den som en längre tid varit utsatt för svaveläväte kan det förekomma symptom som slemhinneirritation, huvudvärk, trötthet, irritation och sömnlöshet. 1)
ppm (parts per million) är en förkortning för miljondel på samma sätt som procent för hundradel och promille för tusendel. För att omvandla lufthalter av gaser och ångor mellan ppm och mg/m3 går det att räkna ut ett omvandlingstal genom att dividera ämnets molekylvikt med 24. T ex är molekylvikten 97 för diklormetylen (C2H2Cl2) och omvandlingstalet är då 4,0. För att omvandla från ppm till mg/m3 multipliceras ppm med omvandlingstalet. T ex är 20 ppm diklormetylen 20*4=80 mg/m3. För att omvandla från mg/m3 till ppm ska mg/m3 divideras med omvandlingstalet. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument] Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument] Process [chemfile(), nC=0 nr=H2S-452, f1=/produkt/info/html/H2S-452.htm] Gasen efter naftalentvätten förs vidare till en svaveltvätt. Det är en absorbtionskolonn och där besprutas gasen med ammoniakvatten från ammoniaktvätten. Den renade gasen, efter svaveltvätten, förs upp genom toppen av kolonnen till ammoniaktvätten. Även där besprutas gasen med ammoniakvatten, som löser ammoniak i gasen. Det är det vatten som sedan används som tvättvätska i svaveltvätten. Tvättvätskan från svaveltvätten förs till destillationskolonner, sk avsyrare och avdrivare. Där frigörs svavelväte och ammoniak genom uppvärmning med ånga. I avdrivare förångas ammoniak och i avsyrare förångas svavelväte. Vattnet efter destillationskolonnerna återförs till ammoniaktvätten och cirkulerar mellan ammoniaktvätten, svaveltvätten, avsyrare och avdrivare i ett kretslopp. Ammoniakångorna (NH3)och svavelväteångorna (H2S) förs vidare till spaltugnen där spaltas ammoniakångorna till grundämnena kväve (N) och väte (H). I den efterföljande sk Clausanläggningen omvandlas svavelväte (H2S) till svavel (S) och här framställs flytande svavel för försäljning. Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
Aluminiumpulver i kontakt med vatten bildar vätgas. Referens = Arbetsmiljö från A till Ö, SO Hanssn, E Hellsten [chemfile(), file(), referens i dokument] Exempel på keramiska produkter som kan innehålla aluminiumpulver är gjutmassor som används till järn- och slaggrännor vid råjärnstillverkning i masugn. Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
Tjära / beck Tjära är en trögflytande vätska som erhålls som kondensat vid pyrolys (torrdestillation) av organiska material som kol och petroleum, tjära som bildas från kol kallas för Det finns risk för hudcancer och överkänslighet för solljus (fototoxiskt eksem) efter långvarig direktkontakt med tjära/beck. Eksem av typ fototoxiskt uppstår då huden utsätts för solljus. Polyaromatiska kolväten, polycykliska aromatiska kolväten eller polyaromater, ofta förkortat PAH av engelska Polycyclic Aromatic Hydrocarbons, är en grupp ämnen som finns i stenkol och petroleum (råolja). Det mest kända av dessa ämnen är benso(a)pyren. Flera av PAH-ämnena är cancerframkallande, t ex benso(a)pyren. Dessa ämnen har dessutom obehaglig lukt redan vid låga koncentrationer. PAH-ämnen är inte flyktiga men de sprids över stora områden med partiklar. Tjära och beck innehåller polyaromatiska kolväten (PAH). Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument] Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
Bensen är giftigt vid inandning, förtäring och långvarig hudkontakt. Ämnet kan lätt tas upp i kroppen vid inandning av ångor och genom hudkontakt med lösning. Stänk i Bensen kan ge ärftliga genetiska skador och leukemi (cancer) vid långvarig och upprepad exponering. Bensen är 1) Ångor av bensen är irriterande på andningsvägar och ögon. Vid långvarig och upprepad inandning av bensen finns risk för 1)
Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument]
[cfile() nchem=2 f1=/produkt/info/html/cyanid-a.htm ] Cyanider Cyanider och cyanföreningar är kemiska föreningar i vilka ingår en cyangrupp (kväve bundet till kol, CN). Cyanider är mycket giftiga vid såväl inandning som hudkontakt och kan orsaka huvudvärk, yrsel, öronsusningar, andnöd, illamående, kräkningar. Höga halter orsakar snabbt oregelbunden puls, andningsstillestånd, kramper och medvetslöshet. Cyanider kan vid uppvärmning bilda den mycket giftiga gasen Risk för att vätecyanid bildas vid exponering för cyanider Vätecyanid kan bildas genom hydrolys av cyanid, t ex då ångor av cyanider inandas och cyaniderna hydrolyseras till vätecyanid t ex i kontakt med slem. Hydrolys är en kemisk process där en molekyl klyvs i kontakt med vatten, t ex vid hydrolys av cyanider då frigörs den farliga cyanidjonen (CN) och då finns risk att vätecyanid bildas. Vid nedsväljning av cyanider i vätska, ångor eller partiklar som är kontaminerade med cyanider kan cyanider reagerar med magens saltsyra till Förgiftning Vätecyanid inaktiverar cellandningen genom att binda till järnet i ett protein i cellen som kallas för cytokrom C. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [cfile()] Cyanider råjärn [cfile() nchem=2 f1=/produkt/info/html/CN056.htm] I masugnen kan cyanid bildas vid extremt höga temperaturer på gasen i masugnens topp. Oftast försvinner den av sig själv på vägen genom masugnen men i speciella fall kan den stanna kvar Den varma gasen från masugnen renas i en torr och en våt behandling i cyklon respektive skrubber. Den våta gasreningen sker med hjälp av vatten. Om det finns cyanider i gasen kan de hamna i vattnet som används vid den våta gasreningen och som recirkuleras i en slambassäng. Det kan även ske cyanidutsläpp till slambassängen vid ojämn drift i masugnen, t ex vid ett bandgångshaveri till matningen av masugnstoppen. Referens = SSAB Luleå [cfile()] [cfile() nchem=2 f1=/produkt/info/html/CN056-r.htm] Vid råjärnstillverkning kan cyanider förekomma i vattnet i slambassängen för recirkulering av vatten som används vid våtgasrening av masugnsgas. Referens = SSAB Luleå [cfile()] Risker Hudkontakt med vattnet i bassängen eller inandning av ångor från bassängen kan medföra att cyanider tas upp i kroppen och då finns det risk att den starkt giftiga gasen Referens = SSAB Luleå [cfile()] Koksgaskondensat [cfile() nchem=2 f1=/produkt/info/html/CN452.htm] Vid torrdestillation av stenkol tilll koks omvandlas 25% av kolet till rågas som innehåller flyktiga ämnen från kolet, bl a cyanider. På koksbatteriet finns risk för exponering för cyanider, eftersom det uppstår rök och stoft då luckor öppnas vid påfyllning av stenkol till batteriet och stoftpartiklarna kan vara kontaminerade med cyanider. Inandning av partiklar kontaminerade med cyanid medför risk för exponering för cyanider. Vid nedsväljning kan cyanider från partiklar lösas i slem och komma i kontakt med magens saltsyra och då finns risk att den starkt giftiga gasen vätecyanid bildas. Rågasen renas i flera steg i gasreninigsanläggningen. Den renade rågasen kallas för koksgas och innehåller metan, koloxid, vätgas, kvävgas, vätesulfid och även spårmängder av fenoler och cyanider. Koksgas tranporteras till användare i rörledningar och det bildas kondensat som samlas upp i vattenlås. På rörens insida och i vattenlåsen kan det därför bildas beläggningar av kondensat som kan innehålla fenoler och cyanider.. Referens = SSAB Luleå [cfile()] [cfile() nchem=2 f1=/produkt/info/html/CN452-r.htm] Cyanider, koksgaskondensat Cyanider kan finnas i koksgaskondensat och avlagringar av koksgaskondensat i ledningssystem och vattenlås för koksgas Referens = SSAB Luleå [cfile()] Risker Cyanider kan vid uppvärmning bilda vätecyanid. Vid arbeten som medför att koksgaskondensat, t ex i koksgasledningar, utsättes för höga temperaturer kan den starkt giftiga gasen Inandning av Referens = Litteratur om kemiska hälsorisker [cfile()]
Definitioner Den mängd partiklar (aerosoler) som fastnar på ett filter vid provtagning. Den mängd partiklar, av totalmängden partiklar i luften, som man inandas genom näsa och mun. Den del av de inhalerbara partiklarna som passerar struphuvudet. De inhalerbara partiklar som når längst ner i luftvägarna, till alveolerna i lungorna. Hälsorisker Faktorer som bidrar till farligheten hos damm är storlek, typ av damm och typ av medföljande ämnen. Det är de Exponering för höga halter damm kan ge upphov till irritation i ögon och i de övre luftvägarna (näsa, hals) och det är de grövre partiklarna som har irriterande egenskaper. De mindre dammkornen når längre ned i luftvägarna och det farligaste dammet är de små dammkornen som når längst ner i luftvägarna och det märker man inte att man andas in. Farligast att andas in är de Inandning av höga halter Flimmerhår Luftvägarnas yta är beklädd med ett tunt lager slem. Innanför detta lager finns celler som är försedda med flimmerhår (cilier). Flimmerhåren slår mycket snabbt fram och tillbaka och deras rörelse förflyttar slemmet uppåt i luftvägarna mot svalget. Dammkorn som fastnar i slemmet forslas uppåt av flimmerhåren. De hamnar så småningom i svalget där de antingen sväljs ned eller hostas upp. Halveringstiden för detta reningssystem är bara några timmar. Makrofager I alveolerna (lungblåsorna) finns makrofager, celler som kan omsluta och svälja utifrån kommande dammkorn. Inuti makrofagerna finns kemiska ämnen (vissa enzymer) som sönderdelar och bryter ned många av de slukade småkornen. Makrofagerna kan effektivt lösa upp många svårlösliga partiklar. Sedan rör sig makrofagrena långsamt ut ur alveolerna, där flimmerhåren (cilierna) tar hand om dem och transporterar dem vidare. Makrofagerna kan också föras bort av det lymfsystem som finns i lungorna. Halveringstiden för detta reningssystem är av storleksordningen 2 mån. Halveringstid = den tid det tar att avlägsna hälften av partiklarna Kvartsdamm Keramiska produkter som innehåller kiseldioxid (SiO2) kan också innehålla I keramiska produkter som innehåller kiseldioxid (t ex gjutmassor och tegel) som används i produktionsanläggningar (t ex skänkar) och som har varit utsatta för höga temperturer, kan en del av kiseldioxiden ha omvandlats till silikosframkallande kvartsformer (alfa-kvarts, kristobalit och tridymit). Vid dammande hantering av murad keramik (t ex rivning) finns därför risk för exponering för silikosframkallande kvartsdamm. Inandning av höga halter Inandade respirabla silikosframkallande kvartspartiklar, som hamnar i lungblåsorna (alveolerna), kan makrofagrerna svälja men inte sönderdela och därför kan dammkorn av detta slag inlagras i lungvävnaderna och leda till silikos och även till cancer. I motsats till andra dammkorn fortsätter silikosframkallande kvarts sin åverkan på makrofagerna även om exponeringen upphör. Det är därför silikos, i motsatt till flertalet andra former av dammlunga, fortsätter att förvärras även efter att exponeringen för dammet upphört. Referens = Arbetsmiljöverkets föreskrifter [chemfile(), file(), referens i dokument] Referens = Arbetsmilö från A till Ö, SO Hansson, E Hellgren [chemfile(), file(), referens i dokument]
Dioxiner Av de totalt 210 kongenerna bedöms 17 kongener, varav 7 PCDD och 10 PCDF, vara både mycket toxiska (giftiga) och persistenta (svårnedbrytbara i miljön). Vanligtvis är det de här 17 olika toxiska PCDD- och PCDF-kongenerna som brukar analyseras. Den mest giftiga kongenen, och den mest studerade, är PCB PCB är en förkortning för polyklorerade bifenyler. Dessa utgör en serie av 209 enskilda kongener (varianter) som skiljer sig genom antalet kloratomer och deras plats i molekylen. PCB är en industrikemikalie som har haft många olika användningsområden pga dess värmetålighet och isolerande förmåga. PCB har t ex använts i kondensatorer, transformatorer, värmeväxlare, fogmassor i hus och i färger. Sedan 1970-talet har användning av PCB varit förbjuden i Sverige. Referens = Livsmedelsverket [chemfile(), file(), referens i dokument] Dioxiner i stålindustrin Dioxiner kan bildas vid skrotsmältning i stålverk och en mindre del bildas vid torrdetillation av stenkol till koks i koksverk. De dioxiner som bildas binds i hög grad till stoft och mängden från stålverk påverkas bl a av hur processerna styrs. Dioxiner som bildas vid skrotsmältning beror på att skrotet kan innehålla klorhaltigt plast, t ex PVC (polyvinylklorid) eller annat material som innehåller klor eller PCB. Referens = SSAB Luleå [chemfile(), file(), referens i dokument] Hälsorisker med dioxin och dioxinlika PCB I olika typer av studier av djur och människa misstänks dioxiner och PCB kunna påverka reproduktionen (fortplantningen), immunförsvarets funktion, utvecklingen av centrala nervsystemet (hjärnan), samt orsaka cancer. Stabila och fettlösliga Dioxiner och PCB är stabila och fettlösliga föreningar som är svåra att bryta ner. De finns därför kvar i miljön och i kroppen under lång tid. Egenskaperna gör också att dessa ämnen anrikas i näringskedjorna, vilket innebär att de högsta halterna återfinns i bl a rovfiskar från förorenade områden. Fettlösligheten gör att dioxiner och PCB ansamlas i fettvävnaden hos djur och människor. Referens = Livsmedelsverket [chemfile(), file(), referens i dokument] [chemfile(), nC=0 nr=dioxin2, f1=/produkt/info/html/dioxin2.htm] Dioxinekvivalenter (TEQ) För att kunna bedöma den totalt effekten av alla dioxinlika ämnen används ofta ett ekvivaleringsverktyg där den samlade halten av dioxiner och dioxinlika PCB uttrycks i TCDD-ekvivalenter (TEQ). Det är de 17 särskilt toxiska (giftiga) dioxinerna som brukar räknas samman som ett viktat medelvärde, till mängd toxiska ekvivalenter (TEQ). Detta innebär att giftigheten hos de olika dioxin- och PCB-kongenerna sätts i relation till TCDDs giftighet. Om en kongen är hälften så giftig som TCDD, får den toxicitetsekvivalentfaktorn (TEF) 0,5. Genom att multiplicera koncentrationen för varje enskild kongen med dess TEF och därefter summera erhålls den totala halten av TCDD-ekvivaler (TEQ). Utgångspunkten för TEQ-systemet är att samtliga dioxiner och dioxinlika PCB verkar via samma mekanism, via den sk dioxin- eller Ah-receptorn, i kroppen och ger upphov till samma effekter. Effekterna anses vara additiva, dvs kan slås ihop. Den senaste översynen av TEF gjordes under 2006 i WHO:s regi (van den Berg et al 2006). Världshälsoorganisationen (WHO) är ett specialiserat organ inom Förenta nationerna (FN) som handlar om internationell folkhälsa. Dioxiner och PCB i maten Människor får i sig mest dioxiner och PCB via maten. Ämnena är fettlösliga och finns främst i feta animaliska livsmedel som fisk, kött och mejeriprodukter. Särskilt höga halter finns i fet fisk som strömming och vildfångad lax från förorenade områden, t ex Östersjön, Bottniska viken, Vänern och Vättern. Referens = Livsmedelsverket [chemfile(), file(), referens i dokument]
Koksgaskondensat är kondensat som samlas upp i vattenlås vid distribution av koksgas i ledningar. Kondensatet innehåller ammoniak, svavelväte, cyanider, fenoler och bensen i arbetshygieniskt betydelsefulla halter. Referens = SSAB Luleå [chemfile(), chemdata.dat, referens i dokument]
Metallröksfeber Metallröksfeber (metallfrossa) är influensaliknande besvär som kan uppstå efter inandning av metallrök och metallångor. Tillståndet karaktäriseras av metallsmak i munnen, irritation i luftvägarna, hosta, feber, trötthet och värk i leder och muskler. Besvären går som regel över inom något eller några dygn. Inandning av zinkoxid (zinkfrossa) är en vanlig orsak till metallröksfeber men rök och ångor från andra metaller, t ex koppar, kadmium, magnesium, mangan och nickel, kan ge samma symptom. Zinkoxid Vid upphettning av zink bildas zinkoxid. Typiskt sker detta vid svetsning av galvaniserad plåt. Inandning av röken ger metallröksfeber, som också kallas svetsarfrossa eller zinkfrossa. Tillståndet är vanligt bland svetsare. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument]
Nitrösa gaser Nitrösa gaser, kväveoxider NOx, är en blandning av flera olika kemiska föreningar mellan kväve och syre. De viktigaste är kväveoxid och kvävedioxid. Vid mätning av nitrösa gaser brukar summahalten av kväveoxid och kvävedioxid bestämmas. Nitrösa gaser är ibland färglösa, ibland gulaktiga (kväveoxid är färglös, kvävedioxid är gulbrun. Nitrösa gaser bildas ur luftens kväve och syre vid all slags förbränning. De utgör en viktig beståndsdel i motoravgaser, främst dieselavgaser. Nitrösa gasr utgör också ett vanligt arbetsmiljöproblem vid svetsning, skärbränning. Nitrösa gaser (främst kvävedioxid) påverkar lungorna redan vid låga halter. Lungfunktionen försämras och motståndskraften mot infektioner i lungorna minskas. Astmatiker förefaller att vara särskilt känsliga för effekterna på lungorna av nitrösa gaser Höga halter ger upphov till livshotande lungödem. Nitrösa gaser (främst kväveoxid) försämrar hämoglobinernas syretransporteande förmåga genom bildning av methemoglobin. Cancerframkallande nitrosaminer kan bildas genom en kemisk reaktion mellan nitrösa gaser och aminer. Aminer är en grupp ämnen som bl a bildas genom nedbrytning av kroppens proteiner. Utsläpp av nitrösa gaser till den yttre miljön bidrar till såväl försurning som övergödning. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument]
Polyaromatiska kolväten Polycykliska aromatiska kolväten, även polyaromatiska kolväten eller polyaromater, ofta förkortat PAH av engelska Polycyclic Aromatic Hydrocarbons, är en grupp ämnen som finns i stenkol och petroleum (råolja) samt bildas vid förbränning av organiskt material. Det mest kända av dessa ämnen är benso(a)pyren. Flera av PAH-ämnena är cancerframkallande, t ex benso(a)pyren. PAH-ämnen är inte flyktiga men de sprids över stora områden med partiklar. Exponering för PAH-ämnen kan medföra en ökad risk för cancer. Olika råoljeraffineringsprocesser bidrar till att koncentrationen PAH ökar i vissa slutprodukter. Det är således mycket PAH i bl a tung eldningsolja. Polyaromater förekommer också i sot, beck, asfalt, kreosot och mineraloljor. Nya oljor som är raffinerade innehåller jämförelsevis låga halter, men efter en tids användning kan halten öka drastiskt, t ex i motoroljor och hydrauloljor som varit utsatta för höga temperaturer. Mätning Enligt Arbetsmiljöverkets föreskrifter om hygieniska gränsvärden, bedöms halten polyaromater i luft utifrån mätning av halten benso(a)pyren. Det bör dock observera att benso(a)pyren bara svarar för en liten och varierande andel av den cancerframkallande effekten hos polyaromaterna. Hälsorisker Långvarig eller upprepad hudkontakt med polyaromater i t ex stenkolstjära eller använda oljor kan ge upphov till hudcancer. Inandning av polyaromater, i gasform eller de som har fastnat på partiklar, kan ge upphov till lungcancer. Yttre miljö Benso(a)pyren är bioackumulerande och svårnedbrytbart. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument] Koksverk, PAH-ämnen vid tillverkning av koks från kol Vid tillverkning av koks från kol i ett koksbatteri bildas koksgas och den orenade processgasen innehåller hög halt PAH. På koksbatteriet förekommer arbeten där luckor måste öppnas för att fylla på kol och det förekommer läckage av orenad processgas. Därför finns det risk för exponering för PAH i gasform men även för PAH som har fastnat på partiklar. PAH-ämnen har relativt låg flyktighet, vilket innebär att de inte håller sig luftburen särskilt länge utan fastnar på partiklar. Den största förekomsten av polyaromater finns i stenkolstjära, som är en biprodukt vid tillverkning av koks från kol. Risk för exponering för höga halter PAH finns på arbetsplatser där stenkolstjära tillverkas eller hanteras. PAH-ämnen i begagnade oljor och smörjfetter Begagnade oljor (t ex motoroljor, hydrauloljor) och smörjfetter som varit utsatta för höga temperaturer kan innehålla höga halter PAH som bildats vid användningen. Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
Syntetiska oorganiska fibrer Tillverkade oorganiska fibrer kallas för syntetiskt oorganiska fibrer, för att skilja dem från naturliga oorganiska fibrer. Fibrer Partiklar med ett längdbreddförhållande, som är större än 3:1. Respirabla fibrer Fibrer med en diameter <0,003 mm, Mikrofibrer Fibrer med diameter <0,001 mm, Mineralullsfibrer Ingår i fibermaterial som används för isolering av t ex byggnader och även för ljudisolering. Syntetiska glasartade fibrer vars totala innehåll av oxiderna (Na2O+K2O+CaO+MgO+BaO)>18 vikt%. Eldfasta keramiska fibrer (RCF) Ingår i fibermaterial som används för högtemperaturisolering i stålindustrin. RCF = Refractory Ceramic Fibres, syntetiska glasartade fibrer vars totala innehåll av oxiderna (Na2O+K2O+CaO+MgO+BaO)<=18 vikt%. Referens = Arbetsmiljöverkets föreskrifter [chemfile(), file(), referens i dokument]
En syra definieras som ett ämne som kan avge protoner (eller vätejoner) (pH <7). Många ämnen har förmågan att kunna avge protoner, men i större eller mindre utsträckning. Syror delas därför in i olika grupper beroende på hur många protoner de kan avge i en lösning (oftast iakttaget i vattenlösning). Citronsyran har inte så stor benägenhet att avge protoner och kan därför ses som en svag syra, medan saltsyra avger alla sina protoner och ses då som en stark syra. Det finns även syror som kan betecknas som medelstarka syror, t ex fosforsyra. Syrors styrka anges av en syrakonstant, en form av jämviktskonstant. En syra kan tillsammans med en korresponderande bas bilda ett buffertsystem. Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), chemdata.dat, referens i dokument] [chemfile(), nC=0 nr=acid, f1=/produkt/info/html/acid.htm]
Syror är kemiska ämnen som innehåller väte och i deras vattenlösningar finns oxoniumjoner H3O+. När en syra reagerar med vatten övergår väte från syran i form av vätejoner (H+) till vattenmolekyler (H2O) och det bildas oxoniumjoner (H3O+). Det är oxoniumjonenerna som ger vattenlösningar av syror deras sura egenskaper och den sura lösningen kallas för Syror reagerar med många sk oädla metaller och det bildas Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), file(), referens i dokument] I reaktionen mellan väteklorid (HCl) och vatten lämnar protonen (vätejonen H+) HCl-molekylen och binds istället vid ett av de fria elektronparen i H2O-molekylen som blir en oxoniumjon (H3O+). Väteatomens elektron stannar kvar hos kloratomen som blir en kloridjon (Cl-). Oxoiumjoner (H3O+) och kloridjoner (Cl-) gör att lösningen kan leda elektrisk ström. Referens = Gymnasiekemi A, utgiven av Liber [chemfile(), file(), referens i dokument] 
Ämne som består av molekyler eller joner som kan avge en proton (ev flera protoner) kallas Det bildas När väteklorid (HCl) löses i vatten avger praktiskt taget alla vätekloridmolekyler (HCl) sina protoner (vätejoner). Lösningen kallas Referens = Gymnasiekemi A, utgiven av Liber [chemfile(), file(), referens i dokument] Starka och svaga syror En syra är ett ämne som genom dissociation 1) kan avge protoner (vätejoner). En syra har pH-värde lägre än 7. Syror delas in i starka och svaga syror, beroende på i hur hög grad de dissocieras.
Den korresponderande basen till en syra är den bas som uppkommer när en syra protolyserats (avger en vätejon) och den korresponderande syran till en bas är den syra som uppkommer när en bas tar upp en vätejon. Syran är saltsyra (HCl), och när en vätejon lämnat molekylen kvarstår en kloridjon (Cl-), kloridjonen är den korresponderande basen till saltsyra. Ammoniak (NH3) är en bas och vill dra åt sig en vätejon, och när den gjort det har den bildat en ammoniumjon (NH4+), ammoniumjonen är den korresponderande syran till ammoniak. Om en syra är stark eller svag beror på hur många vätejoner som syran avger då den löses i vatten. I en stark syra frigör nästan alla syramolekyler vätejoner. I en svag syra frigör kanske bara 1/10 av syramolekylerna vätejoner. T ex citronsyra har inte så stor benägenhet att avge protoner (vätejoner) och betecknas därför som en svag syra, medan saltsyra avger alla sina protoner och betecknas därför som en stark syra. Koncentrerade och utspädda syror Koncentrationen av syra beror på hur mycket vatten den löses i. Om mycket syra löses i lite vatten, blir syran koncentrerad. Om lite syra löses i mycket vatten, blir syran utspädd. Både starka och svaga syror kan vara koncenterade eller utspädda. 
Referens = Kemi Direkt, Gidhagen, Åberg [chemfile(), file(), referens i dokument] Saltsyra, HCL (aq) Då väteklorid (HCl) löses i vatten, bildas saltsyra HCl (aq). Om så mycket väteklorid som möjligt löses i vatten, bildas koncentrerad saltsyra. Den innehåller ca 37% väteklorid (HCl). Salpetersyra, HNO3 Salpetersyra är en färglös frätande vätska, som protolyseras 1) fullständigt i vatten. 1) [chemfile(), nC=0 nr=fdiv, f1=/produkt/info/html/fdiv.htm]
Då mycket utspädd salpetersyra reagera med vatten bildas vätgas. Utspädd salpetersyra och koncentrerad salpetersyra reagerar med de flesta metaller, då bildas giftiga nitrösa gaser kväveoxid (NO) och rödbrun kvävedioxid (NO2). Koncentrerad salpetersyra bör förvaras i mörka glasflaskor. Syran sönderfaller under inverkan av ljus och det bildas kvävedioxid (NO) som färgar syran gul. Svavelsyra, H2SO4 Svavelsyra är en färg- och luktlös vätska, i koncentrerad form är den tung och tjockflytande. En svavelsyramolekyl kan avge två protoner, den är tvåprotonig. Vid reaktion med vatten sker protolysen med i två steg. I det första steget är protolysen fullständig medan i det andra steget endast en del av vätesulfatjonerna protolyseras.
svavelsyra + vatten -> oxoniumjon + vätesulfatjon H2SO4(l) + H2O -> H3O+(aq) + HSO4-(aq) Protolys 2 vätesulfatjon + vatten -> oxoniumjon + sulfatjon HSO4- + H2O -> H3O+(aq) + SO42-(aq) Då koncentrerad svavelsyra och vatten blandas utvecklas värme. Värmeutvecklingen kan bli så stor att kokpunkten för vatten överskrids. Därför måste försiktighet iaktagas vid utspädning av koncentrerad svaelsyra. Regeln är att syran ska hällas i vatten och inte tvärtom. Syran som har högre densitet än vatten sjunker då ner och blandas med vatten. Om vatten hälls i koncentrerad svavelsyra, är det risk att blandningen stänker. Kolsyra, H2CO3 När koldioxid (CO2) leds i vatten bildas en sur lösning som kallas kolsyra. Det är en tvåprotonig syra som protolyseras i två steg.
CO2(g) + H2O -> H2CO3(aq) Protolys 1 kolsyra + vatten -> oxoniumjon + vätekarbonatjon H2CO3(aq) + H2O -> H2O+(aq) + HCO3-(aq) Protolys 2 vätekarbonatjon + vatten -> oxoniumjon + karbonatjon HCO3-(aq)+ + H2O -> H3O+ + CO32-(aq) Starka och svaga syror Koncentrerade syror Skilj mellan begreppen stark och koncenrerad. Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), file(), referens i dokument]
Vätejoner är av grundläggande betydelse vid beskrivning av syror. En vätejon är en jon som består av en positivt eller negativt laddad väteatom. Väteatomen består av en proton och en elektron. En positiv vätejon (H+) är en väteatom där elektronen saknas och består endast av en proton. En negativ vätejon (H-) har två elektroner och kallas för hydridjon. I praktiken bildas vätejoner bl a vid upplösning av syror eller sura salter i protiska lösningsmedel (lösningsmedel som har väte som är bundet till kväve eller syre t ex vatten). Vätejoner kan dock ej existera någon längre tid i fritt tillstånd utan binds snabbt, solvatiseras, till lösningsmedlet, som då fungerar som en bas. I vatten bildas snabbt sk oxoniumjoner (H3O+). Koncentrationer av vätejoner i en lösning brukar användas som mått på dess aciditet eller surhetsgrad, ju högre koncentration desto surare lösning. Eftersom vätejoner inte i någon högre grad kan existera fria som sådana i lösning är den egentliga koncentrationen svår att bestämma. I stället mäts den sk Att vätejoner bara består av en proton gör dem väldigt reaktiva. Vätejoner bildas då det finns vissa ämnen (syror) som har förmågan att avge vätejoner, och om det samtidigt finns andra ämne (baser) som omedelbart kan ta upp den igen. Syror Defintionen av Det som händer när en vätejon avges, är att väteatomen lämnar molekylen utan att ta med sig sin elektron, vilket får vätet att bli en positivt laddad vätejon, medan kloret, som plötsligt har ett överskott på en elektron, blir en negativt laddad kloridjon. 
Vätejoner är reaktiva och existerar inte fritt någon längre stund. För att de inte ska hoppa tillbaka till kloridjonerna måste det finnas något annat ämne som kan ta upp dem i närheten. Ett typiskt sådant ämne är vatten. Om väteklorid löses i vatten sker en reaktion enligt den här modellen. 
Vätejonen fäster på vattenmolekylen och bildar vad man kallar för en Principen är exakt den samma för syror som löses i vatten. De ger bort en vätejon till vattenmolekylerna, som blir till oxoniumjoner, och bildar själva en negativt laddad jon, en sk syrarest. Ett annat exempel på en syra är ättiksyra, som ger ättika dess sura smak. Det är en lite större molekyl än väteklorid, men principen är densamma. När det kommer vattenmolekyler i närheten av en ättiksyramolekyl kan en vätejon lossna från syramolekylen och i stället fästa på vattenmolekylen. Det bildas en positivt laddad oxoniumjon och en negativt laddad ättiksyrarest. 
Oxoniumjonerna (H3O+) är mycket stabilare än helt fria vätejoner (H+), men är fortfarande väldigt reaktiva. Får de möjlighet att avge sina extra vätejoner till andra molekyler kommer de mer än gärna ta den möjligheten. Detta är det som ligger bakom de speciella, kemiska egenskaperna hos vattenlösningar av syror. Syrors egenskaper Syror kan ge mat sur smak och det är genom att oxoniumjoner kan ta sig in i smakcellerna och där få andra positiva joner att flytta på sig, vilket ger upphov till nervsignaler som hjärnan sedan i sin tur tolkar som sur smak. Syror kan vara frätande och skada naturen. Även det har med oxoniumjonerna att göra. Bl a kan de byta ut andra positivt laddade joner som sitter fast i marken och som exempelvis kan vara gifitiga tungmetalljoner. Att syrorna är frätande beror på att det i kroppen finns ämnen som är mer benägna att ta upp vätejoner än vatten. Spill av syralösning på t ex händer innebär att just sådana ämnen tar upp vätejoner och därmed får ändrad struktur och funktion. Eftersom molekylerna inte länge fungerar som de ska uppkommer en skada och kroppen varnar genom att skicka smärtsignaler när det blir för mycket oxoniumjoner på samma ställe. Surhetsgraden Det är ofta intressant att veta hur stor koncentration oxoniumjoner, dvs hur många oxoniumjoner per liter, det finns i en lösning. Medan en lösning med låg koncentration oxoniumjoner på sin höjd kanske smakar surt, kan en lösning med hög koncentration vara mycket frätande. Ju högre koncentrationen av oxoniumjoner är, desto surare är lösningen. I artikeln om pH-värde berättar vi mer om hur man mäter hur sur en lösning är. Men just nu ska vi i stället reda ut vad som påverkar hur sur en lösning blir. En sak som är lätt att inse direkt, är att det spelar roll hur många syramolekyler vi har löst upp i varje liter lösning, det vill säga hur stor koncentrationen av själva syran är. Många syramolekyler kommer ju naturligtvis att ge många oxoniumjoner. 
Vissa syror är Andra syror, som t ex 
Vanliga syror Referens = naturvetenskap.org [chemfile(), file(), referens i dokument]
Fluorvätesyra kan bildas i stålindustrin då gjutpulver, som innehåller kalciumforid (CaF2) doseras i kokill. Då gjutpulver, som innehåller flusspat, doseras i kokill bildas fluorgas som reagerar med luftens fuktighet till vätefluorid. Då vätefluorid kommer i kontakt med fuktig hud eller slemhinnor bildas fluorvätesyra. Ångor av fluorväte och fluorvätesyra verkar i låga halter irriterande och i höga halter frätande på andningsvägar, ögon och hud. Fluorväte och fluorvätesyra tas upp i kroppen både genom hud och vid inandning. Vid samtidig förekomsta av damm i luften kan fluorväte ge upphov till astmaliknande symptom. Förmodligenn gör dammpartiklarna det möjligt för fluorväte att tränga djupare ned i lungorna.
Fosforsyra är färglös och förekommer vanligen som vattenlösning. Koncentrerad fosforsyra (över 85%) är vid rumstemperatur ett fast ämne. Dimma av fosforsyra verkar frätande på andningsvägar, ögon, hud och tänder. Stänk på huden och ögon kan förorsaka svårläkta sår, och måste omedelbart spolas bort med vatten. Inandning av lägre halter under lång tid kan ge frätskador på tänderna. Vid upphetning av fosforsyra bildas fosforoxider. Vid kontakt med metaller bildas den giftiga gasen fosforväte (fosfin) och vätgas. Vätgas bildar med luft blandingar som vid antändning kan explodera. Referens = Litteratur om kemiska hälsorisker [chemfile(), file(), referens i dokument]
Salpetersyra är en gulaktig, starkt frätande vätska med stickand lukt. Vid koncentrationer över 70% är den rödrykande, dvs avger gulbruna eller rödbruna ångor som består av nitrösa gaser (kväveföreningar). Även mer utspädd salpetersyra avger nitrösa gaser vid uppvärmning, i solljus, i fuktig luft eller vid kontakt med en del metaller. Vid hantering av salpetersyra kan det uppstå dels syra ånga, dels nitrösa gaser. Syraångorna verkar irriterande och frätande på andningsvägar, ögon, hud och tänder. Nitrösa gaser kan i höga koncentrationer ge upphov till livshotande lungskador (lungödem). Stänk i ögonen kan ge allvarliga ögonskador. Stänk av salpetersyra ger upphov till svårläkta frätsår samt till gulfärgningar av huden. Förtäring av redan små mängder kan ge inre frätskador. Salpetersyra är i sig själv inte brännbar. Däremot kan många organiska ämnen, som trä, papper och tyg samt många organiska lösningsmedel antändas vid kontakt med salpetersyra.
Saltsyra (klorvätesyra, HCl) är en färglös eller gulaktig, starkt frätande vätska. Koncentrerad syra är rykande och avger frätande ångor som består av klorväte (HCl). Vätskan och ångorna förorsakar kraftig rostangrepp på metaller. Stänk av saltsyra ger frätskador på ögon och hud. Hudskadorna yttrar sig som sveda, rodnad, blåsor och sår. Saltsyraångor verkar irriterande och frätande på andningsvägar, ögon och hud. Högre halter kan förorsaka livshotande lungödem. Inandning under längre tid kan ge frätskador på tänderna. Vid kontakt mellan saltsyra och de flesta metaller bildas vätgas, som ger exploiva blandningar med luft.
Svavelsyra (H2SO4) är en starkt frätande vätska. Ren syra är luktlös och färglös eller svagt gul. Förorenad syra kan vara brun. Svavelsyra angriper och förstör de flesta material. Vid kontakt med många kemiska ämnen bildas giftiga och brandfarliga ämnen. T ex varm koncentrerad syra är oxiderande och bildar svaveldioxid i kontakt med metaller. Dimma av svavelsyra verkar starkt irriterande och frätande på andningsvägar, ögon och hud. Mycket höga halter kan ge livshotande lungödem. Långvarig inandning av svavelsyradimma kan ge svåra frätskador på tänderna. Stänk på huden ger svårläkta frätsår. Stänk i ögonen kan ge svåra ögonskador med bestående synnedsättning, även risk för blindhet. Vid uppvärmning av svavelsyra avges syradimma och svaeltrioxid (frätande). Svavelsyra reagerar häftigt med vatten under stark värmeutveckling. Spädning måste ske genom att syran hälls i vatten, och inte tvärtom.
SSAB I koksverket vid SSAB i Luleå finns en gasbehandlingsanläggning med en serie olika processer där rågasen från torrdestillationen av kol till koks renas i flera steg och där utvinns Stenkolstjära Stenkolstjära från rågasen separeas i förlaget genom att kyla gasen, i kylaren med ammoniakvatten och resten i elektrofilter. Från kylaren leds kondensatvatten till kondensatbehandlingen där tjära och beck separeras 1). Stenkolstjära och beck är hälsofarliga och de är även starkt hud- och ögonirriterande. Hudkontakt i kombination med solexponering kan ge svårartade eksem. 1)
Tjära / beck Tjära är en trögflytande vätska som erhålls som kondensat vid pyrolys (torrdestillation) av organiska material som kol och petroleum, tjära som bildas från kol kallas för Det finns risk för hudcancer och överkänslighet för solljus (fototoxiskt eksem) efter långvarig direktkontakt med tjära/beck. Eksem av typ fototoxiskt uppstår då huden utsätts för solljus. Polyaromatiska kolväten, polycykliska aromatiska kolväten eller polyaromater, ofta förkortat PAH av engelska Polycyclic Aromatic Hydrocarbons, är en grupp ämnen som finns i stenkol och petroleum (råolja). Det mest kända av dessa ämnen är benso(a)pyren. Flera av PAH-ämnena är cancerframkallande, t ex benso(a)pyren. Dessa ämnen har dessutom obehaglig lukt redan vid låga koncentrationer. PAH-ämnen är inte flyktiga men de sprids över stora områden med partiklar. Tjära och beck innehåller polyaromatiska kolväten (PAH). Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument] Referens = SSAB Luleå [chemfile(), file(), referens i dokument] Råbensen I naftalentvätten absorberas naftalen, bensen, toluen och xylen från gasen i processolja. I bensentvätten absorberas bensen, xylen och toluen från gasen i processolja. Processoljan leds till bensenanläggningen för utvinning av råbensen (bensen, xylen, toluen). Referens = SSAB Luleå [chemfile(), file(), referens i dokument] [chemfile(), nC=0 nr=452-b, f1=/produkt/info/html/452-b.htm] Rågas, koksgas Vid koksningen, som är en torrdestillation utan lufttillförsel, avdrivs flyktiga ämnen i kolet som gas, sk Rågasen renas i flera steg. Den renade rågasen ( Koksningsprocessen Vid koksningsprocessen avger kolet sina flyktiga beståndsdelar i form av rågas, med följer även vattenångan från fukten i kolet. Den största delen av rågasen består av vätgas och metangas, men den innehåller även ämnen som bensen, svavel, tjära samt en mängd olika kolväteföreningar t ex cyanider. Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
Råbensen är en flyktig organisk vätska extraherad från gasen som utvecklas vid torrdestillation av kol. Består främst av bensen (>70%), toluen (10-15%) och xylen (2-5%), kan innehålla andra kolväten i låga halter. Bensen kan ge cancer (leukemi) och finns tillsammans med 95 andra ämnen i den högsta cancerriskklassen. Klassningen är gjord av International Agency for Research on Cancer (IARC). Bensen tas lätt upp i kroppen, både vid inandning av gas och ångor samt vid hudkontakt med lösning, och förs sedan snabbt vidare till alla kroppens vävnader framförallt till fettvävnaden. Vid exponering för ämnet i höga doser påverkar bensen det centrala nervsystemet. Vid långvarig och upprepad inandning av bensen finns risk för anemi 1) och ökad infektionskänslighet. 1)
Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
Tjära / beck Tjära är en trögflytande vätska som erhålls som kondensat vid pyrolys (torrdestillation) av organiska material som kol och petroleum, tjära som bildas från kol kallas för Det finns risk för hudcancer och överkänslighet för solljus (fototoxiskt eksem) efter långvarig direktkontakt med tjära/beck. Eksem av typ fototoxiskt uppstår då huden utsätts för solljus. Polyaromatiska kolväten, polycykliska aromatiska kolväten eller polyaromater, ofta förkortat PAH av engelska Polycyclic Aromatic Hydrocarbons, är en grupp ämnen som finns i stenkol och petroleum (råolja). Det mest kända av dessa ämnen är benso(a)pyren. Flera av PAH-ämnena är cancerframkallande, t ex benso(a)pyren. Dessa ämnen har dessutom obehaglig lukt redan vid låga koncentrationer. PAH-ämnen är inte flyktiga men de sprids över stora områden med partiklar. Tjära och beck innehåller polyaromatiska kolväten (PAH). Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument] Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
SSAB I processen har 1/4 av kolet övergått i gasform som renas i gasbehandlingsprocessen. I svaveltvätten besprutas gasen med ammoniakhaltigt vatten. Tvättvätskan från svaveltvätten förs till destillationskolonner. Där frigörs svavelväte och ammoniak genom uppvärmning med ånga. Både ammoniakångorna och svavelväteångorna förs vidare till den sk spaltugnen. Där spaltas ammoniakgasen katalytiskt upp i sina grundämnen, kväve (N) och väte (H). Referens = SSAB Luleå [chemfile(), file(), referens i dokument] Svavel [chemfile(), nC=0 nr=H2S-452, f1=/produkt/info/html/H2S-452.htm] Gasen efter naftalentvätten förs vidare till en svaveltvätt. Det är en absorbtionskolonn och där besprutas gasen med ammoniakvatten från ammoniaktvätten. Den renade gasen, efter svaveltvätten, förs upp genom toppen av kolonnen till ammoniaktvätten. Även där besprutas gasen med ammoniakvatten, som löser ammoniak i gasen. Det är det vatten som sedan används som tvättvätska i svaveltvätten. Tvättvätskan från svaveltvätten förs till destillationskolonner, sk avsyrare och avdrivare. Där frigörs svavelväte och ammoniak genom uppvärmning med ånga. I avdrivare förångas ammoniak och i avsyrare förångas svavelväte. Vattnet efter destillationskolonnerna återförs till ammoniaktvätten och cirkulerar mellan ammoniaktvätten, svaveltvätten, avsyrare och avdrivare i ett kretslopp. Ammoniakångorna (NH3)och svavelväteångorna (H2S) förs vidare till spaltugnen där spaltas ammoniakångorna till grundämnena kväve (N) och väte (H). I den efterföljande sk Clausanläggningen omvandlas svavelväte (H2S) till svavel (S) och här framställs flytande svavel för försäljning. Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
Svavel Svavel är ett grundämne som vid rumstemperatur är ett gult fast ämne. Vid antändning av svavel bildas giftig gas (svaveldioxid). Blandningar mellan luft och svaveldamm är explosiva. Inandning av svaveldamm ger upphov till inflammation i näshålan och till lungskador (emfysem 1)) med försämrad lunfunktion som följd. Hudkontakt med svavel kan orsaka irritation och svaveldamm kan ge upphov till ögonskador. 1)
Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), chemdata.dat, referens i dokument] Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), chemdata.dat, referens i dokument] Produktion svavel Svavel erhålls som en biprodukt från koksgas i koksverk vid tillverkning av koks från kol. Referens = SSAB Luleå [chemfile(), chemdata.dat, referens i dokument]
Svavelväte, vätesulfid (H2S), är en kemisk förening av svavel och väte. Det är en giftig gas med en lukt som påminner om ruttna ägg. I höga koncentrationer kan gasen förorsaka snabbt medvetslöshet och vara livshotande. I koncentrationer över 150 ppm 1) bedövas luktsinnet och då fungerar inte längre lukten som varningssignal. Vid lägre koncentrationer av svavelväte visar sig verkningarna i form av trötthet och irritation i luftvägarna. Vid halter om ca 50-100 ppm 1) uppstår svår ögonirritation, ofta med synrubbningar. Med stigande halter påverkas hjärnan och nervsysyemet allt mer. Luktsinnet förlamas, omdömesförmågan minskar, balansförmågan försämras. Det kan också uppstå livshotande lungskador (lungödem). Vid mycket höga halter uppstår snabbt medvetslöshet. Hos den som en längre tid varit utsatt för svaveläväte kan det förekomma symptom som slemhinneirritation, huvudvärk, trötthet, irritation och sömnlöshet. 1)
ppm (parts per million) är en förkortning för miljondel på samma sätt som procent för hundradel och promille för tusendel. För att omvandla lufthalter av gaser och ångor mellan ppm och mg/m3 går det att räkna ut ett omvandlingstal genom att dividera ämnets molekylvikt med 24. T ex är molekylvikten 97 för diklormetylen (C2H2Cl2) och omvandlingstalet är då 4,0. För att omvandla från ppm till mg/m3 multipliceras ppm med omvandlingstalet. T ex är 20 ppm diklormetylen 20*4=80 mg/m3. För att omvandla från mg/m3 till ppm ska mg/m3 divideras med omvandlingstalet. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument] Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument]
Svaveldioxid (SO2) är en färglös gas med stickande lukt. Om gasen löses i vatten bildas svavelsyrlighet, som är en färglös och frätande syra, som är svagare än svavelsyra. Då svaveldioxid kommer i kontakt med fuktigheten i ögon och andningsvägarnas slemhinnor bildas svavelsyrlighet, som är starkt irriterande och frätande. Svaveldioxid som sugits upp i kläderna och förenats med vatten fräter på huden. Vid inandning påverkar svaveldioxid luftvägarna redan vid relativt låga halter, t ex ökar andningsmotståndet i luftvägarna. Astmatiker är särskilt känsliga för svaveldioxid. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument]
Brunkol Kol har bildats från vegetationsrester som ansamlats i våtmarker. Rörelser i jordskorpan utsatte växtrester för högt tryck och hög temperatur. Detta har genom årmiljonerna fysikaliskt och kemiskt successivt omvandlat växtresterna till kol av olika kvaliteter. Först har torv omvandlats till brunkol. Brunkol har en låg organisk omvandlingsgrad och därmed lågt energiinnehåll. I jämförelse med andra kolsorter är brunkol ofta mjukt och färgen kan variera från svart till olika nyanser av brunt. Sub-bituminöst kol De fortsatta effekterna av tryck och temperatur har lett till att det lågvärdiga kolet efter hand har kommit att nå en högre omvandlingsgrad och därvid omvandlats till vad som brukar kallas sub-bituminöst kol. Stenkol Under ytterligare process har sedan det hårdare Antracit Huvuddelen av stenkolet benämns ofta bituminöst kol, men det allra mest omvandlade och därmed mest högvärdiga kolet går under benämningen antracit. Bergarten antracit bildas av stenkol som utsätts för högt tryck och hög temperatur. Den är det näst sista stadiet i inkolningskedjan från torv till grafit. Antracit är en typ av bergart och det högsta metamorfiska stadiet 1) av kol. Antracit är hårt och har en hög kolhalt, över 91%. 1)
Stenkol är en form av den sedimentära bergarten kol 1) och innehåller 84-91% kol 2) med amorft kol i varierande halt och lite antracit. Resten är väte, syre, kväve, svavel och andra ämnen. Bergarten kol består till största delen av omvandlade växtdelar. Beroende på vilka växter som fanns under aktuell kolbildningsperiod och på hur omvandlingen gått till, får de olika slagen av bergarter varierande karaktär och kvalitet. Stenkol, antracit och en del andra bergarter innehåller amorft kol i varierande halter. 1)
Beroende på hur hög kolhalten är, dvs i hur hög grad växtresterna omvandlats, delas kol som bergart in i olika grupper, i denna sk inkolningsserie ingår bl a - Torv (65-84% kol) 2) - Stenkol, butiminöst kol (84-91% kol) 2) - Antracit (över 91% kol) 2) - Grafit Torv är ett förstadium till brunkol och innehåller 65-84% kol. 2) Stenkol är ett mellanläge i omvandligen från brunkol till antracit och innehåller 84-91% kol. 2) Antracit är det näst sista stadiet i inkolningskedjan från torv till grafit och innehåller över 91% kol. 2) Vid torrdestillation av stenkol till koks övergår 25% av stenkolet i gas och den fasta återstoden kallas koks. 2)
SSAB Koks tillverkas i koksverk genom torrdestillation av stenkol. Torrdestillation eller pyrolys är en process där ett ämne upphettas till en hög temperatur, i en syrefri miljö, så att det sönderfaller utan att förbränning sker. Vid torrdestillation av stenkol avgår flyktiga ämnen från kolet i gasform, medan en fast återstod som kallas för Gaserna som avgår från kolet kallas för rågas och innehåller samma föroreningar och flyktiga ämnen som kolet innehåller. I gasreningsanläggningen kyls rågasen och då utkondenseras tjära och vatten som lagras i kondensatbehandlingen. Vätskan sedimenterar och det tyngsta (beck) faller till botten och det lättaste (tjäran) hamnar överst. Den avskilda tjäran lagras och säljs till kemisk industri. Beck återförs till kollagret. Det renade vattnet, dvs gaskondensatet, återförs till förlaget för kylning av rågasen. Öveskottet mellanlagras i en ammoniakvattentank. Referens = SSAB Luleå [chemfile(), chemdata.dat, referens i dokument] [chemfile(), nC=0 nr=koks, f1=/produkt/info/html/koks.htm]
Koksgaskondensat är kondensat som samlas upp i vattenlås vid distribution av koksgas i ledningar. Kondensatet innehåller ammoniak, svavelväte, cyanider, fenoler och bensen i arbetshygieniskt betydelsefulla halter. Referens = SSAB Luleå [chemfile(), chemdata.dat, referens i dokument]
Cyanider Cyanider och cyanföreningar är kemiska föreningar i vilka ingår en cyangrupp (kväve bundet till kol, CN). Cyanider är mycket giftiga vid såväl inandning som hudkontakt och kan orsaka huvudvärk, yrsel, öronsusningar, andnöd, illamående, kräkningar. Höga halter orsakar snabbt oregelbunden puls, andningsstillestånd, kramper och medvetslöshet. Cyanider kan vid uppvärmning bilda den mycket giftiga gasen Risk för att vätecyanid bildas vid exponering för cyanider Vätecyanid kan bildas genom hydrolys av cyanid, t ex då ångor av cyanider inandas och cyaniderna hydrolyseras till vätecyanid t ex i kontakt med slem. Hydrolys är en kemisk process där en molekyl klyvs i kontakt med vatten, t ex vid hydrolys av cyanider då frigörs den farliga cyanidjonen (CN) och då finns risk att vätecyanid bildas. Vid nedsväljning av cyanider i vätska, ångor eller partiklar som är kontaminerade med cyanider kan cyanider reagerar med magens saltsyra till Förgiftning Vätecyanid inaktiverar cellandningen genom att binda till järnet i ett protein i cellen som kallas för cytokrom C. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument]
Masugnsgas SSAB i Luleå använder malmpellets från LKAB för framställning av råjärn i masugn. För att omvandla malmpellets till råjärn i masugnen måste syret i pelletsen tas bort. Det kallas för reducering. Masugnsprocessen är en smältreduktionsprocess. Som reduktionsmedel används kol, med kemisk beteckning C, i form av koks och injektionskol. I reduktionsprocessen i masugnen reagerar syret i pelletsen och kolet till gas, kolmonoxid (CO) och koldioxid (CO2). Den bildade masugnsgasen innehåller ca 20-24% koloxid och ca 20-24% koldioxid. Masugnsgasen innehåller även ca 50% kvävgas och 2-4% vätgas och gasen leds från masugnen via grova gasrör till en gasreningsanläggning. Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
Blandgas vid SSAB i Luleå är en blandning av 60-100% masugnsgas, 0-40% LD-gas och 0-10% koksgas. Koksgas blandas in för att ersätta energi som försvinner vid låg LD-gas inblandning, max 10% då duken i gasklockan tar skada vid högre halt. Blandgasen lagras i en blandgasklocka och distribueras till LuleKraft AB (LUKAB) och Luleå Energi AB (LEAB). Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
SSAB I cowprarna används en blandning av koksgas och masugnsgas som energibärare för uppvärmning av blästerluften till masugnen. Blästerluft är uppvärmd luft som blåses in i masugnen med högt tryck. I kolinjektionen används koksgas som energibärare till varmluftsgeneratorer för uppvärmning av luft och för torkning och transport av kolpulver till masugnen. Referens = SSAB Luleå [chemfile(), chemdata.dat, referens i dokument]
Koksgas Koksgas är hälsofarligt genom gasens innehåll av koloxid, bensen och svavelväte. Gasen innehåller 2-3% bensen, som kan ge cancer (leukemi) vid långvarig exponering. Bensen är ett jämförelsevis starkt cancerframkallande ämne och vid långvarig exponering finns även risk för blodbrist (anemi) och ökad infektionskänslighet. Anemi är ett tillstånd där blodets förmåga att ta upp syre är nedsatt pga brist på röda blodkroppar. Koloxid är en färglös, luktlös och mycket giftig gas. Inandning av koloxid tränger undan syret i kroppen och det kan leda till koloxidförgiftning, som är en form av inre kvävning. Svavelväte är en färglös, mycket giftig gas med stark lukt. Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
[chemfile(), nr=CO-SSAB, f1=/produkt/chemdata.dat] Koloxid, stålindustrin Vid koks-, råjärns- och ståltillverkning bildas processgaser som innehåller bl a koloxid. Vid torrdestillation av kol till koks omvandlas 25% av kolet till sk rågas, som innehåller bl a koloxid. I reduktionsprocessen i masugnen reagerar syret i malmpelletsen och kolet till gaser, koloxid (CO) och koldioxid (CO2). I LD-konverter färskas råjärn till råstål, det innebär att syrgas blåses in i konvertern och syret reagerar med kolet i råjärn till koloxid (CO). Färskning är den process inom järnmetallurgin där kolhalten i råjärn sänks. Referens = SSAB Luleå [chemfile(), chemdata.dat, referens i dokument] [chemfile(), nr=CO-risk, f1=/produkt/chemdata.dat] Koloxid, risker I de röda blodkropparna finns det särskilda molekyler (hemoglobin) som har till uppgift att ta upp syre från luften i lungorna och transportera till kroppen olika delar. Koloxid binder sig mycket starkt till dessa molekyler och förhindrar dem då att transportera syre. Koloxidförgiftning är en form av inre kvävning. Redan mycket låga halter av koloxid i luften kan förorsaka syrebrist i kroppen. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), chemdata.dat, referens i dokument]
SSAB Kalk tillsätts i masugnsprocessen för att samla upp kisel och andra oönskade ämnen till en slagg. Slaggen består huvudsakligen av kisel och kalk samt aska från koks och kol. Kisel är rester från malmens gråberg. Askan i slaggen kan bl a innehålla sulfater (svavelföreningar) från kol och koks. Slaggen ligger ovanpå det flytande råjärnet. När råjärnet och slaggen tappas ur masugnen kan det bildas Referens = SSAB Luleå [chemfile(), file(), referens i dokument] Svaveldioxid [chemfile(), nC=0 nr=SO2, f1=/produkt/info/html/SO2.htm] Svaveldioxid (SO2) är en färglös gas med stickande lukt. Om gasen löses i vatten bildas svavelsyrlighet, som är en färglös och frätande syra, som är svagare än svavelsyra. Då svaveldioxid kommer i kontakt med fuktigheten i ögon och andningsvägarnas slemhinnor bildas svavelsyrlighet, som är starkt irriterande och frätande. Svaveldioxid som sugits upp i kläderna och förenats med vatten fräter på huden. Vid inandning påverkar svaveldioxid luftvägarna redan vid relativt låga halter, t ex ökar andningsmotståndet i luftvägarna. Astmatiker är särskilt känsliga för svaveldioxid. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument]
LD-gas 1) 1)
LD är en förkortning för Linz-Donawitz, efter de orter där tekniken först användes i fullskaledrift, och det är en process inom kategorin BOS (Basic Oxygen Steelmaking) med syrgasblåsning via lans. Referens = Jernkontoret, Stockholm [chemfile(), file(), referens i dokument] LD-gas bildas i LD-konvertern då råjärn färskas till råstål. Färskning är den process inom järnmetallurgin vid vilken kolhalten i råjärn sänks genom oxidation till de nivåer som gör järnet smidbart. Råjärnet som kommer direkt från masugnen innehåller vanligtvis ca 4-5% kol och är för sprött för att smidas, valsas eller härdas. Genom färskningen sänks kolhalten till under 2%, och järnet blir då smidbart. Genom en lans blåses 99% rent syrgas i konvertern och kolet som är löst i råjärnet reagerar med syre till koloxid (CO) och koldioxid (CO2) och råjärnet övergår i råstål då kolhalten har sänkts till under 2%. Gasen sugs från konvertern till gasreningssystemet med ett kraftigt fläktsystem. Luft från omgivningen sugs även med processgaserna till gasreningssystemet, vilket innebär att en del av koloxiden reagerar med luftens syre till koldioxid (CO2). I gasreningssystemet som är av typ våtgasrening renas gasen från stoft som följer med från konvertern. Som ett komplement till syrgasblåsning i LD-konverter finns bottenspolning med kvävgas (N2) eller argon (Ar), LBE - Lance Bubbling Equipment, för att bl a uppnå en mer effektiv omrörning. Halten av löst kväve i stålet bestämmer vilken spolgas, kvävgas (N2) eller argon (Ar), som används. En vanlig metod är att spola med kvävgas (N2) i början då kvävehalten i stålet är låg, för att sedan växla till argon (Ar) i slutet av blåsningen. Processgasen som bildas kallas för Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
[chemfile(), nr=CO-SSAB, f1=/produkt/chemdata.dat] Koloxid, stålindustrin Vid koks-, råjärns- och ståltillverkning bildas processgaser som innehåller bl a koloxid. Vid torrdestillation av kol till koks omvandlas 25% av kolet till sk rågas, som innehåller bl a koloxid. I reduktionsprocessen i masugnen reagerar syret i malmpelletsen och kolet till gaser, koloxid (CO) och koldioxid (CO2). I LD-konverter färskas råjärn till råstål, det innebär att syrgas blåses in i konvertern och syret reagerar med kolet i råjärn till koloxid (CO). Färskning är den process inom järnmetallurgin där kolhalten i råjärn sänks. Referens = SSAB Luleå [chemfile(), chemdata.dat, referens i dokument] [chemfile(), nr=CO-risk, f1=/produkt/chemdata.dat] Koloxid, risker I de röda blodkropparna finns det särskilda molekyler (hemoglobin) som har till uppgift att ta upp syre från luften i lungorna och transportera till kroppen olika delar. Koloxid binder sig mycket starkt till dessa molekyler och förhindrar dem då att transportera syre. Koloxidförgiftning är en form av inre kvävning. Redan mycket låga halter av koloxid i luften kan förorsaka syrebrist i kroppen. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), chemdata.dat, referens i dokument]
Koksgas Koksgas är hälsofarligt genom gasens innehåll av koloxid, bensen och svavelväte. Gasen innehåller 2-3% bensen, som kan ge cancer (leukemi) vid långvarig exponering. Bensen är ett jämförelsevis starkt cancerframkallande ämne och vid långvarig exponering finns även risk för blodbrist (anemi) och ökad infektionskänslighet. Anemi är ett tillstånd där blodets förmåga att ta upp syre är nedsatt pga brist på röda blodkroppar. Koloxid är en färglös, luktlös och mycket giftig gas. Inandning av koloxid tränger undan syret i kroppen och det kan leda till koloxidförgiftning, som är en form av inre kvävning. Svavelväte är en färglös, mycket giftig gas med stark lukt. Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
SSAB Koksgas används som energibärare i stationera för torkning och varmhållning av murade skänkar. Referens = SSAB Luleå [chemfile(), chemdata.dat, referens i dokument]
SSAB Koksgas används som energibärare i stationen för torkning och varmhållning av murade torpedon. Referens = SSAB Luleå [chemfile(), chemdata.dat, referens i dokument]
[chemfile(), nC=0 nr=1214-t, f1=/produkt/info/html/1214-t.htm] (RH)
RH-processen RH-processen är uppkallad efter de två företag, Ruhrstahl och Heraeus, som utvecklade den. 1)
ppm (parts per million) är en förkortning för miljondel på samma sätt som procent för hundradel och promille för tusendel. För att omvandla lufthalter av gaser och ångor mellan ppm och mg/m3 går det att räkna ut ett omvandlingstal genom att dividera ämnets molekylvikt med 24. T ex är molekylvikten 97 för diklormetylen (C2H2Cl2) och omvandlingstalet är då 4,0. För att omvandla från ppm till mg/m3 multipliceras ppm med omvandlingstalet. T ex är 20 ppm diklormetylen 20*4=80 mg/m3. För att omvandla från mg/m3 till ppm ska mg/m3 divideras med omvandlingstalet. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), file(), referens i dokument] Referens = Jernkontoret, Stockholm [chemfile(), file(), referens i dokument] Tillsatsen av legeringar kan ske automatiskt eller manuellt. Det finns en legeringssluss för tillsats av legeringar under vakuum. Referens = SSAB Luleå [chemfile(), file(), referens i dokument] I RH-anläggningen cirkulerar stålet under vakuumbehandlingen. Behandlingstiderna varierar beroende på stålsort och ståltemperatur. Efter behandlingen kan kolhalter <=20 ppm kol erhållas och vätehalter <=2 ppm väte. Vid vakuumbehandling av stål, i RH-anläggningen, kan följande fördelar nås - Avkolning till kolhalter under 0,003% kol (C) - Väterening till vätehalter under 2 ppm - Kväverening - Avskiljning av desoxidationsprodukter 1) i stål med höga krav på slaggrenhet - Hög träffsäkerhet vid justering av analys 1)
Desoxidation av stål är en teknik vid ståltillverkning, i vilken koncentrationen (aktiviteten) av syre löst i smält stål reduceras till en önskad nivå. Syre löst i en metallsmälta är ofta mycket skadligt i stål och brukar då avlägsnas (desoxidation) genom tillsats av ett element som bildar en stabil oxid, vilken samlas som slagg på smältans yta. Kisel (Si), aluminium (Al), natrium (Na), magnesium (Mg), kalcium (Ca), mangan (Mn) kan användas ofta som desoxiderare. En stålsmälta desoxideras framför allt med mangan (Mn) och kisel (Si) i vissa fall även med aluminium (Al). Referens = Jernkontoret Stockholm [chemfile(), file(), referens i dokument] Vid Från LD transporteras råstålet till RH-anläggningen, som är en station för vakuumbehandling av stål. Det låga trycket gör att kemiska reaktioner går fortare än vid atmosfärstryck. I RH processen utnyttjas undertryck för att påskynda reaktioner som är tryckberoende, som t ex bildandet av koloxid (CO). Omrörning av stålet sker genom spolning av argongas och legeringar tillsätts genom en legeringsficka i en syrefri miljö, vilket ökar legeringsutbytet. I RH processen tillverkas i huvudsak stålkvalitéer med ultralåg halt kol. Stålet kan också vakuumrenas från väte och kväve. Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
Skänkmetallurgi, CAS-OB (cas-ob) (cas-ob)
I Referens = Jernkontoret, Stockholm [chemfile(), file(), referens i dokument] Här sker den sista kemiska- och termodynamiska finjusteringen på stålet för att uppnå de analys- och temperaturkrav som gäller för den stålsort som ska produceras. Vid SSAB i Luleå är CAS-OB en skänkmetallurgianläggning med trådmatning och bulkmatning av legeringar. Här behandlas stålet till rätt temperatur och kemisk analys för leverans till stränggjutningen. Utrustning - Ferromangan (FeMn), - Ferrokisel (FeSi), - Kiselkarbid (SiC), - Ferroniob (FeNb), - Ferrovanadin (FeV), - Ferromolybden (FeMo), - Ferrotitan (FeTi) , - kol - Aluminium (Al), - Ferrobor (FeB), - Kalciumkisel (CaSi) - Instrument för mätning av temperatur och syreaktivitet - Utrustning för provtagning av stål - Processtyrningsutrustning - System för tillsättning av kylskrot - System för gasspolning via spolsten alternativt spollans - Tråd hasplas på i stora haspeltrummor och tillförseln av tråd ner i smältan kan ske med ett vanligt trådmatarverk Process - Skänken placeras i position - Argonspolning startas för att lösa upp hård slagg och för att homogenisera stålet i skänken - Nedsänkning av skyddsklockan - Temperaturmätning och första provet tas för kemisk analys - Eventuell justering av temperatur - Tillsats av legeringar enligt tillverkningsföreskrifter, t ex niob (Nb), mangan (Mn), titan (Ti), bor (B), aluminium (Al), och argonspolning. - Ny temperaturmätning och prov för kemisk analys - Då stålet i skänken har rätt temperatur och kemisk analys skickas den vidare till stränggjutning Processoperatören styr så att chargen (skänken) har rätt mängd legeringsämnen och temperatur för gjutning i stränggjutningen. Under större delen av processen spolas argon i botten av skänken för omrörning så att blandningen blir homogen samt för att transportera oönskade inneslutningar till slaggen. Vid SSAB i Luleå har varje stålsort ett unikt recept som måste följas exakt. Operatörerna använder datorer och laboratoriesvar från analysprover för att kontrollera att stålet innehåller rätt mängd av rätt ingredienser och har rätt temperatur. Legeringar I CAS-OB justeras stålet till rätt temperatur och kvalitet genom tillsatser av legeringsämnen och genom homogenisering. För att homogenisera stålet blåses argon in genom en spolsten i botten på skänken. Stålet kan värmas med syrgas och tillsats av aluminium eller kylas med stålskrot. Temperaturen justeras i skänken genom att samtidigt tillsätta aluminium och syrgas som ger en exoterm reaktion där aluminiumoxid (Al2O3) bildas. I den exoterma reaktionen när aluminium oxideras avges nödvändig energi direkt in i stålet. En exoterm reaktion är en kemisk reaktion där energi (oftast värme) avges. Referens = SSAB Luleå [chemfile(), file(), referens i dokument]
Inandning av respirabla partiklar av järn och järnoxid i rök- och damm under lång tid kan ge upphov till en form av dammlunga, som kallas järnlunga eller sideros. Referens = Litteratur om kemiska hälsorisker [chemfile() chemdata.dat (efter *)]
Mangan är ett ämne som används vid stålframställning och som ingår som legeringsämne i olika specialstål. Vid högre halter är mangan och manganföreningar starkt giftiga. De kan förorsaka allvarliga och obotliga skador i hjärna och nervsystem, samt nedsätta kroppens försvar mot infektioner i luftvägarna. Hygieniska nivågränsvärden (8 tim) för mangan är i totaldamm 0,2 mg/m3 och i respirabelt damm 0,1 mg/m3. I litteraturen framgår att förgiftning med mangan med symptom från nervsystemet kan uppkomma vid halter om 1-5 mg mangan/m3 luft. Förstatdier till symptomen kan uppkomma vid halter om 0,5-1 mg mangan/m3 luft. Det framgår också i litteraturen att förstadier till symptomen även kan uppkomma vid längre tids exponering för genomsnittshalter om 0,2-0,4 mg mangan/m3 luft. Det kan jämföras med att hygieniska nivågränsvärden (8 tim) för mangan är 0,2 mg/m3 i totaldamm och 0,1 mg/m3 i respirabelt damm. Mangan och manganföreningar skadar cellerna i andningsvägarna. Därigenom ökar risken för inflamationer avsevärt. Det finns risk för att mangandioxid akut kan ge upphov till lunginflammation. Inandning av höga halter mangan i damm och stoft kan ge upphov till metallröksfeber. Referens = Litteratur om kemiska hälsorisker [chemfile() chemdata.dat (efter *)]
Enligt uppgift i litteraturen kan titan anses vara en jämförelsevis oskadlig metall. Vid inandning av respirabelt titandioxid under lång tid inlagras dammet i lungorna, men detta tycks inte ge upphov till någon uppkomst av bindväv i lungorna (dammlunga). Referens = Litteratur om kemiska hälsorisker [chemfile() chemdata.dat (efter *)]
Inandning av aluminiumdamm, eller aluminiumhaltig rök, kan orsaka hosta och irritation i andningsvägarna. Långvarig upprepad exponering kan orsaka en form av dammlunga som kallas för aluminos. Aluminos uppkommer då inandade respirabla dammkorn som innehåller aluminium inlagras i lungorna. Respirabelt damm är partiklar som är så små så att de kan nå lungblåsorna (alveolerna). Vid exponering för respirabelt damm från aluminiummnineral, som bauxit och korund, under lång tid finns ochså risk för dammlunga av typ aluminos. I litteraturen framgår att eftersom aluminiummineral är förorenade med kiseldioxid vet man inte om det är aluminium eller silikosframkallande kvartsformer av kiseldioxid eller en kombination av båda som ger upphov till dammlungan. Referens = Litteratur om kemiska hälsorisker [chemfile() chemdata.dat (efter *)]
Kiseldioxid, SiO2 Kiseldioxid (SiO2) är en kemisk förening av kisel och syre och förekommer i naturen i flera olika former. De kan indelas i två typer, Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), chemdata.dat, referens i dokument] I naturen förekommer kiseldioxid bland annat i form av kvarts (lågkvarts), mineral med sammansättningen SiO2. Det förekommer i två modifikationer, alfa-kvarts (lågkvarts) och beta-kvarts (högkvarts). Lågkvarts är stabil vid temperaturer under 573 °C. Stabilitetsområdet för högkvarts är mellan 573 och 867 °C, varför detta mineral normalt inte förekommer inom den övre jordskorpan. Tridymit och kristobalit är högtemperatur polymorfer av kiseldioxid , vilket innebär att de har samma kemiska formel, SiO2, men med olika kristallstrukturer. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), chemdata.dat, referens i dokument]
Keramiska massor (gjutmassor, murbruk, sprutmassor, stampmassor) som innehåller kiseldioxid (SiO2) kan innehålla högkvarts (alfa-kvarts, kristobalit och tridymit). Dammande hantering, t ex blandning av produkter i pulverform, kan då medföra risk för kvartsexponering. Högkvarts kan bildas då keramiska massor som innehåller kiseldioxid utsätts för höga temperaturer i produktionsanläggningar, t ex i murade skänkar. Det innebär att mekanisk bearbetning av murad keramik, t ex rivning av skänkar, kan medföra risk för exponering för slilkosframkallande kvartsdamm. Om mängden högkvarts av kiseldioxid är mer än 3 vikt% i keramiska massor , klassificeras de som kvartshaltiga och då måste Arbetsmiljöverkets föreskrifter om kvarts tillämpas. Hälsorisker Högkvartsformer av kiseldioxid är alfa-kvarts, kristobalit och tridymit. Långvarig inandning av respirabelt damm som innehåller högkvarts kan ge upphov till en allvarlig form av dammlunga som kallas för silikos. Säkerhetsdatablad En del leverantörer anger i säkerhetsdatablad, i rubrik 3, om det finns kvartsformer av kiseldioxid i keramiska produkter. Det kan t ex stå att produkten innehåller <1% kvarts. Det innebär att halten högkvartsformer av kiseldioxid är mindre än 1%, dvs summan av alfa-kvarts, kristobalit och tridymit. Det kan även finnas med CAS-nr och EG-nr för kvarts i säkerhetsdatablad.
En del leverantörer skriver bara hur mycket kiseldioxid som ingår i produkten och då framgår inte mängden av de silikosframkallande kristallina formerna (högkvarts, kristobalit och tridymit). Referens = Litteratur om kemiska hälsorisker [chemfile() chemdata.dat (efter *)]
Inandning av respirabla partiklar av järn och järnoxid i rök- och damm under lång tid kan ge upphov till en form av dammlunga, som kallas järnlunga eller sideros. Referens = Litteratur om kemiska hälsorisker [chemfile() chemdata.dat (efter *)]
Koloxid bildas Koloxid (kolmonoxid) är en färglös, luktlös och mycket giftig gas. Den bildas vid förbränning med låg syretillförsel (ofullständig förbränning). Ju lägre syretillförsel, desto mer koloxid bildas. Koloxid är brandfarligt och bildar explosiva blandningar med luft. Inverkan av koloxid på kroppen I de röda blodkropparna finns det särskilda molekyler (hemoglobin) som har till uppgift att ta upp syre från luften i lungorna och transportera till kroppen olika delar. Koloxid binder sig mycket starkt till dessa molekyler och förhindrar dem då att transportera syre. Koloxidförgiftning är en form av inre kvävning. Redan mycket låga halter av koloxid i luften kan förorsaka syrebrist i kroppen. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), chemdata.dat, referens i dokument]
Inandning av respirabla partiklar av järn och järnoxid i rök- och damm under lång tid kan ge upphov till en form av dammlunga, som kallas järnlunga eller sideros. Referens = Litteratur om kemiska hälsorisker [chemfile() chemdata.dat (efter *)]
Mangan är ett ämne som används vid stålframställning och som ingår som legeringsämne i olika specialstål. Vid högre halter är mangan och manganföreningar starkt giftiga. De kan förorsaka allvarliga och obotliga skador i hjärna och nervsystem, samt nedsätta kroppens försvar mot infektioner i luftvägarna. Hygieniska nivågränsvärden (8 tim) för mangan är i totaldamm 0,2 mg/m3 och i respirabelt damm 0,1 mg/m3. I litteraturen framgår att förgiftning med mangan med symptom från nervsystemet kan uppkomma vid halter om 1-5 mg mangan/m3 luft. Förstatdier till symptomen kan uppkomma vid halter om 0,5-1 mg mangan/m3 luft. Det framgår också i litteraturen att förstadier till symptomen även kan uppkomma vid längre tids exponering för genomsnittshalter om 0,2-0,4 mg mangan/m3 luft. Det kan jämföras med att hygieniska nivågränsvärden (8 tim) för mangan är 0,2 mg/m3 i totaldamm och 0,1 mg/m3 i respirabelt damm. Mangan och manganföreningar skadar cellerna i andningsvägarna. Därigenom ökar risken för inflamationer avsevärt. Det finns risk för att mangandioxid akut kan ge upphov till lunginflammation. Inandning av höga halter mangan i damm och stoft kan ge upphov till metallröksfeber. Referens = Litteratur om kemiska hälsorisker [chemfile() chemdata.dat (efter *)]
Enligt uppgift i litteraturen kan titan anses vara en jämförelsevis oskadlig metall. Vid inandning av respirabelt titandioxid under lång tid inlagras dammet i lungorna, men detta tycks inte ge upphov till någon uppkomst av bindväv i lungorna (dammlunga). Referens = Litteratur om kemiska hälsorisker [chemfile() chemdata.dat (efter *)]
Inandning av aluminiumdamm, eller aluminiumhaltig rök, kan orsaka hosta och irritation i andningsvägarna. Långvarig upprepad exponering kan orsaka en form av dammlunga som kallas för aluminos. Aluminos uppkommer då inandade respirabla dammkorn som innehåller aluminium inlagras i lungorna. Respirabelt damm är partiklar som är så små så att de kan nå lungblåsorna (alveolerna). Vid exponering för respirabelt damm från aluminiummnineral, som bauxit och korund, under lång tid finns ochså risk för dammlunga av typ aluminos. I litteraturen framgår att eftersom aluminiummineral är förorenade med kiseldioxid vet man inte om det är aluminium eller silikosframkallande kvartsformer av kiseldioxid eller en kombination av båda som ger upphov till dammlungan. Referens = Litteratur om kemiska hälsorisker [chemfile() chemdata.dat (efter *)]
Kiseldioxid, SiO2 Kiseldioxid (SiO2) är en kemisk förening av kisel och syre och förekommer i naturen i flera olika former. De kan indelas i två typer, Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), chemdata.dat, referens i dokument] I naturen förekommer kiseldioxid bland annat i form av kvarts (lågkvarts), mineral med sammansättningen SiO2. Det förekommer i två modifikationer, alfa-kvarts (lågkvarts) och beta-kvarts (högkvarts). Lågkvarts är stabil vid temperaturer under 573 °C. Stabilitetsområdet för högkvarts är mellan 573 och 867 °C, varför detta mineral normalt inte förekommer inom den övre jordskorpan. Tridymit och kristobalit är högtemperatur polymorfer av kiseldioxid , vilket innebär att de har samma kemiska formel, SiO2, men med olika kristallstrukturer. Referens = Arbetsmiljö från A till Ö, SO Hansson, E Hellsten [chemfile(), chemdata.dat, referens i dokument]
Keramiska massor (gjutmassor, murbruk, sprutmassor, stampmassor) som innehåller kiseldioxid (SiO2) kan innehålla högkvarts (alfa-kvarts, kristobalit och tridymit). Dammande hantering, t ex blandning av produkter i pulverform, kan då medföra risk för kvartsexponering. Högkvarts kan bildas då keramiska massor som innehåller kiseldioxid utsätts för höga temperaturer i produktionsanläggningar, t ex i murade skänkar. Det innebär att mekanisk bearbetning av murad keramik, t ex rivning av skänkar, kan medföra risk för exponering för slilkosframkallande kvartsdamm. Om mängden högkvarts av kiseldioxid är mer än 3 vikt% i keramiska massor , klassificeras de som kvartshaltiga och då måste Arbetsmiljöverkets föreskrifter om kvarts tillämpas. Hälsorisker Högkvartsformer av kiseldioxid är alfa-kvarts, kristobalit och tridymit. Långvarig inandning av respirabelt damm som innehåller högkvarts kan ge upphov till en allvarlig form av dammlunga som kallas för silikos. Säkerhetsdatablad En del leverantörer anger i säkerhetsdatablad, i rubrik 3, om det finns kvartsformer av kiseldioxid i keramiska produkter. Det kan t ex stå att produkten innehåller <1% kvarts. Det innebär att halten högkvartsformer av kiseldioxid är mindre än 1%, dvs summan av alfa-kvarts, kristobalit och tridymit. Det kan även finnas med CAS-nr och EG-nr för kvarts i säkerhetsdatablad.
En del leverantörer skriver bara hur mycket kiseldioxid som ingår i produkten och då framgår inte mängden av de silikosframkallande kristallina formerna (högkvarts, kristobalit och tridymit). Referens = Litteratur om kemiska hälsorisker [chemfile() chemdata.dat (efter *)]
Gjutpulver används vid stålgjutning för att smörja kokillen, skydda smältan mot syre och värmeförlust, underlätta slaggbildning samt att ge stålet en för gjutningen lämplig viskositet. Gjutpulver kan delas upp i - Gjutpulver med alkaliska ämnen - Gjutpulver med starkt alkaliska ämnen - Gjutpulver med fluorider, med alkaliska ämnen - Gjutpulver med fluorider, med starkt alkaliska ämnen - Gjutpulver med med mer än 3% kvarts, med fluorider, med starkt alkaliska ämnen Hälsorisker Damm från gjutpulver som innehåller alkaliska ämnen, Damm från gjutpulver som innehåller Upprepad hudkontakt med gjutpulver kan orsaka hudirritation. Då gjutpulver som innehåller Koncentrerad fluorvätesyra är frätande medan utspädd fluorvätesyra kan hinna verka en lång stund t ex på huden innan man märker något. Ångor av vätefluorid och fluorvätesyra verkar i låga halter irriterande och i höga halter frätande på andningsvägar, ögon och hud. Koncentrerad fluorvätesyra är frätande medan utspädd fluorvätesyra kan hinna verka en lång stund t ex på huden innan man märker något. Referens = Järnbruksförbundets skyddsblad [chemfile(), file(), referens i dokument]
Täckmedel används vid stränggjutning och funktionen är att hindra en alltför snabb avkylning av smältan, skydda mot syre och ge en lämplig slaggbildning. Täckmedel kan delas upp i - Täckmedel utan hälsofarliga tillsatser - Täckmedel med starkt alkaliska ämnen - Täckmedel med mer än 3% kvarts - Täckmedel med fluor Hälsorisker - Dammande material - Damm som uppstår vid hantering kan ge upphov till irritation i ögonen och kan verka irriterande på luftvägarna - Damm som innehåller oorganiska fluorider kan orsaka irritation i ögonen och andningsvägarna. - Damm från täckmedel som innehåller alkaliska ämnen (kalciumoxid) i sådana mängder att pH i en mättad vattenlösning av produkten ligger mellan 10 och 12 kan orsaka irritation i ögonen, andningsvägar och på huden och risk för frätskador i ögonen kan inte uteslutas. Upprepad hudkontakt med täckmedel kan ge upphov till hudirritation. Då täckmedel som innehåller fluor kommer i kontakt med flytande stål kan hälsofarliga fluorföreningar bildas , t ex vätefluorid, som i kontakt med fuktig hud kan bilda fluorvätesyra. Om ångor av vätefluorid kommer i kontakt med fuktig hud, ögon eller slemhinnor bildas fluorvätesyra. Ångor av vätefluorid och fluorvätesyra verkar i låga halter irriterande och i höga halter frätande på andningsvägar, ögon och hud. Koncentrerad fluorvätesyra är frätande medan utspädd fluorvätesyra kan hinna verka en lång stund innan det ger upphov till symptom. Referens = Järnbruksförbundets skyddsblad [chemfile(), file(), referens i dokument]
Då gjutpulver tillsätts i kokillen kan det uppstå mycket rök och damm från kokillen. Stoftets innehåll är beroende på gjupulvrets sammansättning. T ex om det finns fluor i gjutpulvret kan röken innehålla hälsofarliga fluorämnen. I rubrik 3 i säkerhetsdatablad framgår produktens sammansättning. Om det står att produkten innehåller flusspat, kryolit eller att det står att ämnet är en fluorförening finns risk att det bildas hälsofarliga fluorämnen då produkten tillsätts i processen. I säkerhetsdatablad, i rubrik 3, brukar det även stå CAS-nr och EG-nr för ämnen. Flusspat har CAS-nr=7789-75-5 och EG-nr=232-188-7. Kryolit har CAS-nr=15096-52-3 och EG-nr=239-148-8. En del leverantöer skriver inte alltid CAS-nr och EG-nr i säkerhetsdatablad. Referens = Litteratur om kemiska hälsorisker [chemfile(), file(), referens i dokument]
Täckmedel brukar vara förpackade i plastpåsar. Men det kan finnas damm på påsarna och det kan finnas trasiga påsar och då kan det uppstå damm då täckmedlet kastas i gjutlådan. Om täckmedel innehåller kalciumkarbonat eller kalciumoxid är dammet starkt irriterande och vid höga halter kan det finnas risk för frätskador om damm kommer i kontakt med ögon. Täckmedel kan innehålla fluor och då kan det också bildas hälsofarliga fluorämnen då täckmedlet kastas i gjutlådan. I rubrik 3 i säkerhetsdatablad framgår produktens sammansättning. Om det står att produkten innehåller flusspat, kryolit eller att det står att ämnet är en fluorförening finns risk att det bildas hälsofarliga fluorämnen då produkten tillsätts i processen. I säkerhetsdatablad, i rubrik 3, brukar det även stå CAS-nr och EG-nr för ämnen. Flusspat har CAS-nr=7789-75-5 och EG-nr=232-188-7. Kryolit har CAS-nr=15096-52-3 och EG-nr=239-148-8. En del leverantöer skriver inte alltid CAS-nr och EG-nr i säkerhetsdatablad. Referens = Litteratur om kemiska hälsorisker [chemfile(), file(), referens i dokument] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||