 typ av folder som betyder, klicka på rubrik - öppnar flik med info
typ av folder som betyder, klicka på rubrik - öppnar flik med info  typ av folder som betyder, klicka på rubrik - stänger flik med info
typ av folder som betyder, klicka på rubrik - stänger flik med info Till rubrik kan det finnas underrubrik, klicka på samma sätt där för att
öppna
 eller stänga
eller stänga  flik med info.
flik med info. | Loading .... [chempa.prj, /produkt/info/html/chem-oi.htm -> /produkt/html/data/chem-oi.php] .... ok |
 typ av folder som betyder, klicka på rubrik - öppnar flik med info typ av folder som betyder, klicka på rubrik - öppnar flik med info  typ av folder som betyder, klicka på rubrik - stänger flik med info typ av folder som betyder, klicka på rubrik - stänger flik med info Till rubrik kan det finnas underrubrik, klicka på samma sätt där för att öppna  eller stänga eller stänga  flik med info. flik med info. |
Introduktion till organisk kemi
Organisk kemi Organisk kemi är kolföreningarnas kemi. Alla organiska föreningar innehåller kol (C). Praktiskt taget alla innehåller också väte (H). Syre (O) och kväve (N) ingår ofta i organiska föreningar medan svavel (S), fosfor (P)och halogener är mindre vanliga. En kolatom har fyra valenselektroner. Den måste, för att erhålla ädelgasstruktur, dela fyra elektronpar med andra atomer, dvs ha fyra kovalenta bindningar. Kolatomen har förmåga att binda andra kolatomer och därigenom bilda molekyler som består av långa kedjor. De fyra valenselektronerna i kol gör att kol kan bilda i princip oändligt antal föreningar. Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), file(), referens i dokument] Indelning Kolatomer kan bilda starka kovalenta bindnningar (elekronparbindningar) till andra kolatomer och även till andra icke-metaller t ex väte (H), syre (O), Kväve (N) och svavel (S). Varje kolatom kan bilda maximalt fyra bindningar, en dubbelbindning räknas som två och en trippelbindning som tre bindningar. Organiska föreningar med samma molekylformel kan ha mycket varierande struktur och egenskaper. För att kunna hålla reda på alla organiska föreningar delas de i grupper enligt två olika system. Det ena bygger på kolkedjans uppbyggnad, medan det andra utgår från de funktionella grupper föreningarna innehåller. Indelningen efter funktionell grupp är mest praktiskt då föreningarnas egenskaper diskuteras, eftersom en viss funktionell grupp reagerar på likartad sätt oavsett molekylernas kolkedja. En Vid namngivningen utgås emellertid från kolkedjan och den funktionella gruppen anges med en ändelse. Referens = Organisk kemi, Studentlitteratur AB Lund, U Ellenvik, O Sterner, N Kann [chemfile(), file(), referens i dokument]
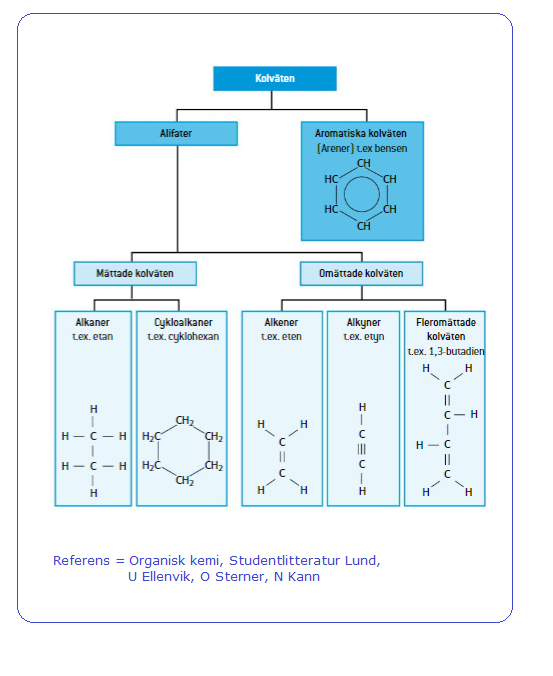
[chemfile(), nC=0 nr=chem-c, f1=/produkt/info/html/chem-c.htm] Kolväten Kemiska föreningar (molekyler) i vilka endast kol och väte ingår kallas 1) Cykliska kolväten består av kol och väte som bildar en sluten ring Kolväten kan delas in i olika ämnesgrupper beroende på struktur och egenskaper, de är
1) 2)
- I 2) - Bensen är en aromatisk förening som har sex kolatomer och sex väteatomer (C6H6). - Bensenderivat är föreningar som liknar bensen (dvs ihopsatta bensenringar). - Polyaromater är kolväten med minst två sammankopplade aromatiska ringar (bensenringar), polyaromatiska kolväten kallas också PAH (Polycyclic Aromatic Hydrocarbons). - Aromatiska kolväten kallas också aromater eller arener och de är kolväten som byggs upp av en ring med sex kol och det finns en dubbelbindning till vart annat kol. Referens = Linköpings universitet, istitutionen för Fysik, Kemi och Biologi [chemfile(), file(), referens i dokument]
Alifatiska och aromatiska föreningar Alkaner, alkener och alkyner är Föreningar som inte är aromatiska kallas för Alifatiska kolväten är kolväten vars molekyl är öppen och inte sluten i en ring (cykliska kolväten). Oktan är ett exempel på ett alifatiskt kolväte, cyklohexan är däremot ett cykliskt ämne. Alkaner är mättade alifatiska kolväten, med bara enkelbindningar. Alkener och alkyner är omättade alifatiska kolväten, med dubbel- respektive trippelbindningar. Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), file(), referens i dokument] Kolväten kan delas in i olika ämnesgrupper beroende på struktur och egenskaper, de är
Referens = Linköpings universitet, istitutionen för Fysik, Kemi och Biologi [chemfile(), file(), referens i dokument] 1) 2)
- I 2) - Bensen är en aromatisk förening som har sex kolatomer och sex väteatomer (C6H6). - Bensenderivat är föreningar som liknar bensen (dvs ihopsatta bensenringar). - Polyaromater är kolväten med minst två sammankopplade aromatiska ringar (bensenringar), polyaromatiska kolväten kallas också PAH (Polycyclic Aromatic Hydrocarbons). - Aromatiska kolväten kallas också aromater eller arener och de är kolväten som byggs upp av en ring med sex kol och det finns en dubbelbindning till vart annat kol. Referens = Linköpings universitet, istitutionen för Fysik, Kemi och Biologi [chemfile(), file(), referens i dokument]
Funktionella grupper (ämnesklasser) En funktionell grupp är i kemin en sammanhängande grupp av atomer som tillsammans utgör en (oftast mindre) del av en molekyl och som på ett avgörande sätt påverkar molekylens egenskaper. Genom att byta ut väteatomer (H) i kolväten mot olika funktionella grupper bildas en mycket stor mängd klasser av ämnen. T ex ger den funktionella gruppen -OH kopplat till en kolvätekedja, en alkohol. Karboxylgruppen -COOH ger en karboxylsyra, osv. R= generell kolvätekedja (alkyl) eller Ar = aromat Z= Funktionell grupp, t ex -Cl, -OH, -COOH, -NH2 Föreningars egenskaper bestäms av Z-gruppen och i mindre grad av R-gruppen (smältpunkt, kokpunkt, löslighet, reaktivitet m.m.). Olika R-grupp med samma funktionell grupp (Z) bildar föreningar med liknande kemiska egenskaper. T ex metanol, etanol, propanol ...... Referens = Linköpings universitet, institutionen för Fysik, Kemi och Biologi [chemfile(), file(), referens i dokument]
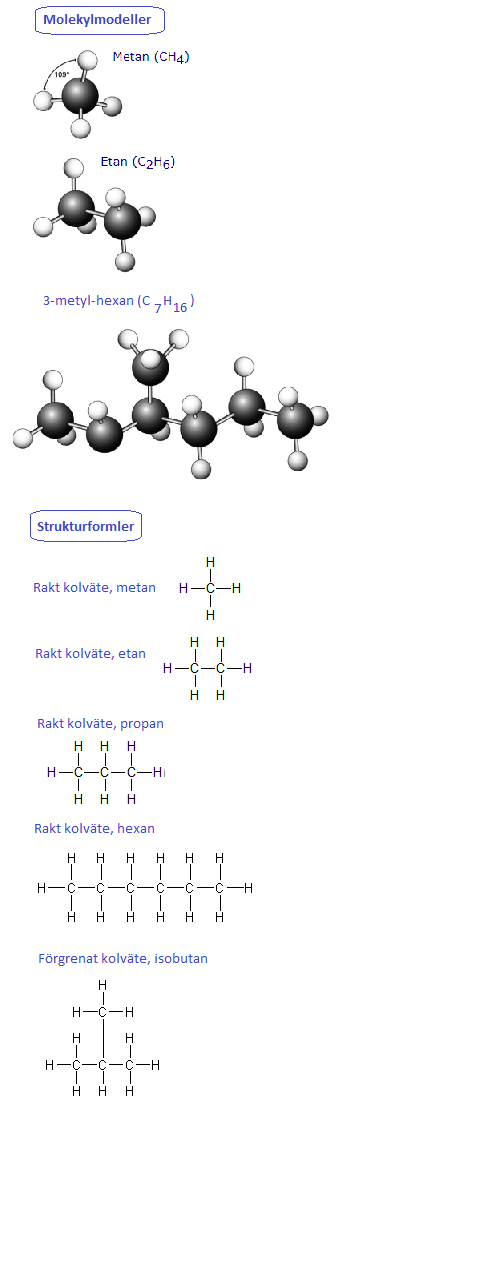
Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), file(), referens i dokument] - Metan (CH4) - Etan (C2H6) - Propan (C3H8) - Butan (C4H10) Referens = Linköpings universitet, istitutionen för Fysik, Kemi och Biologi [chemfile(), file(), referens i dokument]

Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), file(), referens i dokument] Ett kolväte med en dubbelbindning kallas omättat eftersom det han ta upp två atomer, t ex väte eller en halogen. Diener har två dubbelbindningar och triener har tre. Kolväten med mer än en dubbelbindning kallas fleromättade och det känns igen från diskussioner om nyttiga fetter. Referens = naturvetenskap.nu [chemfile(), file(), referens i dokument] Referens = Linköpings universitet, istitutionen för Fysik, Kemi och Biologi [chemfile(), file(), referens i dokument]
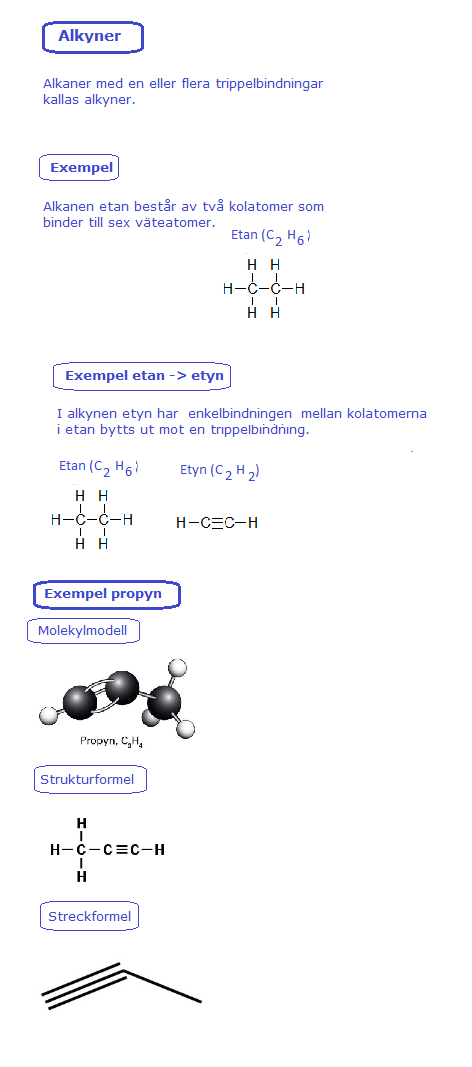
Referens = naturvetenskap.nu [chemfile(), file(), referens i dokument] Referens = Linköpings universitet, istitutionen för Fysik, Kemi och Biologi [chemfile(), file(), referens i dokument]
Aromatiska föreningar 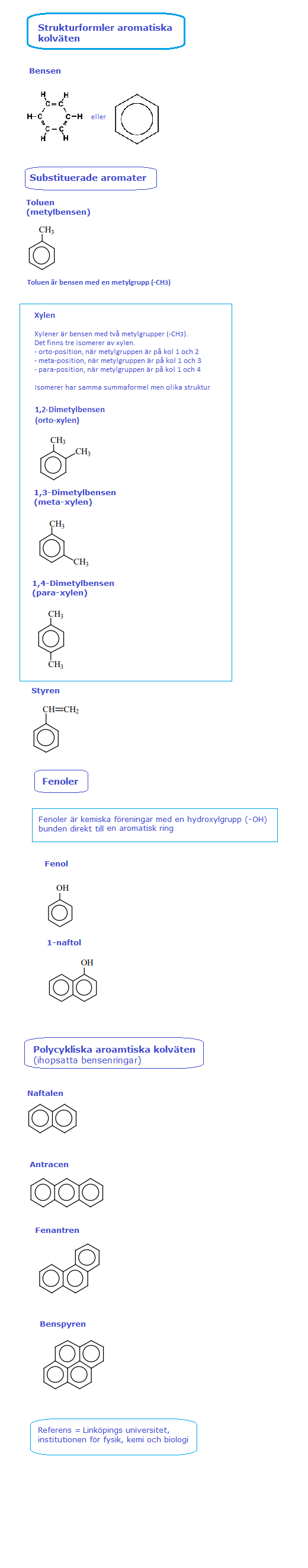
Råvaror till aromatiska föreningar är främst stenkol och petroleum. Genom torrdestillation 1) av stenkol erhålls koks och stenkolstjära. Vid fraktionerad destillation av stenkolstjära erhålls bensen, toluen, xylener, fenol, kresoler, naftalen etc. Bensenföreningar produceras också genom dehydrogenering av cykliska föreningar som erhålls från petroleum. Bensen och flertalet av dess derivat är hydrofoba föreningar. De är alltså olösliga i vatten men goda lösningsmedel för organiska föreningar. 1) Referens = Biokemi med organisk kemi, O Nylander [chemfile(), file(), referens i dokument] Aromatiska föreningar är cykliska kolväteföreningar 1) med en, eller flera, bensenringar. Bensen är den enklaste aromaten, och den har sex kolatomer och sex väteatomer (C2H6). Gruppen inkluderar PAH, polycykliska aromatiska kolväten som består av tre eller flera kondenserade bensenringar 2) med enbart kol och väte. Föreningar som inte är aromatiska kallas alifatiska (de har raka kolkedjor).
Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), file(), referens i dokument] 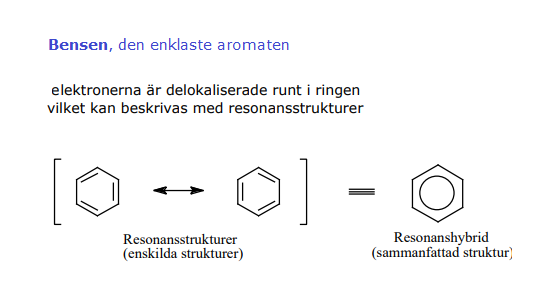
Alkoholer 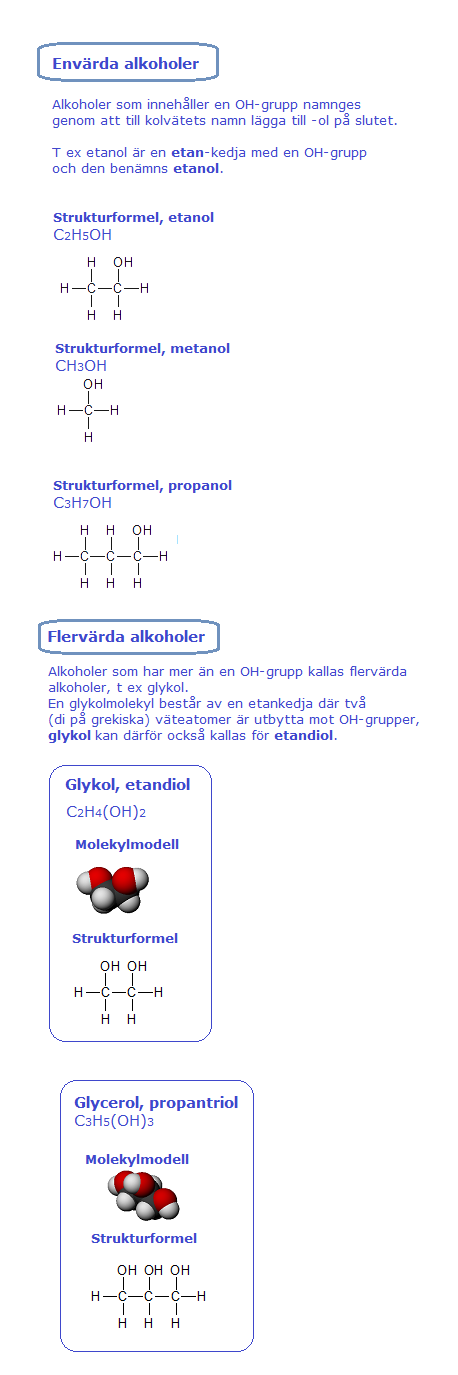
Alkoholer är organiska ämnen där en eller flera hydroxylgrupper (OH) är bundna till kolatomer i en kolkedja. Den enklaste alkoholen är metanol (CH3OH) med enbart en kolatom och en OH-grupp. Det ämne som oftast kallas alkohol i vardagsspråk är etanol (CH3CH2OH).
Genom att byta ut väteatomer i kolväten mot olika funktionella grupper bildas en mycket stor mängd klasser av ämnen. T ex ger den funktionella gruppen -OH kopplat till en kolvätekedja, en alkohol. Karboxylgruppen -COOH ger en karboxylsyra, osv. Alkaner, alkener, alkyner, cykloalkaner och andra organiska föreningar kan bilda alkoholer. Föreningar med en hydroxigrupp (OH) bunden till aromatiskt bundna kolatomer, såsom en bensenring, kallas däremot inte alkoholer utan fenoler, bensendioler osv. Indelning av alkoholer Alkoholerna kan indelas efter olika principer. En grund för indelning är efter - Alkoholer med en OH-grupp kallas - Alkoholer med två OH-grupper kallas - Alkoholer med tre OH-grupper kallas Ett annat sätt att indela alkoholer är i Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), file(), referens i dokument] - Envärda alkoholer indelas i primära, sekundära och tertiära alkoholer. - Primära alkoholer (normalalkoholer) innehåller gruppen -CH2-OH, hydroxylgruppen (-OH) är bunden till en kolatom, som binder en annan kolatom. - Sekundära alkoholer innehåller gruppen -|CH-OH, hydroxylgruppen är bunden till en kolatom, som binder två andra kolatomer. - Tertiära alkoholer innehåller gruppen -||CH-OH, hydroxylgruppen är bunden till en kolatom, som binder tre andra kolatomer. Referens = Biokemi med organisk kemi, O Nylander [chemfile(), file(), referens i dokument]
Karboxylsyror Karboxylsyra är en organisk syra som innehåller den funktionella gruppen (-COOH). Referens = Analytisk kemi Umeå universitet [chemfile(), file(), referens i dokument] Karboxylgruppen (-COOH) är den funktionella grupp, som ger karboxylsyrorna deras karakteristiska egenskaper. Karboxylgruppen består av en karbonylgrupp (en kolatom som har en dubbelbindning till en syreatom, -C=O) och en hydroxigrupp (-OH). Karboxylsyrorna namges genom att ändelsen -syra läggs till namnet för motsvarande kolväte. För den enklaste syran med endast en kolatom blir det systematiska namnet metansyra.
En del karboxylsyror, t ex palmetinsyra och stearinsyra, kan erhållas genom att fetter sönderdelas. De kallas därför Exempel på en aromatisk karboxylsyra är bensoesyra (C6H5COOH). Bensoesyra förekommer naturligt i bl a lingon och hjortron där det fungerar som konserveringsmedel. Ättiksyra, som är vanligt i hushållet, har en stickande lukt. Smörsyra, som bl a bildas då smör härsknar, är mycket illaluktande. Myrsyra, som finns i giftkörtlarna hos rödmyran och orsakar sveda vid dess bett, har även den mycket stickande lukt. Myrsyra används för konservering av grönfoder (ensilage). Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), file(), referens i dokument]
Estrar Då en karboxylsyra reagerar med en alkohol sker reaktionen, karboxylsyra + alkohol -> ester + vatten Det här är ett exempel på en Den bildade produkten är en Det är estrar som ger många frukter deras karakteristiska lukter. Estrar som är lätta att framställa i stora mängder används som lösningsmedel i t ex färger och som mellanprodukter i organisk syntes. De utnyttjas även inom parfymindustrin och för att smaksätta godis, bakverk och läskedrycker. Estrar bildar inte vätebindningar och har därför lägre smält- och kokpunkter än alkoholer och karboxylsyror med motsvarande molekylmassor. De är också mindre vattenlösliga än alkoholer och karboxylsyror. Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), file(), referens i dokument]
Aldehyder och ketoner En aldehyd är en oxidationsprodukt av en primär alkohol (alkohol med en OH-grupp) 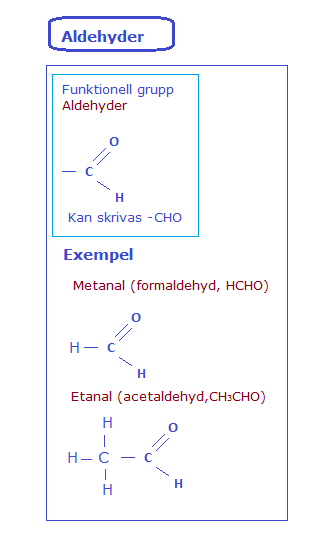
Närbesläktade till aldehyderna är ketonerna, som bildas då sekundära alkoholer oxideras (alkoholer med två OH-grupper). 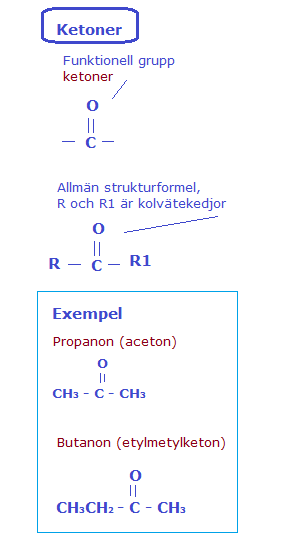
Referens = Biokemi med organisk kemi, O Nylander [chemfile(), file(), referens i dokument] Många naturligt förekommande ämnen är aldehyder och ketoner. De har ofta angenäm lukt och utgör de aktiva komponenterna i naturligt doftande ämnen. De används därför ofta i parfymer och för att ge frisk doft inomhus. Mogna hallon innehåller många olika aldehyder och ketoner och alkoholer. Aldehydens karbonylgrupp 1) binder en alkylgrupp (kolvätekedja) och en väteatom. En keton har två alkylgrupper (kolvätekedjor) bundna till karbonylgruppen. 1)
Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), file(), referens i dokument]
Kolhydrater Det mesta av kolhydraterna bryts ner i kroppen till sockerarten 1)
Socker är ett samlingsnamn för flera olika sockerarter. Olika sockerarter finns naturligt i frukt, bär och mjölk. Referens = Livsmedelsverket [chemfile(), file(), referens i dokument] Sockerarterna delas upp i enkla (monosackarider) och sammansatta sockerarter (disackarider). De här enkla sockerarterna kan också sitta ihop två och två. Då kallas de för Laktos (mjölksocker) består av glukos och galaktos, och är en disackarid som finns naturligt i mjölk. Referens = www.arla.se, hälsa, hälsosam mat, näringsamnen, kolhydrater, socker [chemfile(), file(), referens i dokument] Fotosyntesen Fotosyntesen kan enkelt förklaras med att växten tar in koldioxid, vatten och solenergi som den sedan omvandlar till syre och glukos. Syre och glukos (druvsocker) kan växten sedan använda under natten och under dagen vid cellandningen. I växternas gröna blad förenas koldioxid (CO2) och vatten (H2O) till Vid fotosyntesen bildas mer glukos (druvsocker) än vad växterna behöver. Överskottet lagras som stärkelse, som är uppbyggt av grenade och ogrenade kedjor av glukos. Tusentals glukosmolekyler bildar Glukosmolekyler, förenade på ett något annorlunda sätt, bildar 1) Prefixen mono- respektive di- anger hur många sockerenheter (ringar av kolatomer) sockermolekylen består av, De vanligaste monosackariderna är De vanligaste disackariderna är Referens = Biokemi med organisk kemi, O Nylander [chemfile(), file(), referens i dokument]
Proteiner Protein brukar kallas för kroppens byggstenar. Det behövs bland annat för att bygga upp celler och för att bilda enzymer och hormoner 1) och proteiner finns i större eller mindre mängd i nästan all mat. Protein byggs upp av cirka 20 aminosyror. Nio av dem är essentiella, dvs de måste tillföras via maten eftersom kroppen inte själv kan producera dem. Protein ingår i kroppens alla vävnadsceller. Dessutom består hormoner, enzymer 1) och viktiga delar i immunförsvaret av proteiner. Protein är därför viktigt för hela kroppens funktion. 1) Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), file(), referens i dokument] Aminosyror Aminosyror innehåller både en bas (NH2-gruppen) och en syra (COOH-gruppen). Referens = Livsmedelsverket [chemfile(), file(), referens i dokument]
Fetter Den energi som kroppen inte utnyttjar lagras dels som kolhydrat (glykogen) och dels som fett. Fetter är estrar av en molekyl av den trevärda alkoholen glycerol och tre fettsyramolekyler. Reaktionen är glycerol + fettsyra -> naturligt fett + vatten. Då en karboxylsyra reagerar med en alkohol bildas en ester. De flesta naturliga fetter är blandade triglycerider 1), dvs en fettmolekyl är uppbyggd av två eller tre olika fettsyror. Fettsyrorna i fetter har oftast 16 eller 18 kolatomer. 1)
Fettsyrorna kan vara Ur hälsosynpunkt anses det bättre att konsumera fetter av fleromättade fettsyror (fetter med flera dubbelbindningar) än av mättade. Orsaken är att de mättade fetterna i större utsträckning leder till att fett upplagras i blodkärlen. Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), file(), referens i dokument]
Tvål och såpa Tvål och såpa är salter av karboxylsyror 1). De fungerar som tvättmedel, därför att de har en vattenlöslig och en fettlöslig del. Sådana ämnen är ytaktiva och kallas 1)
Tvättmedlet ska lösa upp vattenolösliga delar, dvs feta ämnen. Det ytaktiva ämnet orienterar sig i en fettfläck så att kolkedjan vandrar in i fettet medan den laddade delen stannar utanför. När tvätten sköljs med vatten följer den vattenlösliga änden av tvättmedelet med och även resten av molekylen, som tar med sig fettet i fläcken. Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), file(), referens i dokument] [chemfile(), nC=0 nr=wash_-o, f1=/produkt/info/html/wash_-o.htm] Ytaktiva ämnen En Synonyma betecknngar till Ytaktiva ämnen klassificeras efter den hydrofila gruppens karaktär. Tvålar Praktiskt taget alla tvålar har som huvudbeståndsdel Natriumstearat (Na(CH3(CH2)16COO) som är natriumsaltet av stearinsyra. Stearinsyra eller oktadekansyra (CH3(CH2)16COOH eller C17H35COOH) är en mättad fettsyra med 18 kolatomer. Salter 1) av stearinsyra får suffixet (ändelse) stearat. 1)
Vid motsvarande tillverkning av såpa används kaliumhydroxid (kalilut) istället för natriumhydroxid. Tvål och såpa är alltså salter av natrium respektive kalium med fettsyror. En fettsyra har en fettlöslig del (svans) och en vattenlöslig del (huvud) och det är den vattenlösliga delen som skapar saltet. Det gör så att tvålmolekyler kan bindas samman med den feta smutsen samtidigt som den kan lösas upp i vatten. Hydrolys är en kemisk process där en molekyl klyvs i två delar efter att en vattenmolekyl har adderats. Vanliga ämnen i pulvertvättmedel Ytaktiva ämnen kallas även surfaktanter, tensider eller detergenter och de har egenskaper som kan göra smuts som består av fett vattenlösligt. De sänker även vattnets ytspänning vilket ökar vattnets tvättverkan. Vanliga vattenavhärdande medel är fosfater av olika slag. De fosfater som framförallt används är tripolyfosfat och pyrofosfat och de tillförda fosfaterna har en gynnsam inverkan på det ytaktiva ämnets effekt och verkar dispergerande (finfördelande) på den lossade smutsen. Fosfaterna gör hårt vatten mjukare genom att binda kalcium - och magnesiumjoner. I många tvättmedel har fosfat helt bytts ut mot zeolit. Zeoliter finns i naturen men framställs framförallt syntetiskt (kemiskt). De är salter (jonföreningar) av aluminiumsilikat med formeln Na12(Al12Si12O48)*27H2O och fungerar som jonbytare genom att byta ut de hårda kalcium (Ca2+)- och magnesiumjonerna (Mg2+) mot den mjukare natriumjonen (Na+). På så sätts mjukgörs hårt vatten. Vattenavhärdande ämnen ökar även tensidernas effektivitet och hindrar uppkomsten av bl a kalktvål och andra svårlösliga salter som kan skada både tvätten och tvättmaskinen. Blekmedel används i vittvättmedel där det bleker bort svårlösliga fläckar. Fläckar (t ex färgade ämnen) som inte kan avlägsnas genom tvättning, bleks bort av t ex natriumperborat. För att avlägsna närvarande joner av tunga metaller (t ex järn- och kopparjoner) tillsätts magnesiumsilikat och EDTA (etykendiamintetraättiksyra). De här jonerna skulle tilsammans med blekmedel annars skada textilfibrerna. Enzymer ingår i många tvättmedel. Proteaser, amylaser och lipaser bryter ner proteiner, stärkele och fetter som finns i fläckar av bl a mat, svett, choklad och smuts på skjortkragar. När enzymer utnyttjas kan tvättprocessen ske vid lägre temperatur. Karboxylmetylcellulosa adsorberas både på textilmaterialet och på den frigjorda smutsen och förhindrar löstvättad smuts att utfällas på fibern igen. Tvättprocessen ur fysikalisk kemisk synpunkt Smutsen som ska avlägsnas består av fett, proteiner, färgämnen diverse partiklar t ex damm samt vattenlösliga ämnen som salter, sockerarter, fruktsyror etc. Allmänt kan sägas att det finns smuts av både hydrofob och hydrofil karaktär 1). Ytaktiva ämnen tvättverkan består i att de sänker ytspänningen vid vattenlösningens gränsytor mot omgivande medier (luft, textilmaterial samt fett och andra typer av smuts). Tvättmedlets molekyler kommer på det sättet i omedelbar kontakt med smutsen och de kommer att orientera sig allt efter smutskomponenternas hydrofoba och hydrofila karaktär 1). Det betyder att den ytaktiva molelylens hydrofoba del kommer att bindas till smuts av fettyp och den hydrofila delen binds till smuts som består av t ex proteiner och andra ämnen av hydrofil karaktär.
Referens = Biokemi med organisk kemi, O Nylander [chemfile(), file(), referens i dokument]
Fenoler är svaga syror Ämnesklassen fenoler kännetecknas av en eller flera hydroxigrupper (-OH) bundna till en aromatföring (bensenring). Anledningen till att fenoler betraktas som en egen ämnesklass är att deras kemiska egenskaper skiljer sig väsentligt från alkoholernas. Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), file(), referens i dokument]
Polymerer Polymerer bildas genom att många små enheter, monomerer, bildar stora molekyler, där atomerna hålls ihop av kovalenta bindningar 1). Polymererna har således stora molekylmassor. Reaktionen som sker när monomererna blir en polymer kallas polymerisation. 1)
Det är den kemiska strukturen som avgör ett ämnes egenskaper. Naturgummi är en naturlig polymer från gummiträd. Syntetiskt gummi (tillverkad gummi) har en liknande struktur som naturgummi och därmed liknande egenskaper. Plaster Plaster är syntetiska polymerer (tillverkade polymerer). De kan delas in på olika sätt, dels efter egenskaper, dels efter framställningsmetoder. Indelning efter egenskaper är Termoplaster mjuknar vid uppvärmning men återfår sina ursprungliga egenskaper då den återgår till normal temperatur. Härdplaster mjuknar först vid så hög temperatur att de samtidigt sönderdelas. Termoplaster är lösliga i lösningsmedel medan härdplaster är olösliga. Skillnader i egenskaper beror på att polymererna har olika struktur. Termoplasterna har linjär eller något grenad struktur. Till termoplasterna hör elastiska material t ex polyeten och nylon. Termoplaster mjuknar och smälter lätt och kan därför omformas i värme. Härdplasterna har nätstruktur med starka bindningar i tre dimensioner. Det gör att de inte mjuknar vid uppvärmning. Exempel på en härdplast är bakelit. För att göra plasten hård och slitstark tillsätts fyllmedel. Vanliga fyllmedel är trämjöl eller vanlig cellulosa. Mjukgörare tillsätts för att plasten ska bli smidig och mjuk, t ex i regnkappor. De vanligaste mjukgörarna är olika estrar av ftalsyra (bensen-1,2-dikarboxylsyra) 1). Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), file(), referens i dokument] 1)
Ftalsyra (bensen-1,2-dikarboxylsyra), formel = C6H4(COOH)2 Referens = Kemiboken A, H Boren, M Larsson, T Liif, S Lilieborg, B Lindh [chemfile(), file(), referens i dokument] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||